Clear Sky Science · it
LAP2α guida la tumorigenesi mammaria attenuando lo stress di replicazione
Perché questo è importante per il cancro al seno
I tumori mammari crescono in parte perché le cellule cancerose trovano modi per sopravvivere allo stress costante durante la copia del DNA. Questo studio rivela come una proteina meno nota, chiamata LAP2α, aiuti le cellule del cancro al seno a proteggere il loro DNA durante la replicazione, promuovendo così la crescita del tumore e rendendo i tumori più difficili da trattare. Comprendere questo sistema di supporto nascosto suggerisce nuove strategie per indebolire i tumori e migliorare l’efficacia dei farmaci esistenti.
Un aiutante nascosto all’interno dei nuclei delle cellule tumorali
Ogni volta che una cellula si divide, deve copiare accuratamente il proprio DNA. Nelle cellule tumorali questo processo è particolarmente sotto pressione: i segnali di crescita rimangono “accesi” e la macchina di replicazione viene spinta al limite. Questa pressione, nota come stress di replicazione, lascia tratti di DNA a filamento singolo che devono essere rapidamente rivestiti e stabilizzati da un complesso proteico chiamato RPA. Gli autori avevano precedentemente scoperto che LAP2α, una proteina legata all’impalcatura interna del nucleo, può legare RPA e aiutarla a raggiungere il DNA danneggiato. Nel lavoro presente si sono chiesti se questa collaborazione LAP2α–RPA alimenti effettivamente lo sviluppo dei tumori mammari e influisca sulla risposta dei tumori ai trattamenti.
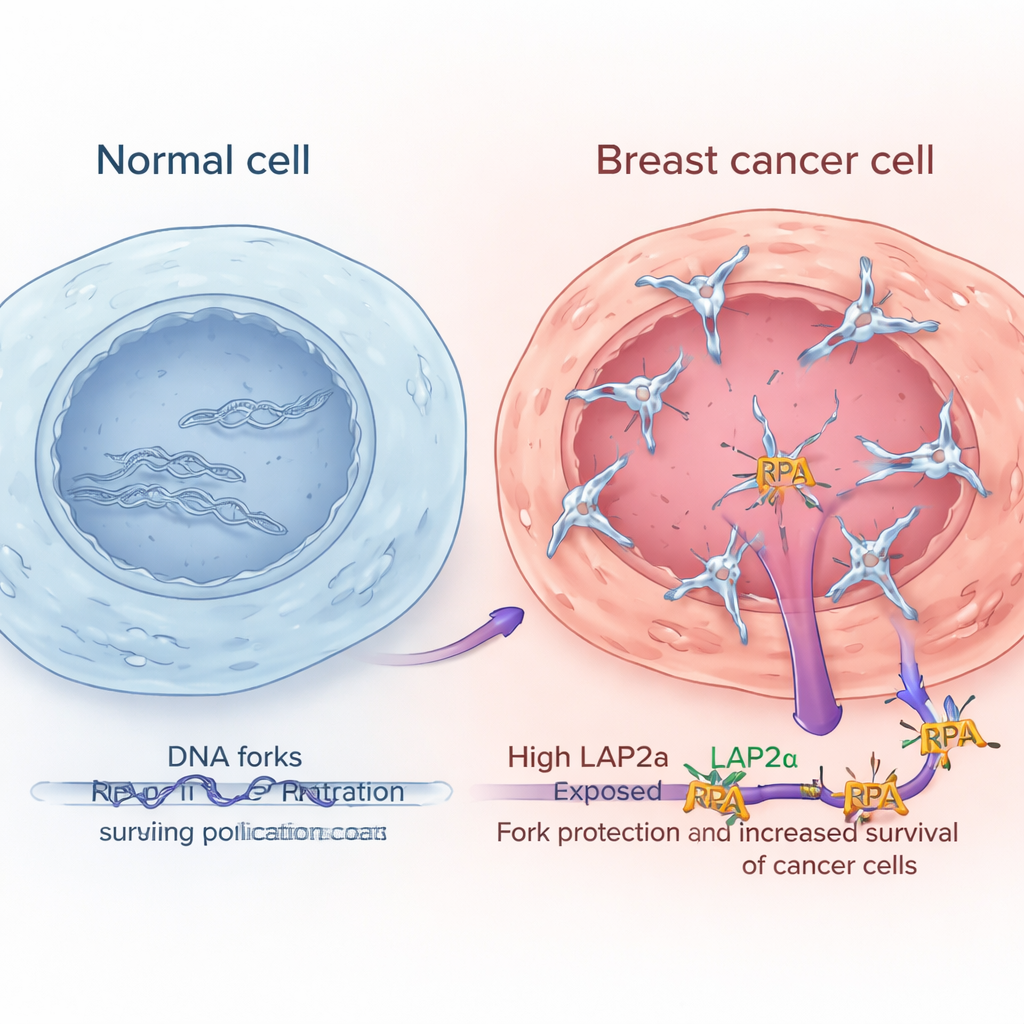
Livelli elevati di LAP2α segnalano tumori mammari più aggressivi
Analizzando ampi dataset pubblici di espressione genica e esaminando campioni tumorali al microscopio, i ricercatori hanno dimostrato che LAP2α è sistematicamente più elevata nei tessuti del cancro al seno rispetto al tessuto mammario normale adiacente. I suoi livelli aumentano con il grado tumorale, cioè i tumori più anomali e aggressivi tendono ad avere più LAP2α. Questo schema è emerso in diversi principali sottotipi di cancro al seno, inclusi i tumori positivi per i recettori ormonali, arricchiti per HER2 e triplo negativi. Importante per i pazienti, coloro i cui tumori presentavano livelli alti di LAP2α avevano tendenzialmente una sopravvivenza peggiore. Al contrario, i componenti centrali di RPA non mostravano cambiamenti simili né legami chiari con l’esito, suggerendo che è la potenziata funzione di LAP2α, più che un semplice aumento di RPA, a aiutare le cellule cancerose a gestire meglio lo stress di replicazione.
Spegnere LAP2α rallenta i tumori ed espone punti deboli
Per andare oltre le correlazioni, il gruppo ha usato modelli murini di cancro al seno in cui LAP2α poteva essere rimossa selettivamente. Una volta formati i tumori mammari, la cancellazione genetica di LAP2α ha causato una crescita tumorale più lenta e ha prolungato la sopravvivenza degli animali. Le cellule tumorali prive di LAP2α si dividevano meno e presentavano più segni di danno al DNA, come evidenziato da una maggiore colorazione per marcatori di rotture del DNA e da un ridotto rivestimento di RPA sul DNA. Quando queste cellule tumorali con deficit di LAP2α sono state trapiantate in nuovi topi, hanno nuovamente formato tumori più piccoli e hanno mostrato una sensibilità aumentata alla chemioterapia che danneggia il DNA, inclusi il farmaco al platino cisplatino e un inibitore di PARP. Esperimenti analoghi in linee cellulari umane di cancro al seno hanno confermato che ridurre LAP2α rende le cellule più vulnerabili a diversi farmaci genotossici, mentre il ripristino di LAP2α normale — ma non di una forma mutante incapace di legare RPA — recuperava sia la protezione del DNA sia la resistenza ai farmaci.
Come LAP2α aiuta a proteggere i filamenti di DNA fragili
Per analizzare il meccanismo, i ricercatori hanno ricreato i passaggi di legame al DNA in saggi in provetta. Hanno miscelato RPA purificata, DNA a filamento singolo e LAP2α normale o una variante incapace di interagire con RPA. Hanno scoperto che LAP2α aumentava direttamente l’efficienza con cui RPA riveste il DNA a filamento singolo e aiutava RPA ad allungare e stabilizzare queste regioni fragili, agendo in modo simile a un fattore di caricamento o a una chaperone. Quando il DNA era presente, RPA tendeva a staccarsi da LAP2α e a legarsi completamente al filamento singolo, mostrando che LAP2α non fa parte del rivestimento protettivo finale ma invece cede RPA al DNA. In assenza di un’interazione funzionale LAP2α–RPA, più forcelle di replicazione collassavano, si accumulavano rotture del DNA e le cellule cancerose erano più propense a morire, specialmente quando ulteriori danni erano indotti dalla chemioterapia.
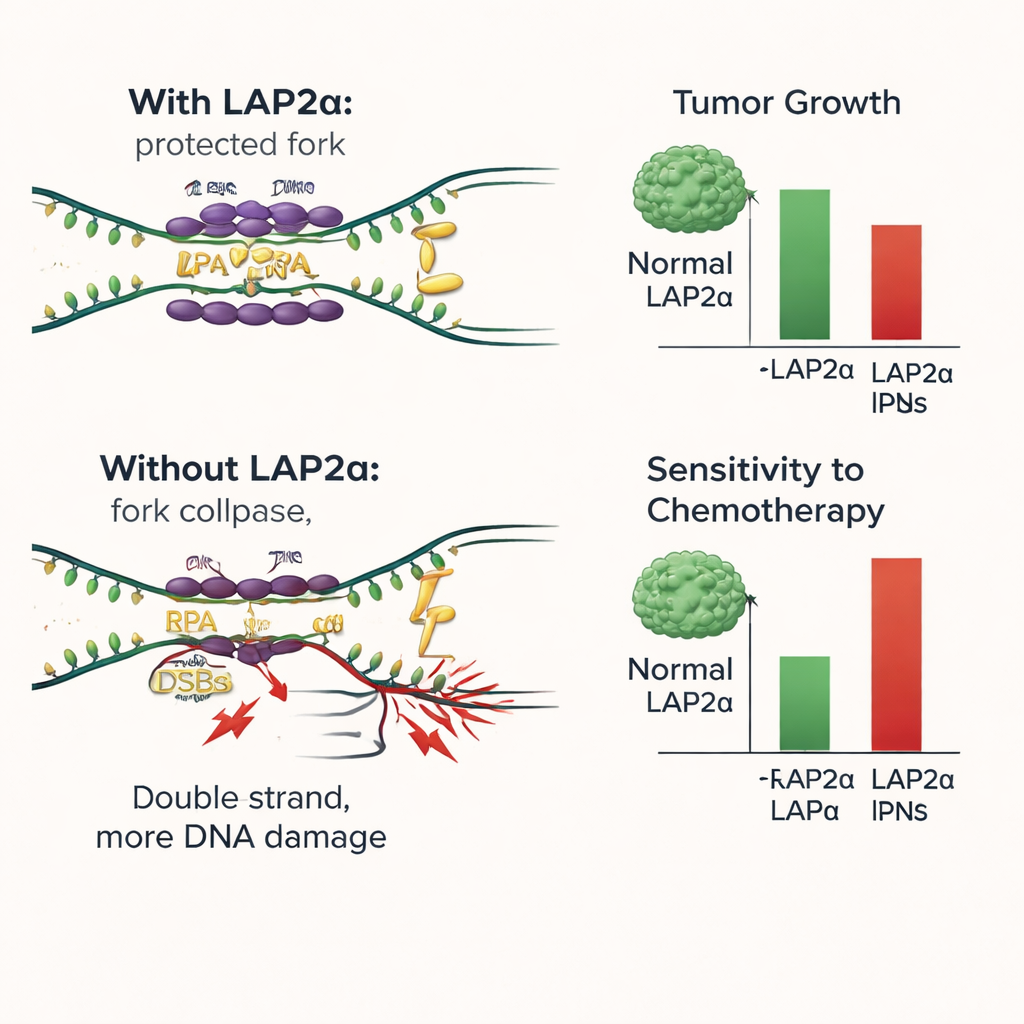
Cosa significa questo per il trattamento futuro del cancro al seno
In termini semplici, questo studio mostra che LAP2α funge da assistente dietro le quinte che aiuta le cellule del cancro al seno a sopportare lo sforzo di copiare il proprio DNA. Caricando efficacemente RPA sul DNA vulnerabile, LAP2α riduce i danni e sostiene la crescita tumorale continua. Rimuovere o disabilitare LAP2α altera l’equilibrio: il danno al DNA si accumula, le cellule smettono di dividersi e i farmaci convenzionali che attaccano il DNA diventano più efficaci. Questi risultati suggeriscono che LAP2α potrebbe essere utilizzata come marcatore di prognosi sfavorevole e come nuovo bersaglio terapeutico. Farmaci che bloccano LAP2α o il suo legame con RPA potrebbero rendere i trattamenti esistenti, come gli agenti al platino e gli inibitori di PARP, più efficaci, specialmente nei tumori che dipendono fortemente da questo sistema di attenuazione dello stress.
Citazione: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Parole chiave: cancro al seno, stress di replicazione del DNA, LAP2 alpha, proteina RPA, sensibilità alla chemioterapia