Clear Sky Science · it
Mirare alla biosintesi dei glicerofosfolipidi per superare la chemioresistenza dovuta alla perdita di SLFN11 nel sarcoma di Ewing
Perché questa ricerca è importante per i tumori infantili
Il sarcoma di Ewing è un cancro raro ma aggressivo che colpisce principalmente bambini e adolescenti. Molti pazienti rispondono inizialmente bene alla chemioterapia, ma per chi sviluppa recidiva i trattamenti attuali spesso non bastano. Questo studio pone una domanda urgente: quando le cellule del sarcoma di Ewing diventano resistenti alla chemioterapia, quali cambiamenti interni permettono loro di sopravvivere — e quei cambiamenti possono diventare nuove vulnerabilità sfruttabili clinicamente?
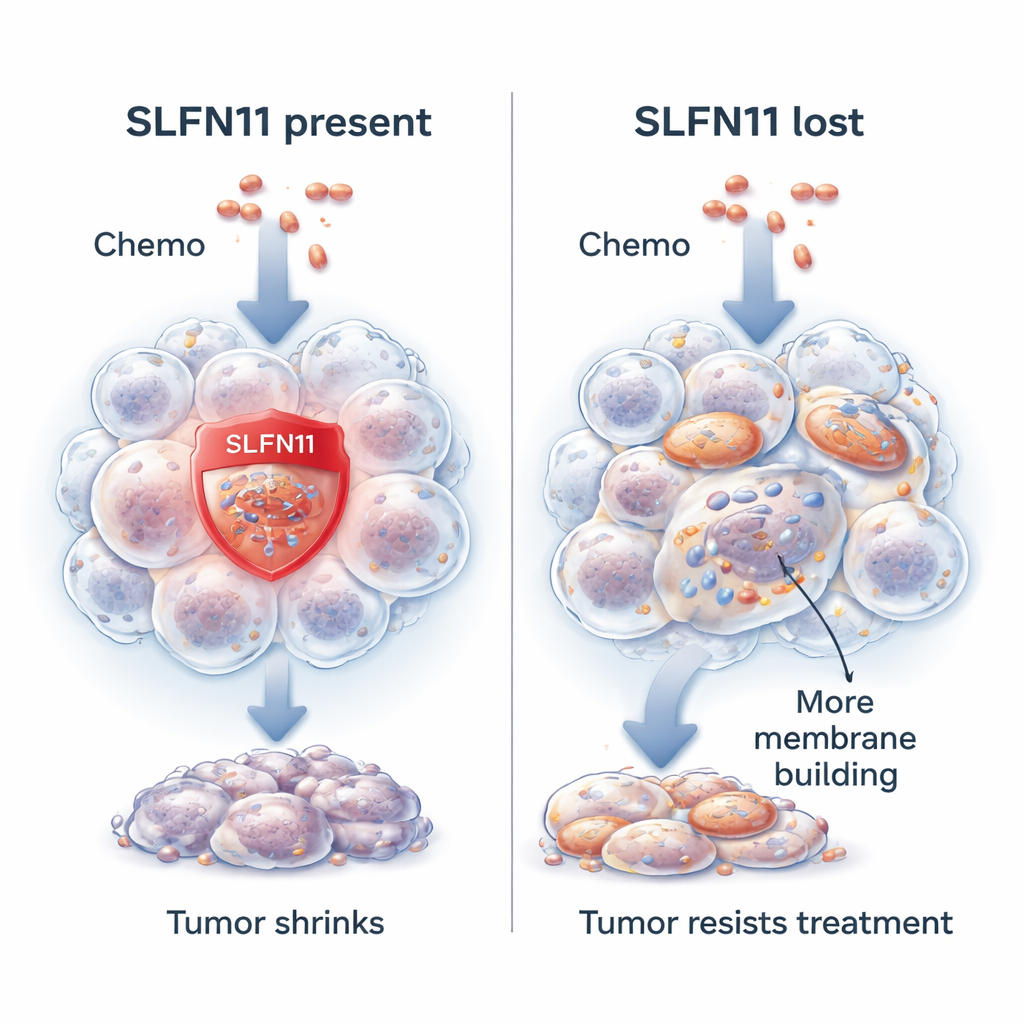
Un gene che rende le cellule cancerose più facili da uccidere
I ricercatori si concentrano su un gene chiamato SLFN11. In molti tumori del sarcoma di Ewing SLFN11 è altamente attivo e rende le cellule tumorali molto più sensibili ai farmaci che danneggiano il DNA, il progetto genetico della cellula. Quando questi farmaci sono somministrati, SLFN11 contribuisce a bloccare la riparazione del DNA e spinge la cellula tumorale verso la morte. I pazienti i cui tumori presentano livelli più elevati di SLFN11 tendono ad avere una sopravvivenza maggiore e rispondono meglio al trattamento. Tuttavia, circa un tumore su dieci presenta inizialmente poco o nessun SLFN11 o lo perde durante la terapia. Quando ciò accade, la stessa chemioterapia diventa molto meno efficace, pur mantenendo la capacità delle cellule tumorali di proliferare.
Come le cellule tumorali riorganizzano l’uso di carburante e lipidi
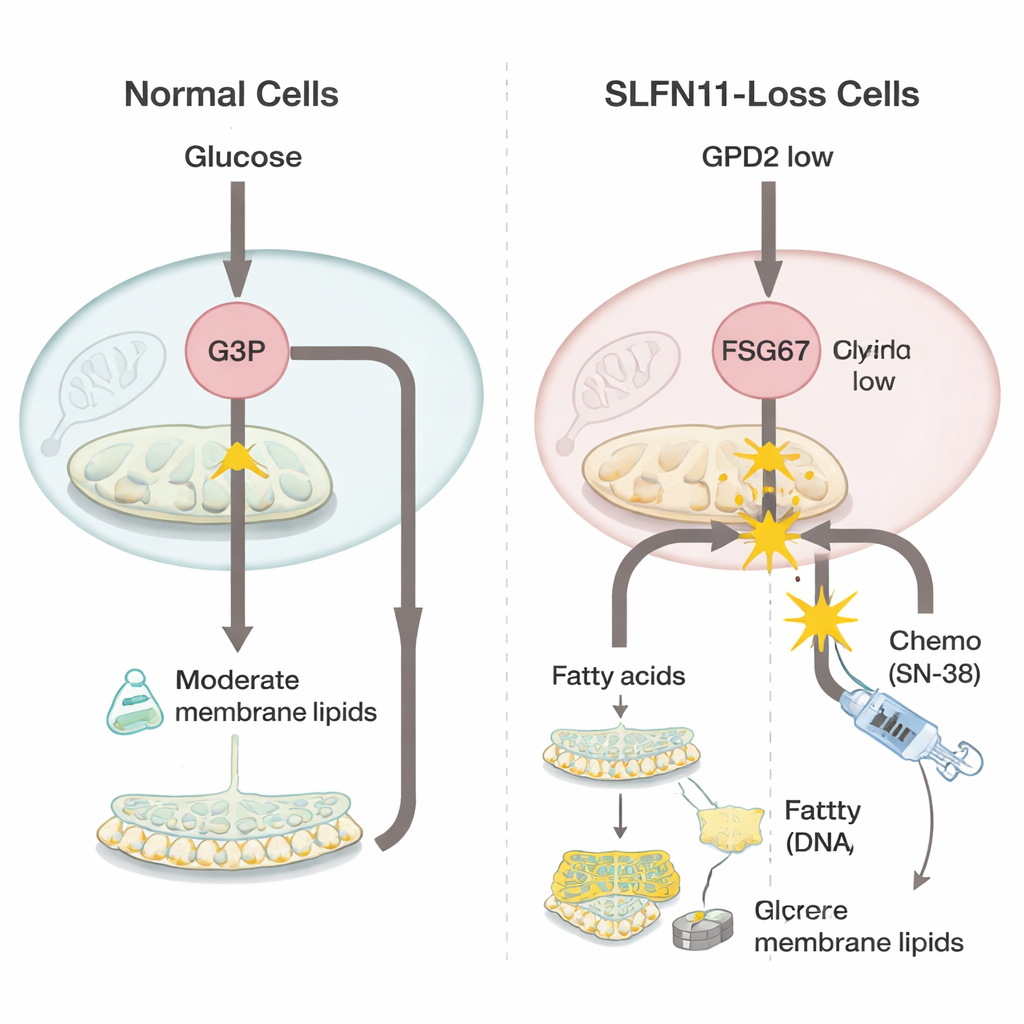
Per capire cosa cambia quando SLFN11 viene perso, il gruppo ha confrontato cellule di sarcoma di Ewing con e senza questo gene usando potenti strumenti “-omici” che misurano migliaia di geni e piccole molecole contemporaneamente. Hanno scoperto che le cellule prive di SLFN11 riducono l’espressione di un enzima mitocondriale chiamato GPD2, che normalmente aiuta a ossidare il glicerolo‑3‑fosfato come parte della produzione di energia. Quando GPD2 è ridotto, il glicerolo‑3‑fosfato si accumula. Piuttosto che andare sprecato, questo precursore in eccesso viene deviato verso la sintesi di più molecole lipidiche che costituiscono le membrane cellulari, un gruppo noto come glicerofosfolipidi. Le cellule mostravano inoltre segnali di una maggiore produzione di grassi insaturi e più flessibili, caratteristica che può aiutare i tumori in rapida crescita ad adattarsi allo stress.
Trasformare un trucco di sopravvivenza in un punto debole
Poiché queste cellule carenti di SLFN11 fanno maggiore affidamento sulla costruzione delle membrane, gli scienziati hanno testato se bloccare questo processo potesse ripristinare la sensibilità alla chemioterapia. Hanno usato un composto chiamato FSG67, che inibisce un passaggio chiave nella produzione di glicerofosfolipidi. Da solo, il farmaco standard che danneggia il DNA SN‑38 era diventato molto meno potente nelle cellule prive di SLFN11, rispecchiando il problema clinico della resistenza. Ma quando SN‑38 è stato combinato con FSG67, le cellule precedentemente resistenti sono risultate molto più vulnerabili e i due farmaci hanno mostrato un effetto combinato maggiore rispetto a quanto atteso dai loro effetti individuali. Al contrario, nelle cellule che mantenevano SLFN11 ed erano già altamente sensibili a SN‑38, l’aggiunta di FSG67 apportava poco vantaggio e poteva persino risultare leggermente controproducente. Questo schema suggerisce che la nuova dipendenza dalla sintesi lipidica e della membrana è specifica dello stato resistente con basso SLFN11.
Un potenziale segnale non invasivo di tumori difficili da trattare
I ricercatori si sono poi chiesti se questo riprogrammamento metabolico potesse essere rilevato in tumori reali, non solo in colture cellulari. Hanno fatto crescere tumori di sarcoma di Ewing in topi, con o senza SLFN11, e hanno usato la risonanza magnetica nucleare (RMN) per analizzare la composizione chimica degli estratti tumorali. I tumori privi di SLFN11 mostravano un rapporto più alto tra due molecole contenenti colina legate al turnover delle membrane: fosfocolina e glicerofosfocolina. Un alto rapporto fosfocolina/glicerofosfocolina è stato associato in altri tumori a comportamenti più aggressivi e a una risposta peggiore al trattamento. Poiché i segnali della colina possono essere misurati con tecniche avanzate di imaging, questo cambiamento potrebbe in futuro servire come marker non invasivo per identificare i tumori di Ewing che hanno adottato questo stato resistente orientato alla costruzione di membrane.
Cosa potrebbe significare per i trattamenti futuri
Complessivamente, lo studio mostra che quando le cellule del sarcoma di Ewing perdono SLFN11 e diventano meno sensibili alla chemioterapia che danneggia il DNA, compensano riorganizzando il metabolismo verso la produzione di più lipidi di membrana. Questo cambiamento non solo aiuta le cellule a sopravvivere; crea anche un nuovo tallone d’Achille. Bloccare la produzione di glicerofosfolipidi con un farmaco come FSG67 può ripristinare parzialmente il potere citotossico della chemioterapia in queste cellule resistenti. Pur non essendo ancora FSG67 un farmaco clinico, il lavoro indica una strategia in cui in futuro i medici potrebbero classificare i tumori dei pazienti in base allo stato di SLFN11 e alle caratteristiche metaboliche, e abbinare le terapie che danneggiano il DNA con inibitori mirati della sintesi lipidica e delle membrane per superare la resistenza.
Citazione: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Parole chiave: Sarcoma di Ewing, chemioresistenza, SLFN11, metabolismo del cancro, biosintesi dei lipidi