Clear Sky Science · it
Mirare l'IGFBP2 esosomiale indotto da ipossia supera l'evasione immunitaria mediata da CD47 nel glioblastoma
Perché affamare i tumori di ossigeno può ritorcersi contro
I medici sanno da tempo che il glioblastoma, un tumore cerebrale letale, cresce spesso in aree povere di ossigeno. Queste sacche ipossiche rendono il tumore più difficile da trattare. Questo studio mostra come la bassa disponibilità di ossigeno aiuti le cellule tumorali a nascondersi dal sistema immunitario e suggerisce una nuova terapia combinata che potrebbe renderle più vulnerabili all'attacco del corpo.
Un tumore cerebrale letale che sfugge alle nostre difese
Il glioblastoma è il tumore cerebrale primario più aggressivo negli adulti, con una sopravvivenza tipicamente misurata in mesi. Anche se cellule immunitarie infiltrano questi tumori, le cellule cancerose spesso sfuggono alla distruzione. Una via chiave di fuga è una proteina di superficie chiamata CD47, talvolta definita segnale "non mangiarmi", che indica alle cellule immunitarie vicine, come i macrofagi, di non fagocitare la cellula tumorale. Farmaci che bloccano CD47 sono già in sperimentazione, ma i risultati nei tumori solidi come il glioblastoma sono stati variabili, suggerendo che altri fattori nell'ambiente tumorale possano compromettere queste terapie.
Zone ipossiche e minuscoli pacchetti tumorali
Utilizzando il sequenziamento dell'RNA a singola cellula, i ricercatori hanno mappato migliaia di cellule da diverse regioni di campioni di glioblastoma, confrontando il nucleo a basso ossigeno del tumore con il suo margine esterno. Hanno identificato un sottotipo particolarmente aggressivo di cellule nel nucleo ipossico, chiamato cellule GBM di tipo mesenchimale, che esprimeva fortemente CD47 e una proteina chiamata IGFBP2. Allo stesso tempo, hanno scoperto che queste cellule del nucleo rilasciavano un gran numero di vescicole nanometriche note come esosomi, che portavano IGFBP2 sulla loro superficie. Poiché gli esosomi possono viaggiare attraverso il cervello e persino entrare nel flusso sanguigno, possono diffondere segnali ben oltre il luogo di origine. 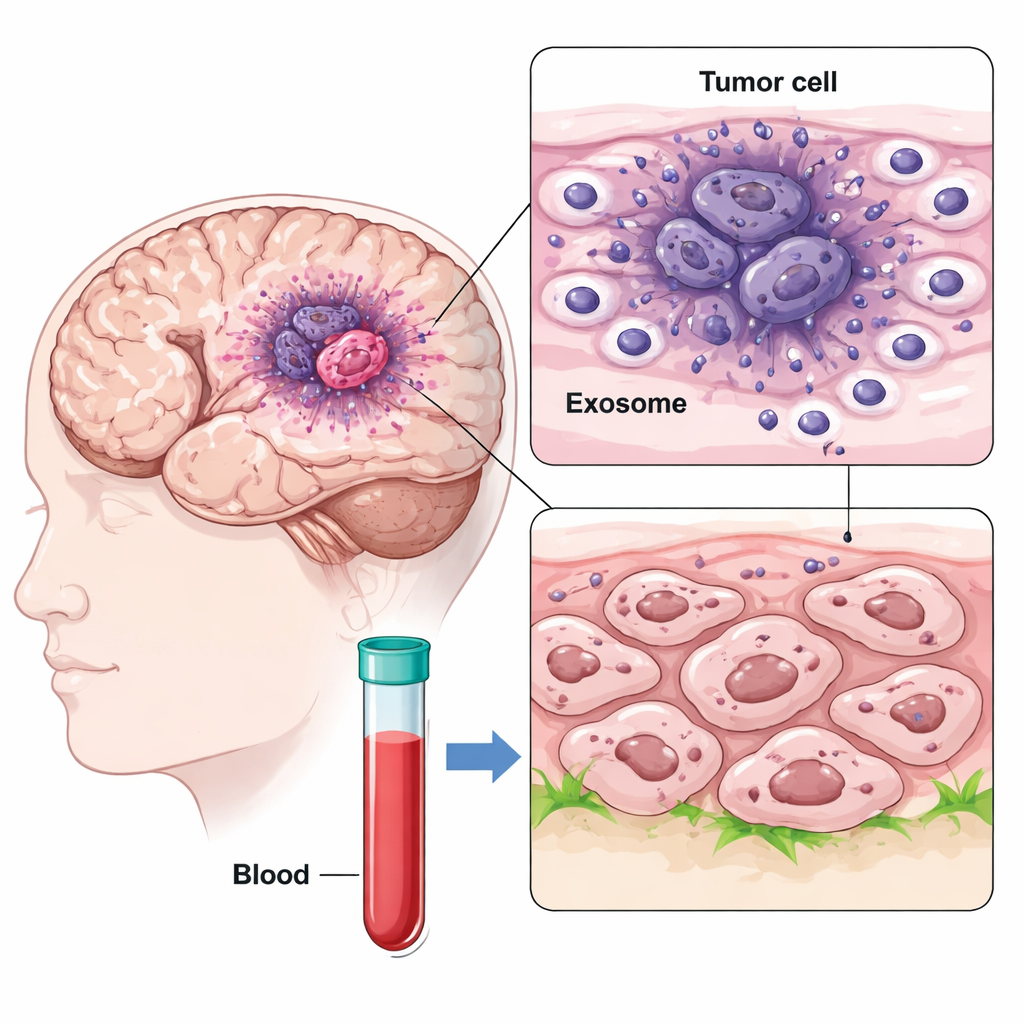
Come una proteina partner rafforza il segnale “non mangiarmi”
Il gruppo ha quindi approfondito il ruolo di IGFBP2. Hanno dimostrato che in condizioni di bassa ossigenazione, una proteina sensore di ipossia chiamata HIF-2α attiva il gene IGFBP2 nelle cellule tumorali. IGFBP2 si lega poi a recettori specifici chiamati integrine sulla superficie degli esosomi, decorandone la membrana esterna. Quando questi esosomi ricoperti di IGFBP2 si fondono con altre cellule tumorali, attivano una catena di segnali intracellulari che coinvolge proteine note come FAK e STAT3. Questa cascata aumenta infine la quantità di CD47 sulla superficie della cellula tumorale, rafforzando il messaggio "non mangiarmi" ai macrofagi e proteggendo ulteriormente le cellule cancerose dall'attacco immunitario. 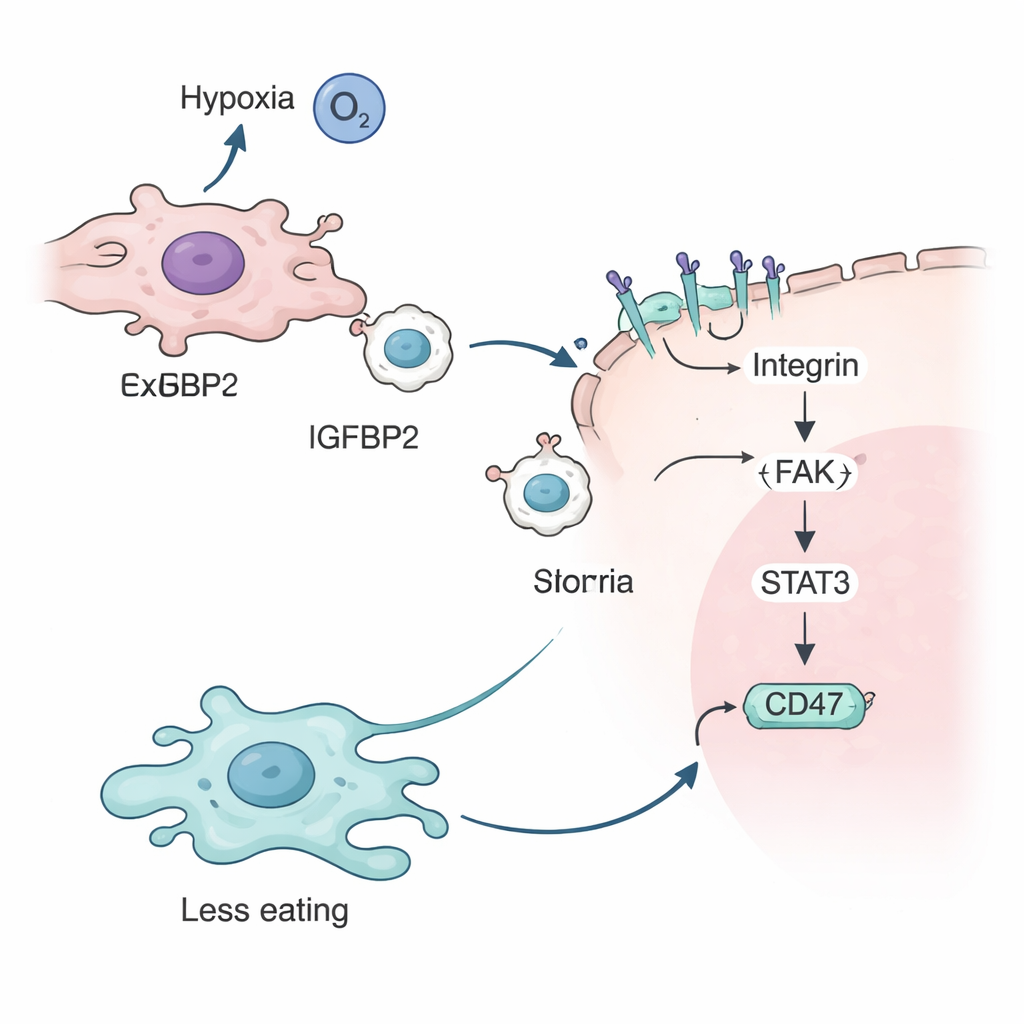
Prove da campioni di pazienti e modelli animali
Per collegare questi risultati di laboratorio alla malattia umana, i ricercatori hanno esaminato tessuto tumorale e sangue di persone con glioma. Hanno riscontrato livelli più elevati di IGFBP2 sia nei tumori sia negli esosomi circolanti nei pazienti con malattia più avanzata, suggerendo che gli esosomi positivi per IGFBP2 potrebbero servire come marker nel sangue del grado tumorale. In modelli murini, ridurre IGFBP2 nelle cellule di glioblastoma le rendeva più vulnerabili alla fagocitosi da parte dei macrofagi, rallentava la crescita tumorale e prolungava la sopravvivenza. Al contrario, l'aggiunta di esosomi ricchi di IGFBP2 aumentava i livelli di CD47, riduceva la fagocitosi e accelerava la progressione tumorale.
Un promettente uno-due terapeutico
Infine, il team ha testato se bloccare IGFBP2 potesse rendere la terapia mirata a CD47 più efficace. Nei topi con tumori cerebrali, il trattamento con anticorpi contro IGFBP2 e CD47 ha indotto una maggiore attività dei macrofagi, tumori più piccoli e una sopravvivenza più lunga rispetto a ciascun trattamento singolarmente. Tagliando il segnale IGFBP2 guidato dall'ipossia e bloccando direttamente il segnale "non mangiarmi" di CD47, questa terapia combinata ha attaccato il camuffamento immunitario del tumore da due direzioni. Per i pazienti, questi risultati suggeriscono che misurare IGFBP2 negli esosomi circolanti potrebbe aiutare a identificare coloro più propensi a beneficiare dell'immunoterapia basata su CD47, e che associare inibitori di IGFBP2 e CD47 potrebbe rappresentare una strategia più efficace contro il glioblastoma rispetto a ciascun farmaco da solo.
Citazione: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Parole chiave: glioblastoma, esosomi, evasione immunitaria, CD47, ipossia