Clear Sky Science · it
Il lungo RNA non codificante AC093895.1 promuove la formazione e la metastasi del tumore ovarico attraverso una rete a feedback positivo dipendente dal fattore di trascrizione SOX4
Perché questa ricerca è importante
Il cancro ovarico è spesso definito un “killer silenzioso” perché tende a essere diagnosticato in fase avanzata, quando si è già diffuso ed è più difficile da curare. Molte donne vanno incontro a recidive anche dopo chirurgia e chemioterapia, e gli attuali esami del sangue non sono sempre affidabili nel prevedere chi avrà una prognosi peggiore. Questo studio scopre un nuovo “circuito di controllo” molecolare all’interno delle cellule del cancro ovarico che favorisce la crescita e la diffusione dei tumori, e suggerisce un nuovo bersaglio che in futuro potrebbe migliorare sia la diagnosi sia il trattamento.
Un RNA nascosto con un grande impatto
Il nostro DNA contiene istruzioni non solo per produrre proteine, ma anche per numerose molecole di RNA che non diventano mai proteine. Questi cosiddetti RNA lunghi non codificanti funzionano più come direttori d’orchestra che come strumenti, coordinando il comportamento di altri geni. I ricercatori si sono concentrati su una di queste molecole, chiamata AC093895.1, e hanno rilevato che è molto più abbondante nei tessuti di carcinoma ovarico rispetto ai campioni di ovaio sano. Utilizzando grandi dataset pubblici e campioni tumorali di pazienti, hanno dimostrato che livelli elevati di AC093895.1 sono particolarmente comuni nei tumori metastatici e sono associati a una sopravvivenza peggiore, suggerendo che questo RNA è correlato a una malattia aggressiva.
Aumentare la crescita e ridurre l’autodistruzione
Per capire cosa fa effettivamente AC093895.1, il gruppo ha usato linee cellulari di carcinoma ovarico coltivate in laboratorio e ha ridotto la quantità di questo RNA con strumenti genetici. Quando AC093895.1 veniva silenziato, le cellule tumorali crescevano più lentamente, restavano bloccate prima di entrare nella fase attiva del ciclo cellulare e avevano una maggiore probabilità di andare incontro a morte cellulare programmata. Anche la loro capacità di migrare e invadere barriere—passaggi chiave nella formazione delle metastasi—è diminuita drasticamente. A livello molecolare, i marcatori associati alla morte cellulare sono aumentati, mentre le proteine che promuovono la divisione cellulare e il movimento sono diminuite. Nei modelli murini, i tumori derivati da cellule deprivate di AC093895.1 erano più piccoli, avevano meno cellule in divisione, più cellule morenti e producevano meno metastasi polmonari.
Una “spugna” di RNA che libera un gene promotore di cancro
Approfondendo, gli scienziati hanno scoperto che AC093895.1 si trova principalmente nel citoplasma delle cellule tumorali, dove può interagire con piccoli RNA regolatori detti microRNA. Hanno identificato uno di questi partner, miR‑1253, che normalmente agisce come soppressore tumorale in diversi tipi di cancro. AC093895.1 e miR‑1253 si legano reciprocamente e si influenzano a vicenda: quando AC093895.1 è alto, miR‑1253 è basso, e viceversa. Agendo come una “spugna” molecolare, AC093895.1 assorbe miR‑1253 e ne impedisce l’azione sui suoi bersagli. Uno di questi bersagli è SOX4, un fattore di trascrizione noto per promuovere la sopravvivenza, l’invasività e la diffusione delle cellule tumorali. Quando miR‑1253 è bloccato, i livelli di SOX4 aumentano; quando AC093895.1 è ridotto, i livelli di SOX4 diminuiscono. Funzionalmente, bloccare miR‑1253 può annullare molti degli effetti benefici del silenziamento di AC093895.1, confermando che questa via è centrale nel modo in cui l’RNA guida la malignità.
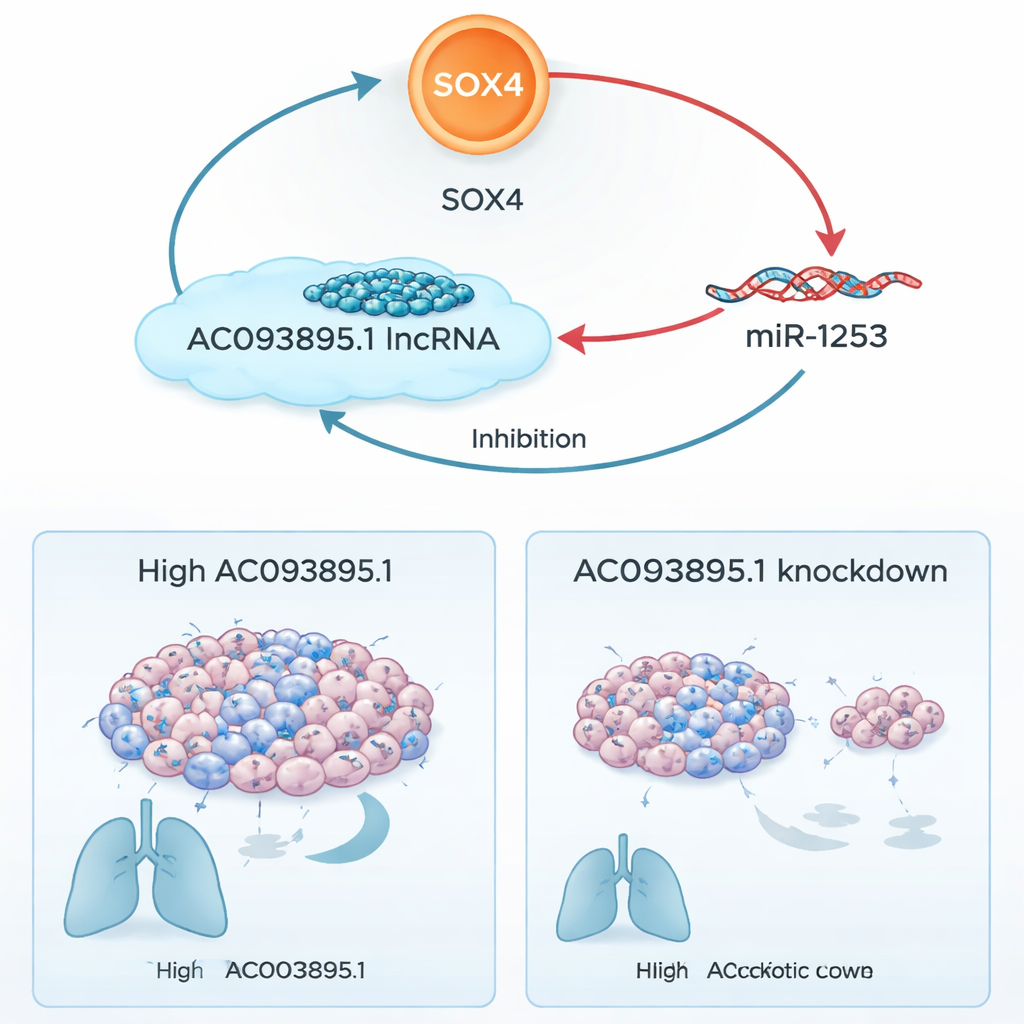
Un circuito canceroso auto‑rinforzante
È sorprendente che la relazione non finisca qui. Lo stesso SOX4 può attivare il gene che produce AC093895.1. Gli autori hanno mostrato che SOX4 si lega fisicamente alla regione promotrice—l’interruttore «on» del DNA—di AC093895.1 e ne aumenta l’attività. Questo crea un circuito chiuso: SOX4 aumenta AC093895.1, AC093895.1 sopprime miR‑1253, e la perdita di miR‑1253 permette l’accumulo di ulteriore SOX4. Nei campioni tumorali di 14 pazienti, le aree con ALTI livelli di AC093895.1 avevano quasi sempre ALTI livelli di SOX4 e bassi livelli di miR‑1253, e questi schemi erano associati a stadi più avanzati e a una maggiore diffusione a linfonodi e organi. Interrompere il circuito abbassando AC093895.1 indeboliva la crescita tumorale e le metastasi guidate da SOX4 sia in colture cellulari sia nei topi.
Cosa potrebbe significare per le pazienti
Per un non specialista, il circuito SOX4/AC093895.1/miR‑1253/SOX4 può essere visto come un pedale dell’acceleratore bloccato nelle cellule del cancro ovarico: una volta premuto, continua a dire alle cellule di crescere, sopravvivere e migrare verso nuovi organi. Questo studio mostra che AC093895.1 è una componente chiave di quel meccanismo e che ridurla può rallentare i tumori e ridurre la diffusione nei modelli sperimentali. Sebbene terapie e test basati su questo RNA non siano ancora disponibili, AC093895.1—e il circuito che controlla—potrebbero costituire la base per futuri strumenti prognostici su sangue o tessuto e per trattamenti mirati volti a prevenire recidive e metastasi nelle donne con carcinoma ovarico.
Citazione: Huang, B., An, H., Qiu, Y. et al. The long noncoding RNA AC093895.1 promotes ovarian cancer formation and metastasis through a positive feedback network dependent on the transcription factor SOX4. Cell Death Dis 17, 202 (2026). https://doi.org/10.1038/s41419-026-08429-2
Parole chiave: cancro ovarico, RNA lungo non codificante, metastasi, SOX4, marcatore