Clear Sky Science · it
HSPA5 promuove la stabilità di YAP/TAZ indipendentemente dalla via Hippo e induce la transizione proneurale‑to‑mesenchimale nel glioblastoma
Perché questo studio sul cancro cerebrale è importante
Il glioblastoma è uno dei tumori cerebrali più letali, in parte perché molti tumori nel tempo si trasformano in uno stato più resistente e difficile da trattare. Questo studio svela come una proteina di risposta allo stress comune, HSPA5, contribuisca a guidare quella trasformazione e mantenga molecole pro‑tumorali vive più a lungo del dovuto. Comprendere questo “trucco di sopravvivenza” suggerisce nuovi modi per rendere il glioblastoma meno aggressivo e più sensibile alle terapie esistenti.
Un tumore che cambia personalità
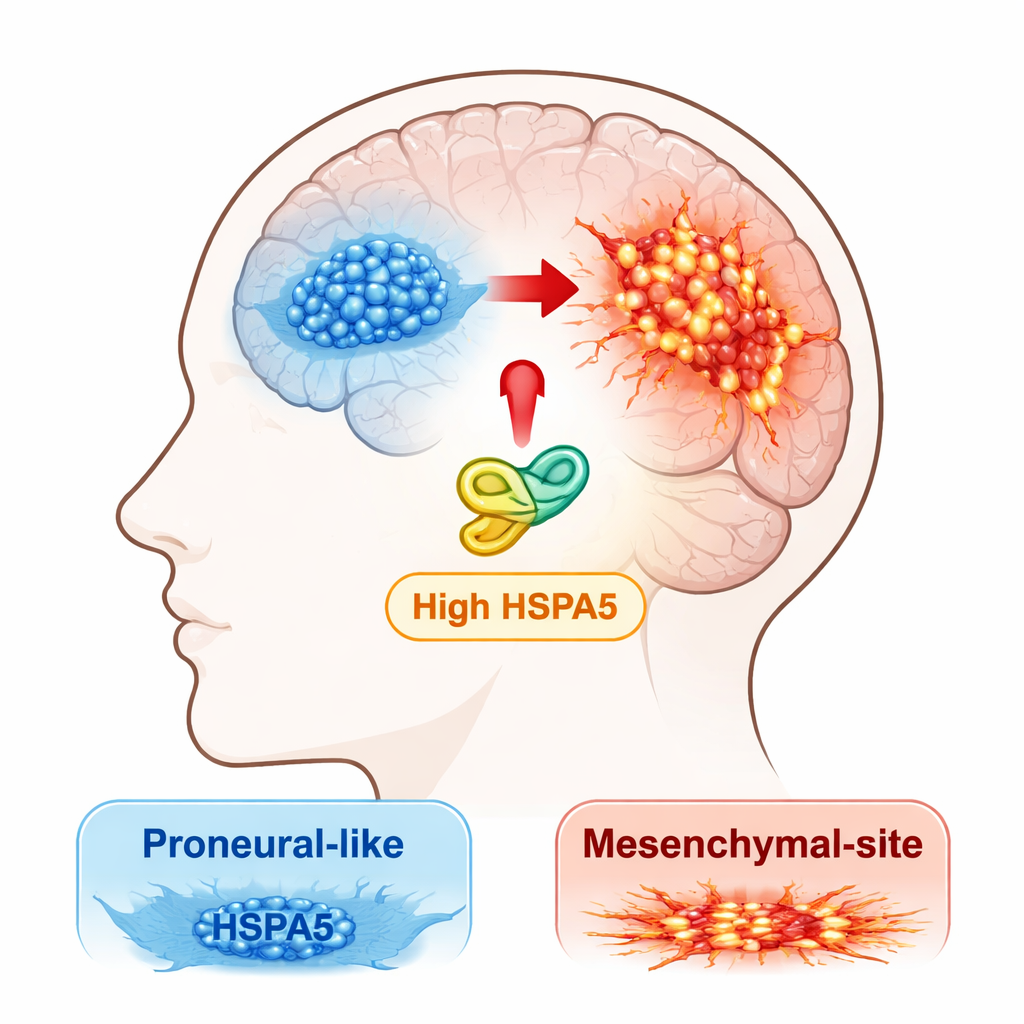
Medici e ricercatori riconoscono oggi che il glioblastoma non è una singola malattia, ma un insieme di sottotipi molecolari. Due forme principali sono quella “proneurale”, che tende a essere relativamente meno aggressiva, e quella “mesenchimale”, che è più invasiva, resistente alle terapie e associata a recidive più precoci. I tumori possono evolvere dallo stato proneurale a quello mesenchimale, un processo che gli autori chiamano transizione proneurale‑to‑mesenchimale, o PMT. Il gruppo ha cercato di identificare quali proteine di risposta allo stress potrebbero spingere i tumori lungo questo pericoloso percorso.
Una proteina helper dello stress sotto i riflettori
I ricercatori hanno iniziato scandagliando grandi banche dati pubbliche sul cancro e i propri campioni di pazienti alla ricerca di membri della famiglia HSP70, un gruppo di proteine “chaperone” che aiutano altre proteine a ripiegarsi e a sopravvivere sotto stress. Una chaperone, HSPA5, è emersa in modo evidente. La sua attività risultava più alta nel sottotipo mesenchimale del glioblastoma e significativamente maggiore nei tumori rispetto al tessuto cerebrale normale. I pazienti i cui tumori esprimevano livelli più elevati di HSPA5 tendevano ad avere una sopravvivenza complessiva peggiore, indicando che potrebbe essere un fattore attivo nell’aggressività della malattia piuttosto che un semplice spettatore.
Costringere le cellule a diventare più aggressive
Per capire cosa faccia HSPA5 nelle cellule tumorali, il team ha coltivato cellule primarie di glioblastoma prelevate direttamente dai pazienti e le ha divise in gruppi con caratteristiche proneurali o mesenchimali. Quando hanno forzato le cellule proneurali a produrre più HSPA5, queste hanno cominciato a comportarsi in modo più simile alle cellule mesenchimali: si dividevano più rapidamente, migravano e invadevano con maggiore facilità e attivavano marcatori mesenchimali tipici come CD44 e c‑MET, mentre riducevano marcatori proneurali come SOX2 e OLIG2. Il contrario era anche vero: ridurre i livelli di HSPA5 nelle cellule mesenchimali attenuava la loro crescita e invasività e le spingeva parzialmente verso un profilo meno aggressivo.
Proteggere gli interruttori chiave della crescita dalla “spazzatura” cellulare
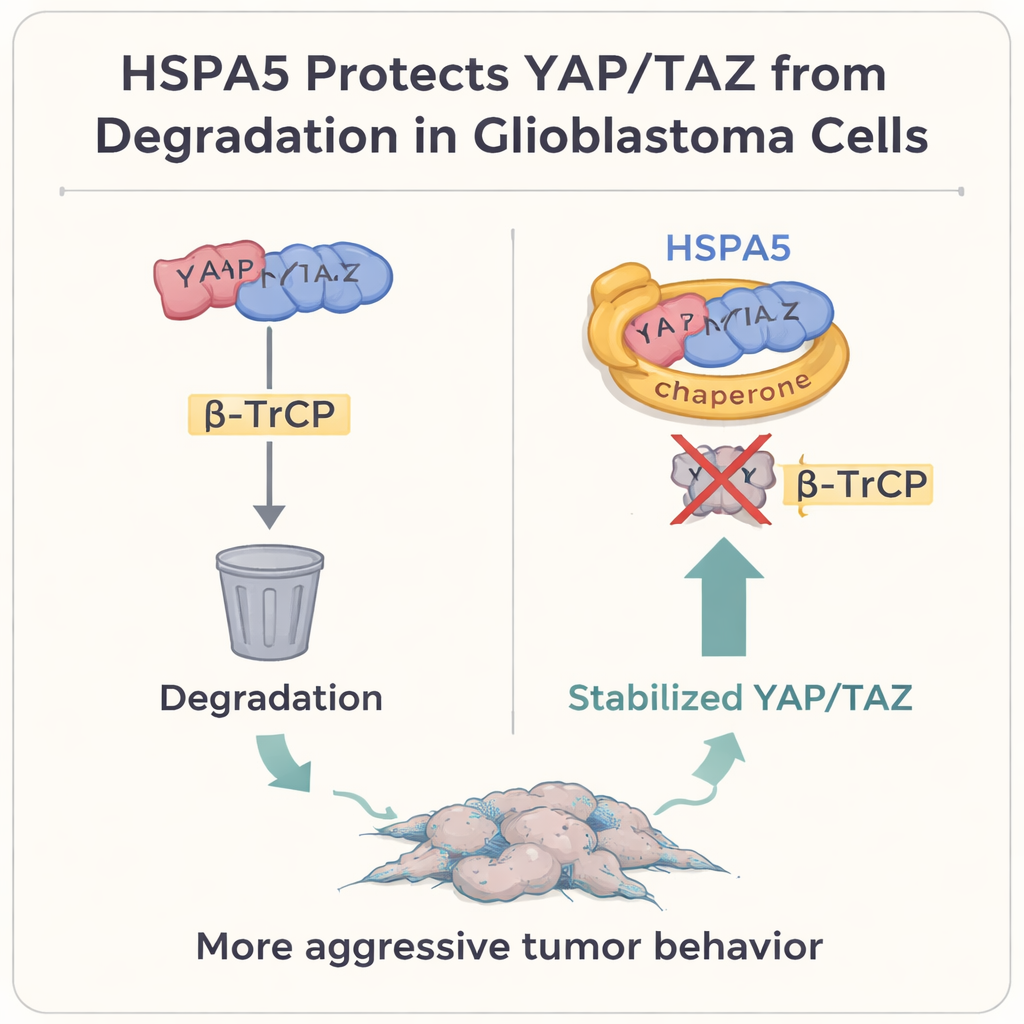
Approfondendo, gli autori si sono concentrati su due potenti regolatori della crescita, YAP e TAZ, che sono al centro della via di segnalazione Hippo. In molti tumori solidi, incluso il glioblastoma, queste proteine agiscono come interruttori principali che promuovono crescita cellulare, plasticità e lo stato mesenchimale. Normalmente, quando la cellula vuole frenare questo programma, marca YAP e TAZ per la distruzione tramite una proteina chiamata β‑TrCP, che li accompagna al “cassonetto” della cellula, il proteasoma. Lo studio mostra che HSPA5 si lega fisicamente a YAP e TAZ, usando il suo dominio di legame al substrato come un guanto protettivo. Così facendo impedisce a β‑TrCP di attaccarsi, evita che YAP/TAZ vengano ubiquitinati e degradati, e permette loro di accumularsi nel nucleo dove attivano i geni mesenchimali, inclusi CD44 e c‑MET.
Dai piatti e dai topi ai tumori dei pazienti
Il gruppo ha confermato questo meccanismo in vari modi. Bloccare HSPA5 accelerava la scomparsa delle proteine YAP e TAZ, a meno che il proteasoma non fosse chimicamente inibito, e aumentava i segnali di “tag” per la spazzatura su di esse. Riattivare YAP e TAZ compensava la perdita di crescita e invasione osservata quando HSPA5 veniva ridotto, mentre silenziare YAP/TAZ annullava gli effetti pro‑tumorali dell’espressione elevata di HSPA5. In modelli murini in cui cellule umane di glioblastoma venivano impiantate nel cervello, i tumori con alto HSPA5 crescevano di più e causavano la morte degli animali più rapidamente; abbassare HSPA5, o interrompere il suo sostegno a YAP/TAZ, rallentava la crescita ed estendeva la sopravvivenza. Infine, in campioni umani corrispondenti presi dagli stessi pazienti prima e dopo la recidiva, i tumori recidivati e più mesenchimali mostravano livelli più alti di HSPA5, YAP, TAZ e marcatori mesenchimali rispetto ai tumori originari di tipo proneurale.
Cosa significa per i futuri trattamenti del cancro cerebrale
In termini pratici, questo lavoro suggerisce che le cellule di glioblastoma sfruttano un aiuto della risposta allo stress, HSPA5, per proteggere importanti interruttori di crescita (YAP e TAZ) dalla degradazione. Questa protezione aiuta i tumori a spostarsi verso e mantenere un’identità più aggressiva e resistente alle terapie. Poiché esistono già inibitori a piccole molecole di HSPA5 e le cellule tumorali possono dipendere da questa chaperone più delle cellule normali, l’asse HSPA5–YAP/TAZ rappresenta un nuovo bersaglio interessante. Terapie che indeboliscono questo scudo protettivo potrebbero rendere le cellule di glioblastoma meno adattabili, meno invasive e più vulnerabili a trattamenti standard come chemioterapia e radioterapia.
Citazione: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Parole chiave: glioblastoma, HSPA5, YAP/TAZ, plasticità tumorale, transizione mesenchimale