Clear Sky Science · it
Arresto del ciclo cellulare G0/G1 mediato da p16 porta a SASP e fibrosi nella distrofia endoteliale corneale di Fuchs
Perché questa malattia oculare è importante
Con l’avanzare dell’età, una delle minacce meno note alla vista è una condizione chiamata distrofia endoteliale corneale di Fuchs (FECD), che offusca lentamente la normale finestra anteriore trasparente dell’occhio. Questo articolo indaga perché alcune cellule sulla superficie interna della cornea si usurano e cicatrizzano nel tempo, e perché le donne sono colpite più frequentemente. Comprendere questi cambiamenti nascosti potrebbe aprire la strada a farmaci che ritardano o addirittura evitano la necessità di trapianti di cornea.
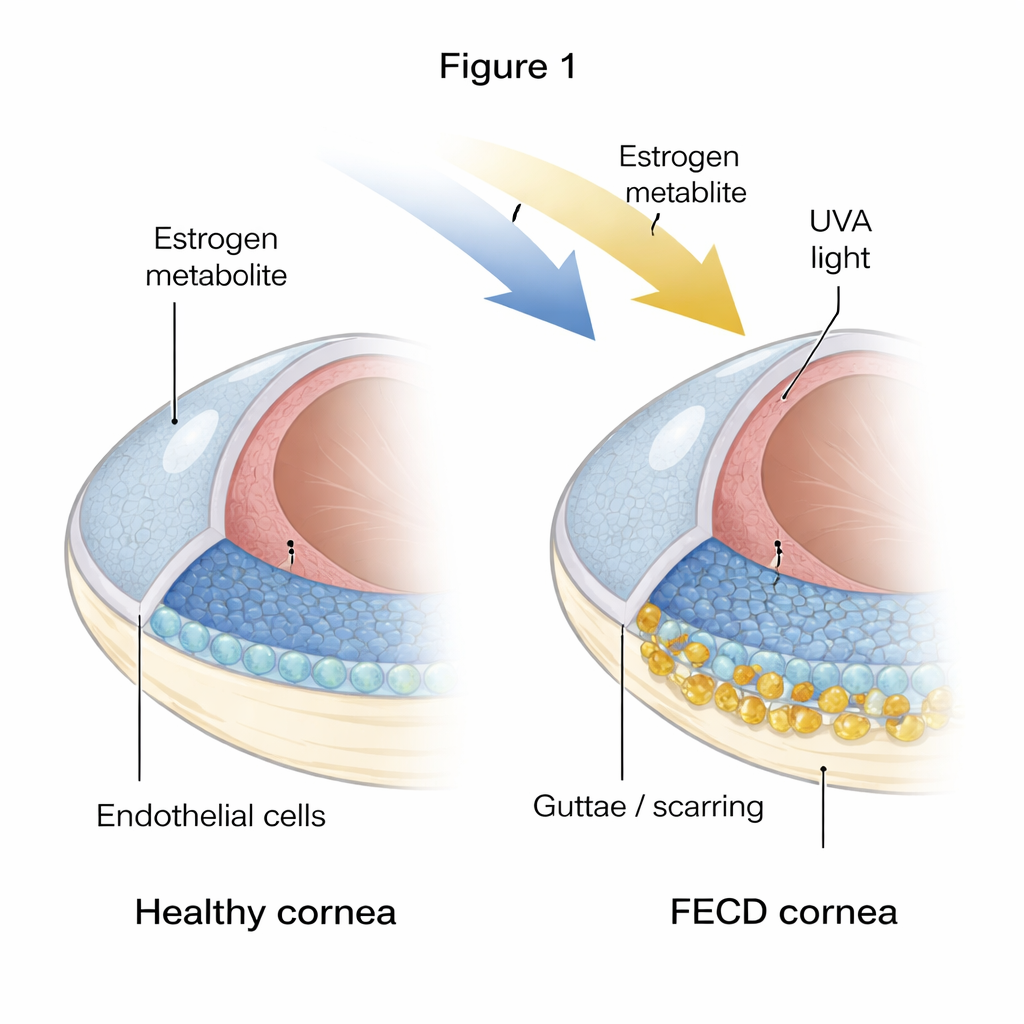
Il fragile rivestimento interno della cornea
La cornea deve rimanere perfettamente disidratata per restare trasparente, compito svolto da un singolo strato di cellule esagonali chiamate cellule endoteliali corneali. Nella FECD molte di queste cellule muoiono e lo strato diventa irregolare e a chiazze. Allo stesso tempo si accumulano sulla superficie interna rigonfiamenti e materiale ispessito, noti come guttae e matrice extracellulare in eccesso. Gli autori hanno confrontato cornee di donatori sani con cornee di pazienti FECD e hanno riscontrato forti segnali che i tessuti malati sono sia “invecchiati” sia fibrotici: le cellule mostrano marcatori di senescenza (uno stato di arresto permanente) e di fibrosi (cellule che si comportano più come cellule che formano cicatrici e depositano tessuto in eccesso).
Stress cronico da luce e ormoni spinge le cellule in un vicolo cieco
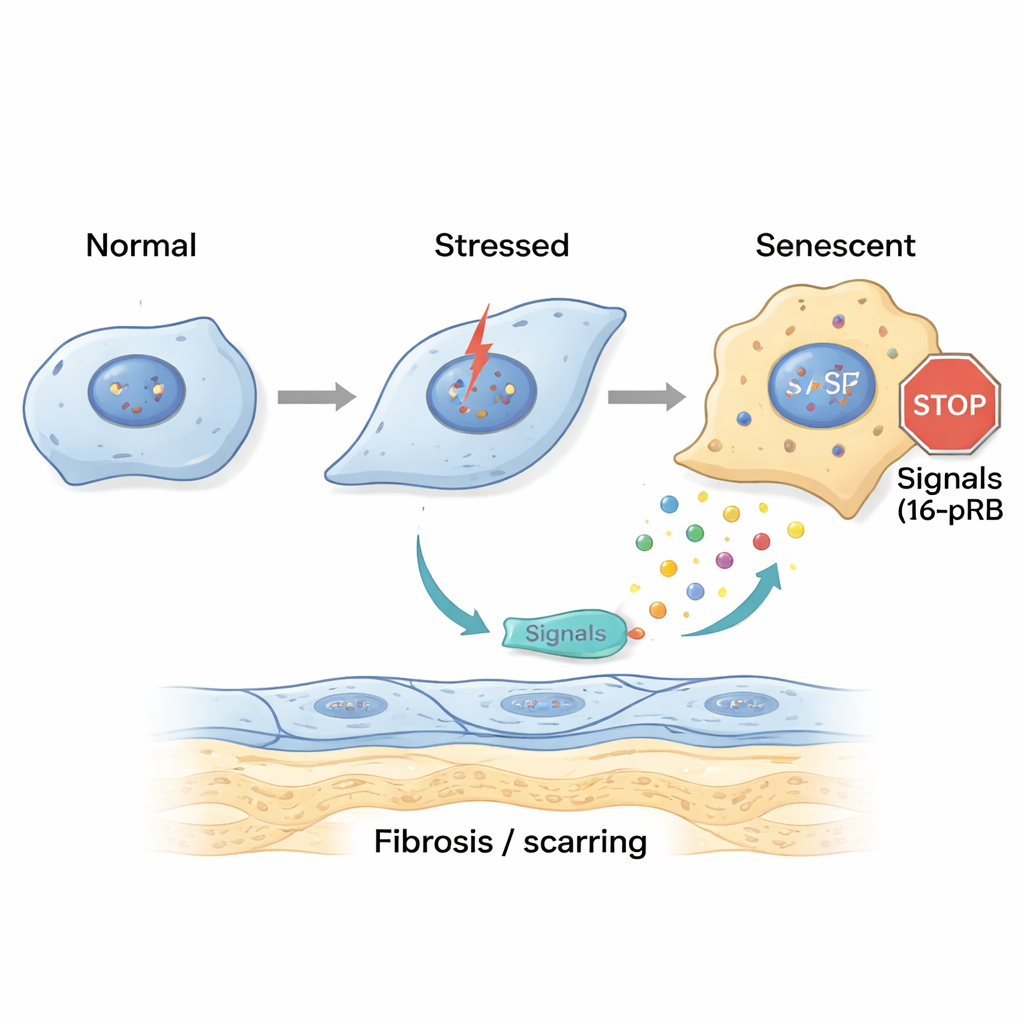
Per sondare come inizi questo danno, i ricercatori hanno ricreato in laboratorio uno stress simile alla FECD. Hanno esposto cellule endoteliali corneali sane a luce ultravioletta A (UVA) e a 4-idrossiestradiolo, un prodotto ossidato dell’estradiolo legato al danno del DNA. Un singolo colpo breve di stress ha fatto sì che le cellule arrestassero temporaneamente in una fase avanzata del ciclo cellulare e iniziassero una transizione precoce verso uno stato più simile a quello dei fibroblasti, ma rimaneva una certa capacità di recupero. Al contrario, esposizioni ripetute e croniche hanno spinto le cellule in uno stato diverso: si accumulavano in una fase precoce del ciclo cellulare chiamata G0/G1 e attivavano un gene chiamato p16, che blocca il ciclo cellulare tramite la proteina partner pRB. Queste cellule sono diventate grandi, piatte e inequivocabilmente senescenti, esprimendo inoltre in modo marcato marcatori di fibrosi e proteine che costituiscono le guttae ispessite nella FECD.
Le cellule senescenti inviano segnali dannosi e diffondono la cicatrizzazione
Le cellule senescenti non stanno semplicemente ferme; secernono un mix di molecole segnalatrici noto come fenotipo secretorio associato alla senescenza (SASP). Il team ha raccolto il fluido da cellule corneali stressate e lo ha applicato a cellule fresche e a cornee di donatori sani. Lo SASP “acuto” ha causato i primi segni di cambiamento della forma cellulare, mentre lo SASP “cronico” ha spinto molte cellule verso la senescenza e ha aumentato l’espressione di geni legati alla fibrosi e al deposito di matrice extra. Test approfonditi hanno mostrato che lo SASP cronico era ricco di messaggeri infiammatori come IL-8 e IL-17, noti per promuovere l’invecchiamento cellulare, la cicatrizzazione fibrotica e il richiamo di cellule immunitarie. Quando i ricercatori hanno bloccato la via dell’IL-17 o il recettore di IL-8, CXCR2, le cellule esposte allo SASP cronico mostravano meno marcatori di senescenza e minor fibrosi, suggerendo che questi segnali sono motori chiave della malattia.
Eliminare le cellule logore per proteggere la vista
Poiché le cellule senescenti p16-positive erano così strettamente legate alla cicatrizzazione, gli autori hanno verificato se eliminarle potesse proteggere la cornea. In un modello murino in cui la luce UVA induce cambiamenti simili alla FECD, hanno trattato gli animali con una combinazione di farmaci senolitici, Dasatinib più Quercetina, che uccide selettivamente le cellule senescenti. Rispetto ai topi non trattati, quelli sottoposti a terapia senolitica mantenevano un mosaico endoteliale più regolare, conservavano più cellule complessivamente e mostravano meno marcatori di senescenza, fibrosi e matrice in eccesso. In altre parole, eliminare le cellule più danneggiate ha alleggerito il carico di secrezioni dannose e ha contribuito a mantenere una superficie corneale più sana.
Cosa significa per le persone con FECD
Per i pazienti, la FECD porta spesso oggi al trapianto di cornea quando la vista diventa troppo offuscata. Questo studio suggerisce un percorso diverso: la malattia potrebbe essere guidata da una lenta accumulazione di cellule stressate e non dividenti che sia non riescono a svolgere il loro compito sia avvelenano attivamente i vicini con segnali infiammatori e fibrotici. Mirare a questi segnali con farmaci contro le vie di IL-17 o IL-8, oppure usare terapie senolitiche per rimuovere selettivamente le cellule più compromesse, potrebbe un giorno ritardare la cicatrizzazione, preservare più tessuto naturale dell’occhio e posticipare o ridurre la necessità di interventi chirurgici.
Citazione: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Parole chiave: Distrofia di Fuchs, endotelio corneale, senescenza cellulare, fibrosi, terapia senolitica