Clear Sky Science · it
Il DNA mitocondriale guida l’attivazione dell’asse NLRP3-IL-1β nelle microglia legandosi a NLRP3, causando neurodegenerazione in modelli di malattia di Parkinson
Perché questo è importante per la malattia di Parkinson
La malattia di Parkinson è nota soprattutto per i tremori e la lentezza nei movimenti, ma sotto questi sintomi si svolge una battaglia complessa nel cervello. Questo studio rivela come piccoli frammenti di materiale genetico provenienti da mitocondri danneggiati nelle cellule immunitarie cerebrali possano innescare un’infiammazione che gradualmente uccide i neuroni produttori di dopamina necessari per movimenti fluidi. Capire questa catena di eventi apre nuovi bersagli molto specifici per farmaci che potrebbero rallentare o prevenire il danno simile al Parkinson.
Cellule immunitarie cerebrali e centrali elettriche sotto stress
Il cervello contiene non solo neuroni ma anche microglia, le sue cellule immunitarie residenti. Nella malattia di Parkinson, queste microglia spesso diventano iperattive, rilasciando molecole tossiche e segnali infiammatori che danneggiano i neuroni vicini. Gli autori si sono concentrati sui mitocondri, le “centrali” delle cellule, che possiedono il proprio DNA. Quando i mitocondri sono lesionati — per tossine, invecchiamento o altri stress — il loro DNA può ossidarsi, un tipo di danno chimico causato dalle specie reattive dell’ossigeno. Poiché il DNA mitocondriale assomiglia al DNA batterico, questi frammenti danneggiati possono comportarsi come segnali di allarme nel cervello, attivando il sistema immunitario e potenzialmente sostenendo un’infiammazione cronica.
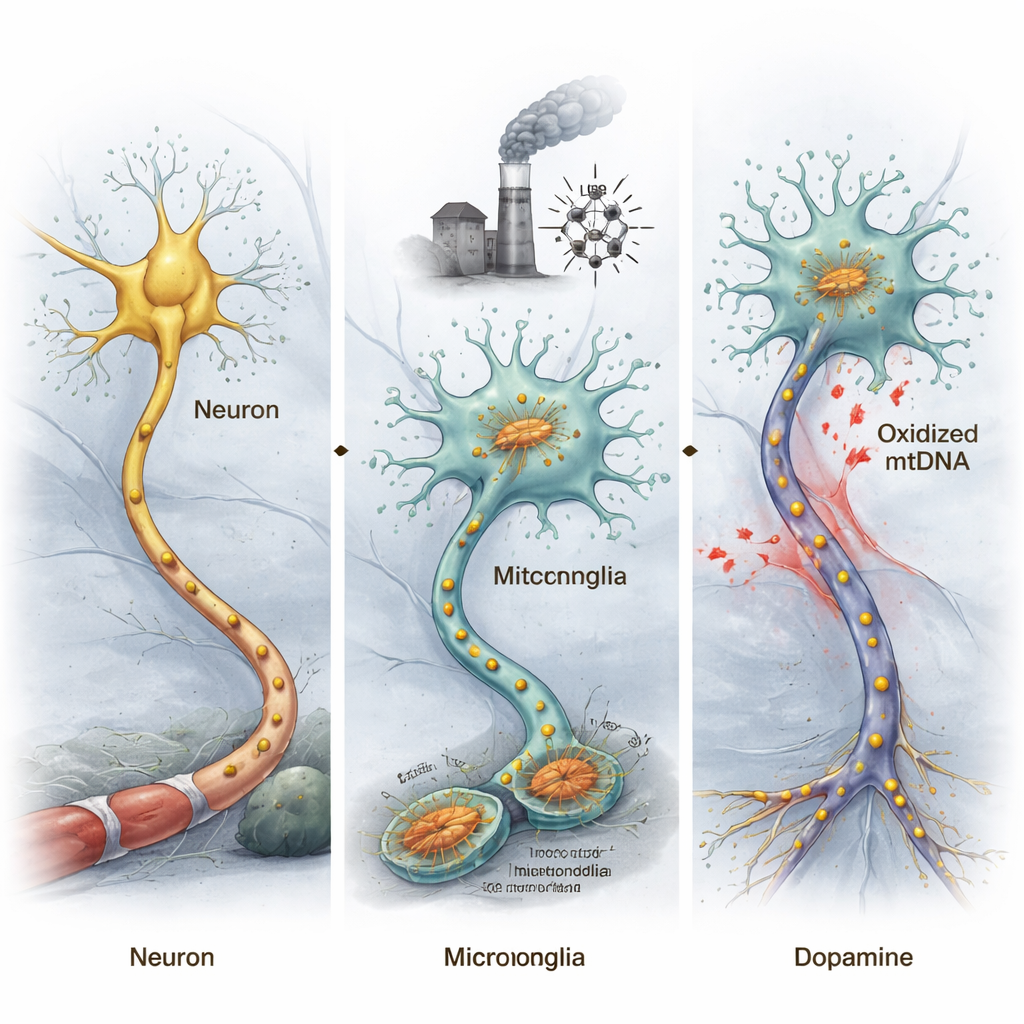
Il DNA mitocondriale danneggiato può spingere i topi verso una malattia simile al Parkinson
Per verificare se il DNA mitocondriale ossidato (ox-mtDNA) può effettivamente scatenare cambiamenti simili al Parkinson, i ricercatori hanno estratto ox-mtDNA da microglia stressate e lo hanno iniettato direttamente in una regione cerebrale che normalmente contiene neuroni produttori di dopamina importanti per il movimento. I topi esposti a questo ox-mtDNA hanno mostrato riduzione del movimento nei test comportamentali e perdita di questi neuroni dopaminergici, riproducendo caratteristiche centrali della malattia di Parkinson. Separando neuroni e microglia del mesencefalo e analizzando la loro attività genica, il team ha trovato che i geni legati al Parkinson diventavano più aberranti nei neuroni, mentre i geni correlati all’infiammazione erano fortemente attivati nelle microglia.
Un interruttore d’allarme molecolare all’interno delle microglia
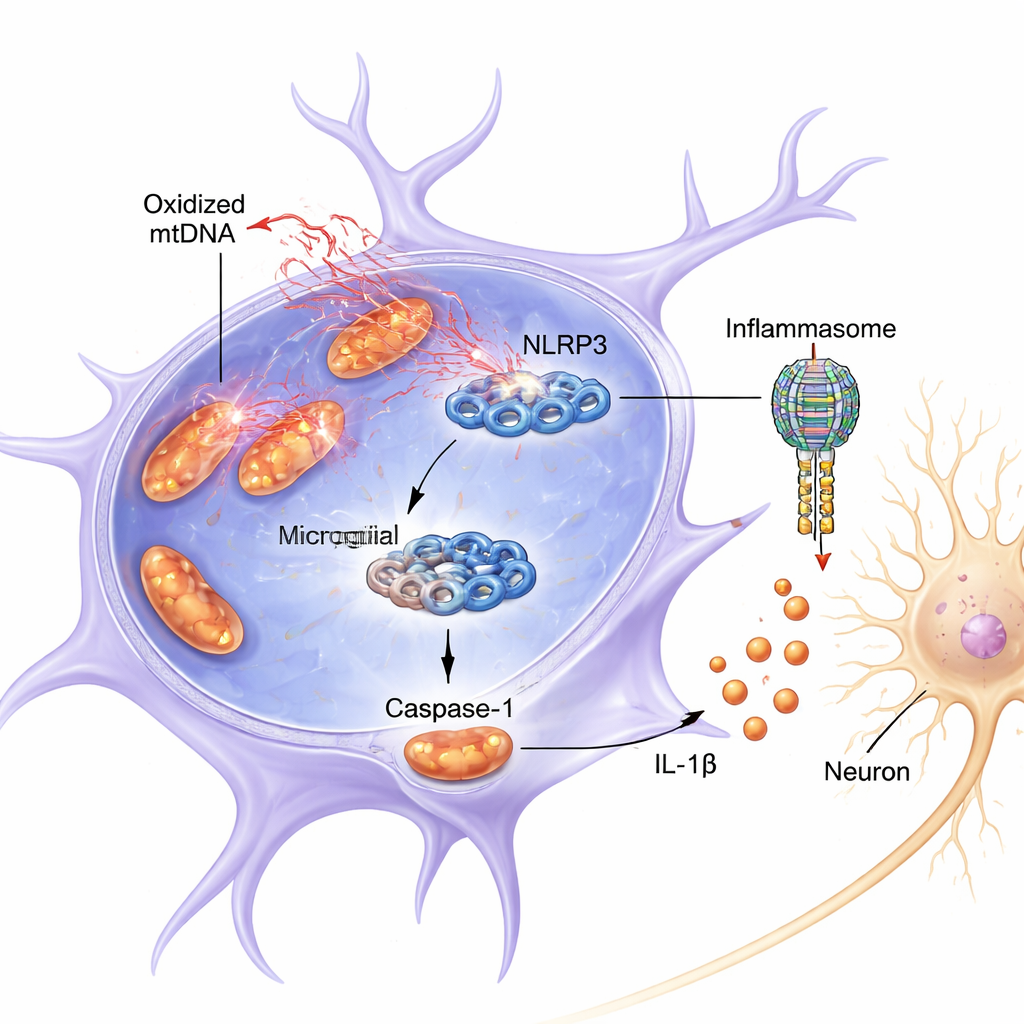
Lo studio si è focalizzato su un complesso proteico nelle microglia chiamato NLRP3, parte di un assemblaggio più ampio noto come inflammasoma. Quando è attivato, NLRP3 contribuisce ad attivare la caspasi-1, un enzima che scinde la molecola infiammatoria IL-1β nella sua forma attiva e dannosa. Sia nei topi sia nelle cellule in coltura, la combinazione di un segnale di priming infiammatorio (LPS, un componente batterico) e la tossina di tipo pesticida rotenone ha fatto sì che i mitocondri nelle microglia rilasciassero DNA mitocondriale ossidato nel citosol. Questo rilascio coincideva con una maggiore attivazione di NLRP3, più caspasi-1 scissa (attiva) e livelli più alti di IL-1β. Il mezzo prelevato da queste microglia iperattivate era direttamente tossico per neuroni simili a quelli dopaminergici coltivati in vitro, riducendo la loro sopravvivenza e il livello del loro marcatore chiave, la tirosina idrossilasi.
Legame diretto: come il DNA ossidato accende l’interruttore NLRP3
Oltre alla semplice correlazione, gli autori hanno mostrato che l’ox-mtDNA non è solo presente durante l’infiammazione: sembra legarsi fisicamente a NLRP3 e attivarlo. Quando hanno bloccato il rilascio del DNA mitocondriale con un farmaco, l’attivazione di caspasi-1 e IL-1β è diminuita. Al contrario, la somministrazione diretta di mtDNA ossidato nelle microglia ha potenziato fortemente la segnalazione di NLRP3, più del mtDNA non ossidato. Usando esperimenti biochimici di pull-down, hanno rilevato mtDNA con marcatori di danno ossidativo legato a NLRP3. Modellizzazione computazionale e chimica delle proteine hanno rivelato che l’ox-mtDNA si lega a un segmento positivo e flessibile di NLRP3 (una “regione intrinsecamente disordinata” che comprende gli amminoacidi 180–187). Quando questa porzione critica è stata rimossa da NLRP3, la sua capacità di legare l’ox-mtDNA e di attivare la caspasi-1 è risultata fortemente ridotta.
Spegnere l’inflammasoma risparmia i neuroni
I ricercatori hanno poi chiesto se interferire con NLRP3 potesse proteggere i neuroni. Nelle microglia in coltura, ridurre geneticamente NLRP3 ha abbassato nettamente l’attivazione di caspasi-1 e IL-1β dopo trattamento con LPS e rotenone, e il mezzo condizionato da queste cellule era molto meno tossico per neuroni simili a quelli dopaminergici. Nei topi, un inibitore selettivo di NLRP3 (MCC950) ha ridotto l’attivazione microgliale, preservato i neuroni dopaminergici e abbassato le proteine correlate all’inflammasoma nei modelli indotti sia da LPS più rotenone sia dall’iniezione di mtDNA. Nel complesso, questi esperimenti mostrano che la catena ox-mtDNA–NLRP3–IL-1β non è solo associata al danno; è necessaria per gran parte della perdita neuronale osservata.
Cosa significa per le future terapie del Parkinson
Per i non specialisti, il messaggio chiave è che il DNA mitocondriale danneggiato che fuoriesce dalle cellule immunitarie cerebrali può legarsi direttamente a un “interruttore d’allarme” interno (NLRP3), scatenando un’ondata di infiammazione che danneggia i neuroni dopaminergici e provoca una malattia simile al Parkinson nei modelli sperimentali. Poiché questa interazione dipende da un segmento corto e definito della proteina NLRP3 e dalla natura ossidata del DNA mitocondriale, offre bersagli farmacologici molto precisi. Terapie che prevengano il danneggiamento o la fuoriuscita del DNA mitocondriale, che blocchino il suo legame a NLRP3 o che inibiscano NLRP3 stesso potrebbero, in linea di principio, attenuare questa cascata infiammatoria e rallentare la progressione della malattia di Parkinson.
Citazione: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Parole chiave: Malattia di Parkinson, microglia, DNA mitocondriale, inflammasoma NLRP3, neuroinfiammazione