Clear Sky Science · it
La carenza mediata da SLC46A1 e la restrizione di folati sopprime l’evoluzione del cancro colorettale tramite riprogrammazione epigenetico-trascrizionale
Perché la vitamina B9 e il cancro intestinale formano una coppia inaspettata
Molti conoscono il folato, o vitamina B9, come un nutriente importante in gravidanza e per la salute cardiovascolare. Questo studio mostra che il folato svolge anche un ruolo sorprendente nel cancro del colon e del retto. Il colpo di scena è che il beneficio del folato dipende da una singola proteina “guardiana” presente sulle cellule tumorali, chiamata SLC46A1, che decide quanto folato arriva effettivamente all’interno delle cellule tumorali. Comprendere questa porta nascosta può aiutare a spiegare perché studi precedenti su folato e cancro sono stati così contraddittori e potrebbe orientare un uso più sicuro del folato in dieta e terapie.
Un guardiano del nutriente nell’intestino
Le cellule del nostro intestino non possono sintetizzare il folato da sole; devono prelevarlo dall’ambiente circostante usando specifici trasportatori. Gli autori dimostrano che SLC46A1 è il principale trasportatore di folato nel colon umano, molto più attivo rispetto ad altri noti vettori del folato. Analizzando grandi banche dati pubbliche sul cancro e campioni tissutali di pazienti, hanno rilevato che i livelli di SLC46A1 erano fortemente ridotti nei tumori colorettali rispetto al tessuto sano vicino. I tumori con meno SLC46A1 tendevano a essere più avanzati, più propensi a metastatizzare e associati a una sopravvivenza peggiore dei pazienti, suggerendo che questo trasportatore si comporti più come un freno che come un acceleratore in questo tipo di cancro.
Come la perdita della porta modifica il comportamento del cancro
Per verificare cosa faccia realmente SLC46A1, i ricercatori hanno modulato i suoi livelli nelle linee cellulari di cancro colorettale. Quando hanno abbassato SLC46A1, le cellule tumorali crescevano più rapidamente, migravano con maggiore facilità e invadevano barriere artificiali in vitro. Quando hanno aumentato SLC46A1 in cellule che ne avevano bassi livelli all’inizio, le cellule sono diventate meno invasive. Pattern simili sono emersi nei topi: i tumori derivati da cellule carenti di SLC46A1 erano più grandi e producevano più metastasi polmonari. Allo stesso tempo, tumori e cellule coltivate con meno SLC46A1 contenevano meno folato all’interno, confermando che questa proteina funziona davvero come un punto chiave di ingresso per la vitamina.
Dalla carenza vitaminica al controllo dei geni alterato
Il folato fa più che aiutare a costruire i mattoni del DNA; alimenta anche un sistema chimico che pone piccole “etichette” metiliche sul DNA, che aiutano ad accendere o spegnere i geni. Il gruppo ha mostrato che quando SLC46A1 viene perso e il folato intracellulare diminuisce, la capacità complessiva di aggiungere queste etichette cala. Questo, a sua volta, rimuove selettivamente le metilazioni dalla regione regolatoria di un gene chiamato FOS, noto per promuovere la proliferazione cellulare. Senza quelle etichette, FOS si attiva e accende diversi geni di “crescita e diffusione”, inclusi CCND1, BCL2 e PLAU, che aiutano le cellule tumorali a dividersi, sfuggire alla morte e invadere i tessuti circostanti. Bloccare FOS o PLAU ha in gran parte annullato la crescita e l’invasività extra causate dalla perdita di SLC46A1, collegando insieme questa catena di eventi.
Quando il folato aiuta solo se la porta è aperta
Lo studio chiarisce anche quando il folato è favorevole o dannoso per i tumori. In colture cellulari cresciute in condizioni povere di folato, reintegrare il folato a livelli simili a quelli del sangue umano ha rallentato la crescita e la mobilità delle cellule tumorali—ma solo se SLC46A1 era presente per portare il folato all’interno. Nei tumori nei topi, iniezioni dirette di folato nella massa tumorale ne hanno ridotto la crescita e i segni di divisione cellulare, ancora una volta solo quando le cellule cancerose esprimevano SLC46A1. I tumori privi del trasportatore hanno risposto appena. Nei campioni dei pazienti, i ricercatori hanno osservato un pattern inverso: i tumori con alto SLC46A1 avevano meno folato nel fluido circostante, come se lo assorbissero efficacemente, e presentavano livelli più bassi di FOS e PLAU. I tumori con basso SLC46A1 lasciavano più folato inutilizzato e avevano livelli più alti di questi marker aggressivi.
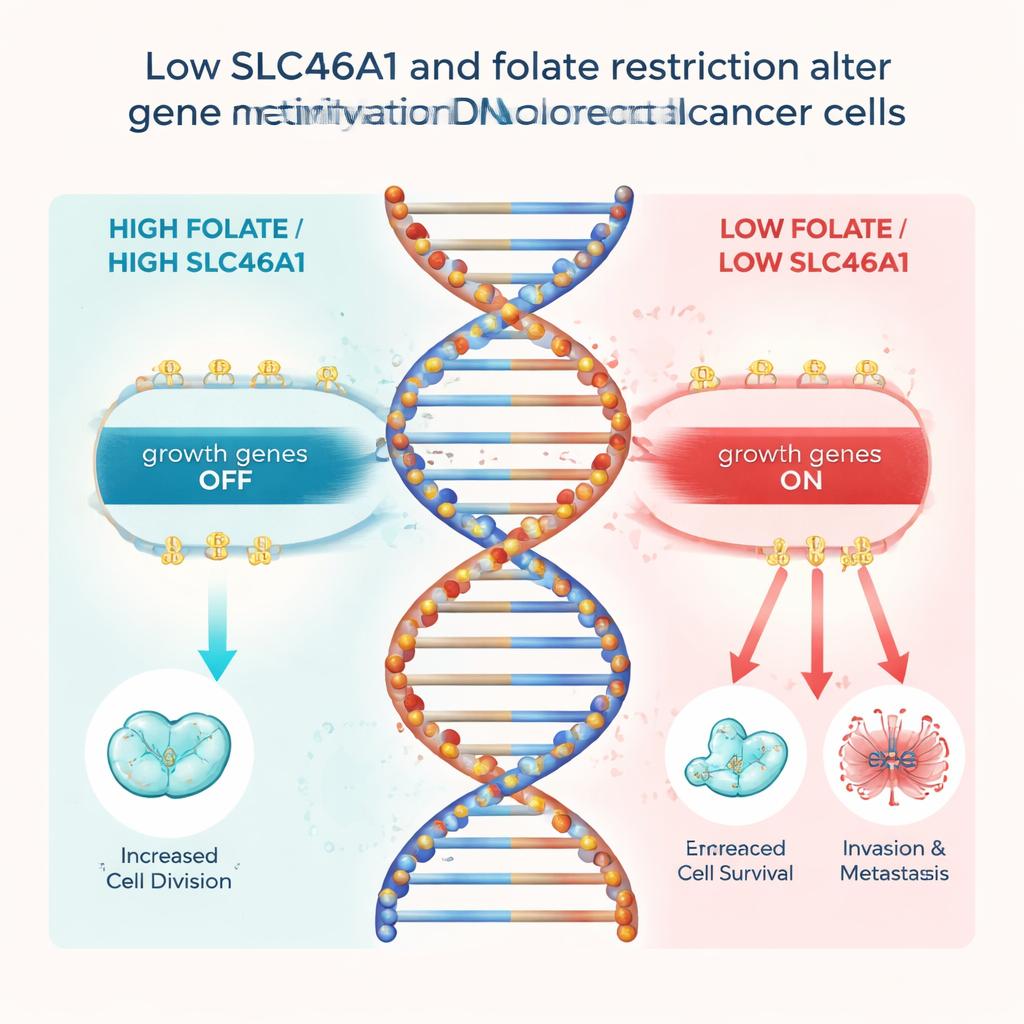
Cosa significa per i pazienti e la prevenzione
Per un lettore non specialista, il messaggio principale è che l’impatto del folato sul cancro colorettale dipende dal fatto che le cellule tumorali esprimano ancora la “porta” SLC46A1 che permette l’ingresso del folato. Quando la porta è presente, quantità realistiche di folato possono sostenere una corretta metilazione del DNA e aiutare a mantenere sotto controllo i geni che guidano la crescita. Quando la porta manca, il tumore non può usare il folato in modo protettivo e tende invece verso uno stato più aggressivo guidato da geni deregolati come FOS. Questo lavoro suggerisce che in futuro lo screening dei tumori colorettali per i livelli di SLC46A1 potrebbe aiutare i medici a prevedere la prognosi e decidere se diete o terapie correlate al folato siano probabilmente utili, rappresentando un passo verso una cura del cancro più personalizzata e consapevole del ruolo dei nutrienti.
Citazione: Zhou, Y., Liu, Y., Liu, Y. et al. SLC46A1 deficiency-mediated folate restriction suppresses colorectal cancer progression through epigenetic-transcriptional reprogramming. Cell Death Dis 17, 189 (2026). https://doi.org/10.1038/s41419-026-08423-8
Parole chiave: folato, cancro colorettale, epigenetica, SLC46A1, metilazione del DNA