Clear Sky Science · it
Lattilazione di SLC26A3 nell’ambiente tumorale acido promuove la progressione maligna del carcinoma colorettale
Perché l’acidità del tumore è importante
Il cancro colorettale rimane uno dei tumori più letali a livello globale, in parte perché i tumori spesso recidivano, si diffondono o smettono di rispondere ai farmaci. Questo studio indaga un colpevole sottovalutato dietro questi comportamenti: l’ambiente acido, ricco di acido lattico, all’interno dei tumori. Scoprendo come questo ambiente ostile destabilizzi una proteina di membrana protettiva chiamata SLC26A3, gli autori rivelano una nuova catena di eventi che aiuta le cellule tumorali a diventare più simili a cellule staminali, più invasive e resistenti ai farmaci — offrendo idee nuove per il trattamento.
Un vicinato ostile intorno alle cellule tumorali
I tumori in rapida crescita consumano grandi quantità di zuccheri e ossigeno, rilasciando acido lattico e ioni idrogeno che rendono il loro ambiente acido. Utilizzando ampi set di dati di pazienti e campioni tissutali, i ricercatori mostrano che questo stato acido, rilevato tramite una proteina marcatore chiamata CA9, è associato a tumori colorettali aggressivi. Nei tumori più avanzati i livelli di CA9 sono elevati, mentre quelli di SLC26A3 risultano costantemente bassi. SLC26A3 normalmente si trova sulla superficie delle cellule del colon e aiuta a bilanciare sali e bicarbonato, contribuendo così al controllo dell’acidità. Nei campioni tumorali, nelle linee cellulari tumorali e nelle analisi a singola cellula, il gruppo rileva che quando aumenta l’acidità, i livelli di SLC26A3 diminuiscono — soprattutto nelle cellule tumorali maligne e con caratteristiche di cellule staminali. 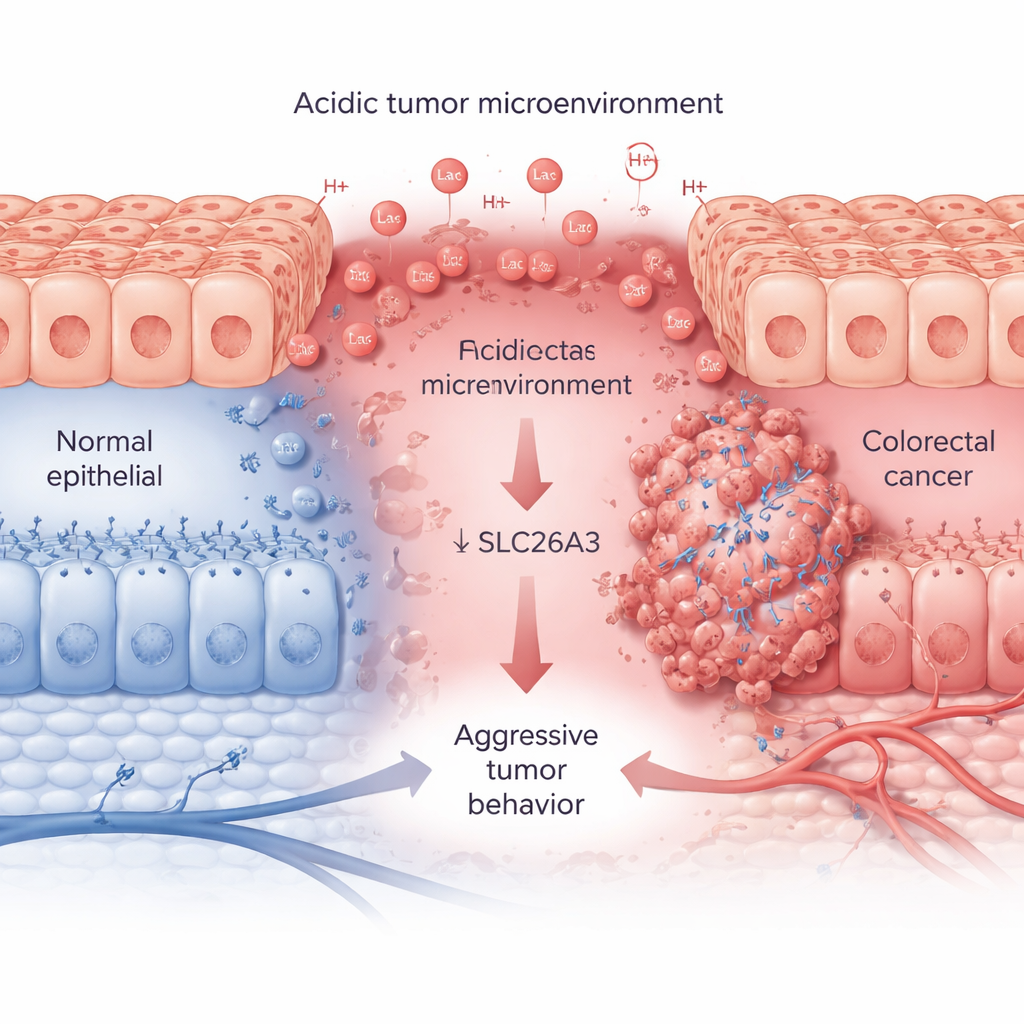
Come l’acido lattico segnala un bersaglio per la distruzione
Gli autori si chiedono quindi perché SLC26A3 diminuisca nei tumori acidi. Si concentrano sulla lattilazione, un’etichetta chimica recentemente scoperta derivata dall’acido lattico che può essere aggiunta alle proteine. Quando le cellule di carcinoma colorettale vengono esposte ad acido lattico o coltivate in condizioni acide, SLC26A3 risulta fortemente lattilata. L’analisi dettagliata delle proteine individua un sito chiave, un amminoacido chiamato K536, su cui viene aggiunto questo segno. La lattilazione su K536 rende SLC26A3 meno stabile: la proteina è più soggetta ad essere marcata con ubiquitina, un segnale cellulare di “smaltire questo”, e inviata ai meccanismi di riciclo della cellula. Bloccare l’enzima p300, che contribuisce all’aggiunta dei marchi di lattilazione, protegge parzialmente SLC26A3 dalla degradazione. Di conseguenza, acidità e lattato creano un circuito vizioso dannoso — più lattato porta a più lattilazione, che riduce SLC26A3, alterando ulteriormente l’equilibrio del pH e favorendo un microambiente ancora più acido.
Disinnescare un freno su staminalità e diffusione tumorale
Con SLC26A3 esaurito, le cellule tumorali si comportano in modo più aggressivo. In colture cellulari, le cellule tumorali colorettali con carattere staminale esprimono naturalmente meno SLC26A3 rispetto ai loro omologhi non staminali. Quando i ricercatori riducono intenzionalmente i livelli di SLC26A3, le cellule tumorali formano più sfere (un segno di staminalità), si autorinnovano più efficacemente, invadono membrane artificiali e migrano più rapidamente attraverso ferite da graffio. Diventano anche meno sensibili a chemioterapici comuni come ossaliplatino e 5‑fluorouracile. Al contrario, aumentare SLC26A3 riduce i marcatori di staminalità e rallenta invasione e migrazione — ma questo vantaggio viene attenuato quando si aggiunge lattato extra, sottolineando come l’acidità possa sovrastare l’effetto protettivo.
Un legame nascosto con il controllo genico
Oltre a contribuire al controllo dell’acidità, SLC26A3 funge anche da impalcatura che lega due proteine leganti l’RNA, HuR e CUGBP1. Queste proteine controllano la durata di molti RNA messaggeri che codificano proteine rilevanti nel cancro. Quando SLC26A3 è abbondante, sequestra parte di HuR e CUGBP1, limitando la loro capacità di stabilizzare o destabilizzare fortemente determinati messaggi legati al cancro. Quando SLC26A3 viene perso mediante lattilazione e degradazione, HuR e CUGBP1 sono più liberi di legare mRNA oncogenici che promuovono staminalità, transizione epitelio‑mesenchimale (EMT), invasione e sopravvivenza. Gli esperimenti mostrano che HuR aiuta a stabilizzare mRNA di marcatori di staminalità e di proteine delle giunzioni cellulari, mentre CUGBP1 può opporsi a HuR per alcuni bersagli, riducendo l’integrità delle giunzioni e favorendo l’EMT — entrambi favoriscono la diffusione tumorale.
Riequilibrare l’ambiente per combattere il cancro
Per verificare se queste intuizioni possano diventare strategie terapeutiche, i ricercatori utilizzano modelli murini di carcinoma colorettale. Neutralizzare l’acidità tumorale con bicarbonato di sodio, bloccare il trasporto di lattato con un inibitore di MCT1 o sovraesprimere SLC26A3 rallenta tutti la crescita tumorale. Combinare il ripristino di SLC26A3 con la chemioterapia riduce ulteriormente i tumori. Nei dati dei pazienti, livelli più alti di SLC26A3 si correlano con una migliore sopravvivenza, meno recidive, meno metastasi e risposte migliori alla chemioterapia, suggerendo che questa proteina potrebbe servire sia come biomarcatore sia come bersaglio terapeutico. 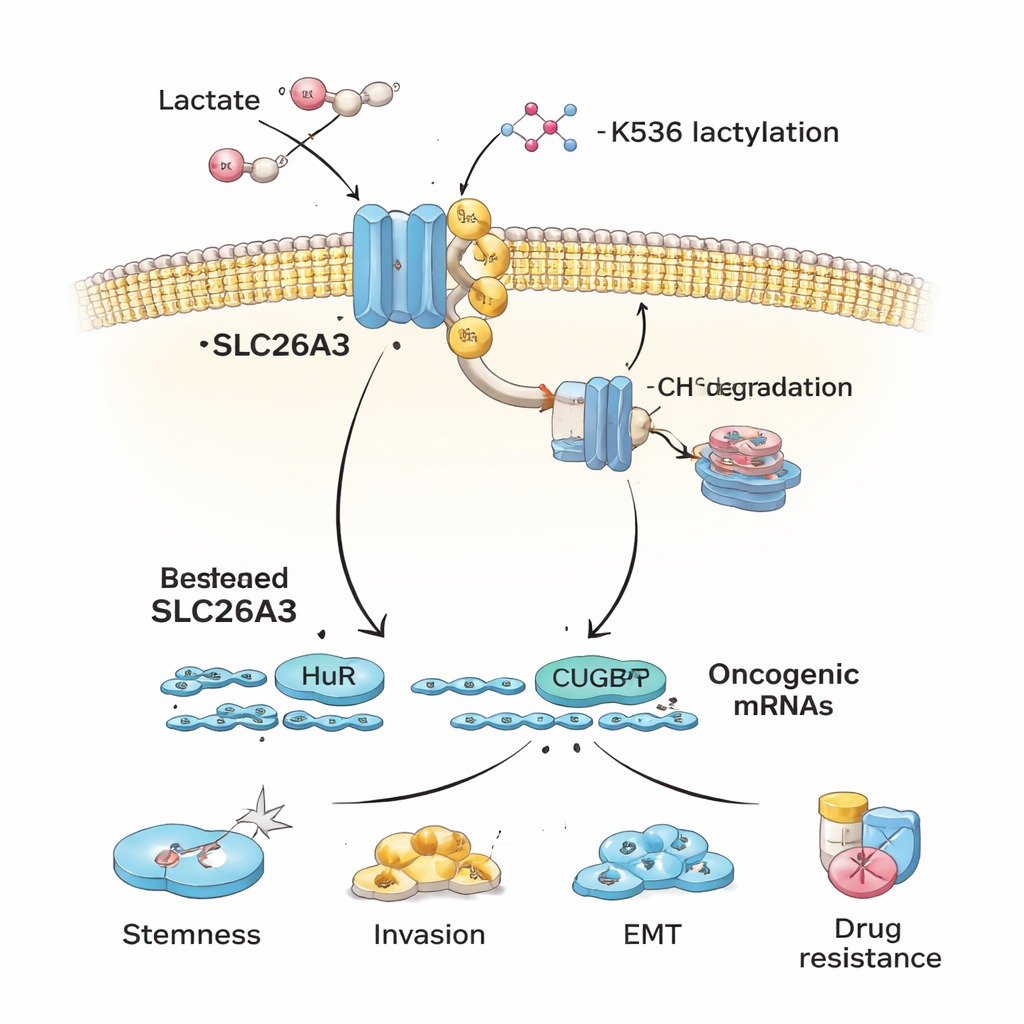
Cosa significa per i pazienti
In termini pratici, questo studio mostra che i tumori colorettali prosperano in un bagno aspro, ricco di acido lattico che chimicamente «etichetta» e distrugge un guardiano protettivo, SLC26A3. Una volta che questo guardiano viene meno, le cellule tumorali adottano più facilmente caratteristiche di cellule staminali, si diffondono e resistono ai trattamenti, favorite da potenti regolatori dell’RNA all’interno della cellula. Neutralizzando l’acidità tumorale, bloccando la gestione del lattato o ripristinando SLC26A3, potrebbe essere possibile indebolire quel circuito vizioso maligno e rendere più efficaci le terapie standard. Sebbene tali approcci richiedano ancora rigorosi test clinici, aprono una nuova e promettente prospettiva su come la gestione dell’ambiente chimico del tumore potrebbe aiutare a controllare il cancro colorettale.
Citazione: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Parole chiave: cancro colorettale, microambiente tumorale, lattilazione, cellule staminali tumorali, resistenza alla chemioterapia