Clear Sky Science · it
Mirare GNG4 inibisce la progressione tumorale e ripristina la sensibilità a enzalutamide nel cancro alla prostata sopprimendo l’autofagia
Perché questa ricerca è importante
Per molti uomini con cancro alla prostata avanzato, potenti farmaci che bloccano gli ormoni come l’enzalutamide funzionano bene all’inizio ma poi perdono efficacia gradualmente. Questo studio mette in luce un trucco di sopravvivenza usato dalle cellule tumorali e individua una proteina specifica, chiamata GNG4, che aiuta i tumori a continuare a crescere e a eludere il trattamento. Comprendere questo meccanismo potrebbe portare a terapie combinate che rendono i farmaci attuali più efficaci e duraturi.
Un interruttore proteico nascosto in bella vista
Le cellule del cancro alla prostata sono fortemente guidate dagli ormoni maschili, quindi la cura standard per la malattia avanzata interrompe questi segnali. Tuttavia la maggior parte dei tumori diventa infine “resistente alla castrazione” e ricomincia a crescere. Gli autori hanno cercato geni molto più attivi nel tessuto tumorale rispetto al tessuto prostatico sano adiacente dei medesimi pazienti. Tra diversi candidati, GNG4 si è distinto: quando ne hanno ridotto i livelli nelle cellule di cancro prostatico, la crescita delle cellule tumorali è calata bruscamente. Analisi su centinaia di campioni dei pazienti hanno confermato che GNG4 è più elevato nei tumori prostatici primari rispetto al tessuto normale ed è particolarmente aumentato nei tumori più aggressivi e di grado più alto.
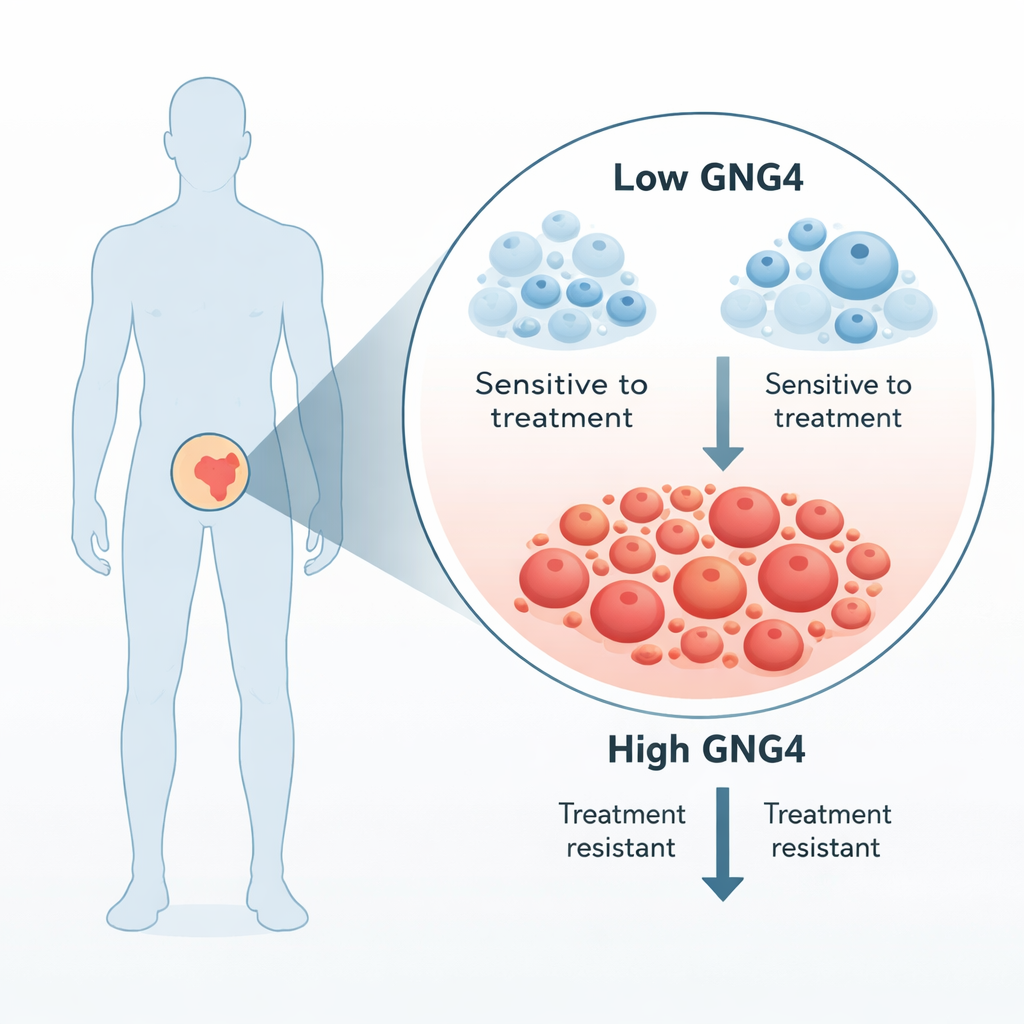
Come GNG4 aiuta i tumori a prosperare
GNG4 fa parte di una famiglia di segnali più ampia nota come proteine G, che si trovano nella membrana cellulare e trasmettono segnali dall’esterno all’interno della cellula. Il gruppo ha dimostrato che ridurre GNG4 in linee cellulari di cancro alla prostata rallentava la divisione cellulare, induceva l’arresto in una fase di controllo del ciclo cellulare e aumentava la morte cellulare programmata. Questi cambiamenti hanno anche ridotto la capacità delle cellule tumorali di migrare e chiudere lesioni nei test in vitro, e i tumori derivati da cellule carenti di GNG4 sono cresciuti più lentamente nei topi. Complessivamente, i risultati suggeriscono che GNG4 funziona come un acceleratore per la crescita e la diffusione del cancro alla prostata.
Autofagia: la dispensa di emergenza della cellula tumorale
I ricercatori si sono quindi concentrati su un processo chiamato autofagia, in cui le cellule degradano e riciclano componenti propri per sopravvivere a stress come la fame o il trattamento farmacologico. In molti tumori avanzati, l’autofagia funge da dispensa di emergenza che aiuta le cellule tumorali a far fronte a condizioni avverse. In questo studio, le cellule di cancro alla prostata con alta attività di GNG4 mostravano più segni di autofagia attiva, mentre le cellule con GNG4 silenziato avevano meno strutture di riciclo e livelli più bassi di marker chiave dell’autofagia. Quando GNG4 era sovraespresso, le cellule tolleravano meglio l’enzalutamide e subivano meno morte cellulare. Bloccare l’autofagia con un inibitore chimico annullava gran parte di questa protezione, indicando che GNG4 aiuta i tumori a sopportare il trattamento in larga parte aumentando questo sistema di riciclo.
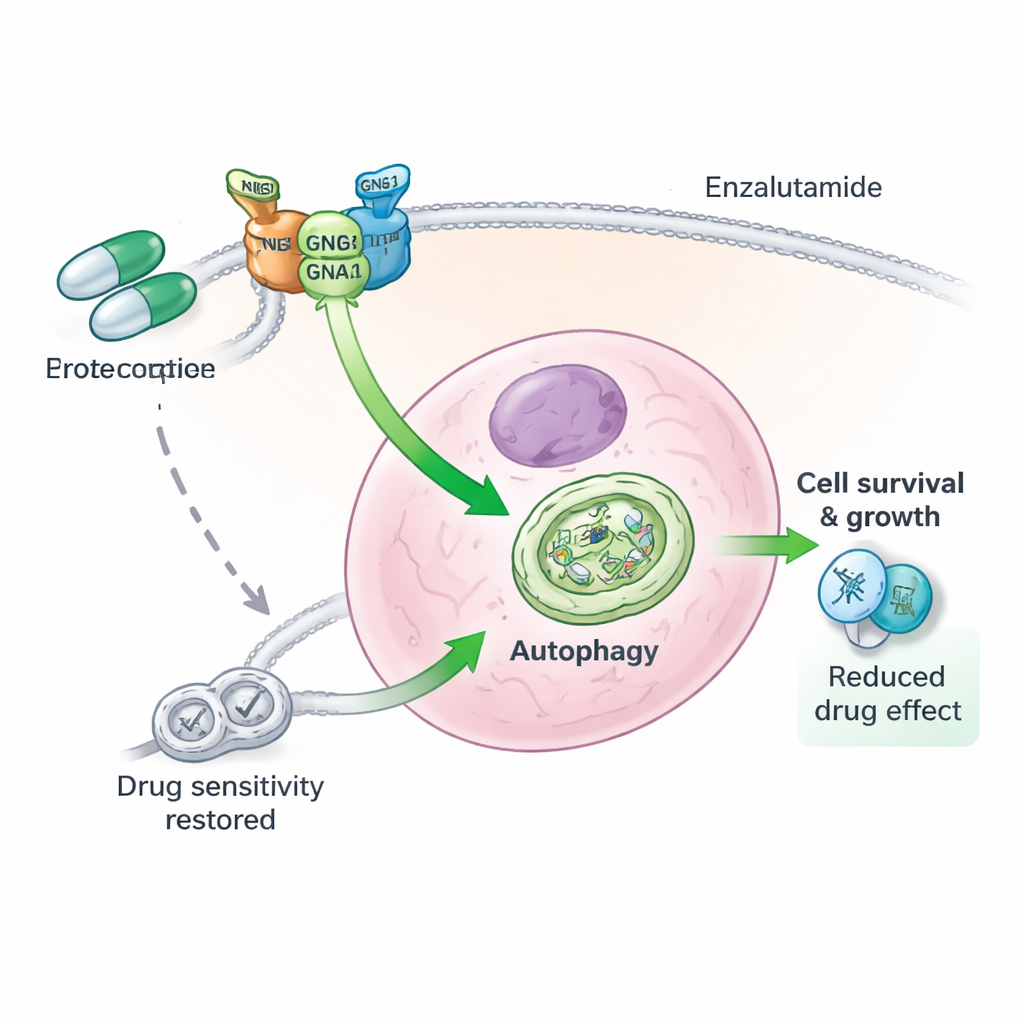
Un trio proteico dietro la resistenza ai farmaci
Approfondendo, gli autori hanno scoperto che GNG4 non agisce da solo. Si associa fisicamente con un’altra subunità delle proteine G, GNB1, per stabilizzare una terza proteina, GNAI3. Insieme, queste tre subunità formano un complesso funzionale che potenzia l’autofagia nelle cellule del cancro alla prostata. Quando GNG4 veniva ridotto, la proteina GNAI3 veniva più rapidamente taggata per la distruzione e degradata dai sistemi di smaltimento cellulare, spegnendo il segnale di autofagia. L’eliminazione di GNAI3 annullava i vantaggi di crescita e sopravvivenza conferiti da un eccesso di GNG4, sia nelle cellule coltivate che nei tumori nei topi. In altre parole, GNG4 guida la malignità e la resistenza allo stress per lo più attraverso questo asse GNG4–GNB1–GNAI3.
Rendere i farmaci attuali più efficaci
Infine, il gruppo ha valutato cosa succede quando il targeting di GNG4 viene combinato con l’enzalutamide, un farmaco di riferimento per il cancro alla prostata avanzato. In laboratorio, il silenziamento di GNG4 ha reso le cellule tumorali nettamente più sensibili all’enzalutamide e ha ridotto la loro capacità di formare colonie dopo il trattamento. Nei topi, i tumori con GNG4 ridotto si sono ristretti maggiormente quando venivano trattati con enzalutamide rispetto ai tumori con livelli normali di GNG4, senza tossicità aggiuntiva evidente. Bloccare direttamente l’autofagia ha prodotto miglioramenti simili. Questi risultati suggeriscono che interferire con l’autofagia indotta da GNG4 può privare le cellule tumorali di un meccanismo vitale di adattamento, consentendo alle terapie ormonali esistenti di infliggere un colpo più forte e duraturo.
Cosa significa per i pazienti
Per un non specialista, il messaggio chiave è che alcuni tumori alla prostata sopravvivono al trattamento attivando un sistema interno di riciclo che funziona come un generatore di riserva. Questo studio identifica GNG4 come l’interruttore principale che accende quel sistema, lavorando insieme a proteine partner per proteggere le cellule tumorali dall’enzalutamide. Disattivando questo interruttore — sia mirando direttamente a GNG4 sia attenuando in modo sicuro l’autofagia — le terapie future potrebbero rallentare la crescita tumorale e ripristinare la sensibilità ai farmaci negli uomini con tumori diventati difficili da trattare.
Citazione: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Parole chiave: cancro alla prostata, resistenza ai farmaci, autofagia, proteine G, enzalutamide