Clear Sky Science · it
Profilo preclinico di coniugati anticorpo-farmaco diretti contro il condroitin solfato oncofetale
Perché questa ricerca è importante per il trattamento futuro del cancro
I farmaci antitumorali spesso agiscono come un bombardamento indiscriminato: colpiscono le cellule in rapida crescita in tutto il corpo, non solo nei tumori, causando effetti collaterali pesanti e talvolta non raggiungendo tutte le cellule tumorali. Questo studio esplora un approccio più intelligente che combina la precisione degli anticorpi con la potenza dei chemioterapici, e prende di mira una struttura presente in molti tumori ma quasi assente nei tessuti sani. Per un lettore non specialista, offre un’idea di come le terapie oncologiche future potrebbero essere più efficaci e meno dannose.
Una “bandiera” speciale presente solo nei tumori
I ricercatori si concentrano su una molecola chiamata condroitin solfato oncofetale, o ofCS. Si tratta di un rivestimento simile a uno zucchero che compare durante lo sviluppo fetale, scompare nella maggior parte dei tessuti adulti sani e poi riemerge in molti tumori. Si trova non solo sulle cellule tumorali stesse, ma anche nell’impalcatura e nelle cellule di supporto intorno al tumore. Questo lo rende un bersaglio particolarmente attraente: colpire ofCS potrebbe significare aggredire sia il tumore sia il suo “terreno” risparmiando per lo più gli organi normali. Il gruppo ha precedentemente identificato un frammento di anticorpo, chiamato Vartumab, che riconosce ofCS in un’ampia varietà di tumori solidi con pochissimo legame ai tessuti normali.
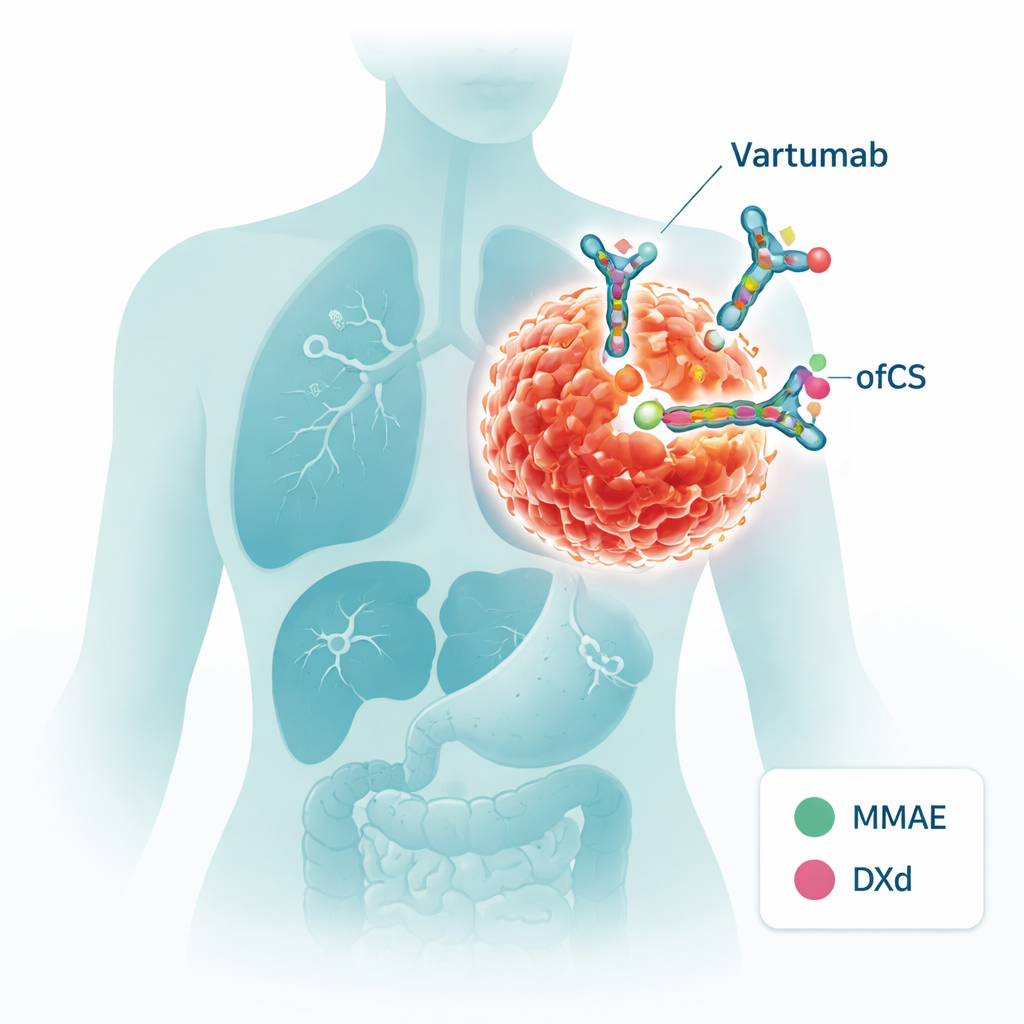
Progettare un missile guidato contro i tumori
In questo lavoro, Vartumab viene trasformato in un coniugato anticorpo–farmaco (ADC) — essenzialmente un missile guidato che trasporta una testata tossica. Gli scienziati hanno attaccato due diversi payload chemioterapici, MMAE e DXd, ciascuno tramite un “linker” chimico che può essere tagliato da enzimi comunemente presenti nell’ambiente tumorale. Quando Vartumab si lega a ofCS, questi linker possono essere scissi, rilasciando il farmaco esattamente dove serve. Il gruppo ha verificato con cura che gli anticorpi modificati restassero stabili in condizioni simili al sangue, rilasciassero il payload se esposti a enzimi correlati al tumore e, cosa fondamentale, riconoscessero ancora ofCS altrettanto bene come il Vartumab originale.
Colpire le cellule tumorali e i loro vicini
Una caratteristica chiave dei payload scelti è l’“effetto di prossimità” (bystander effect). Una volta rilasciati, MMAE e DXd sono in grado di diffondere fuori dalla prima cellula che uccidono ed entrare nelle cellule vicine, anche se questi vicini non esprimono il bersaglio ofCS. I ricercatori hanno testato questo mescolando cellule di melanoma positive per ofCS con cellule ingegnerizzate negative per ofCS. Gli ADC che trasportavano MMAE o DXd hanno ucciso non solo le cellule bersaglio, ma anche i vicini privi del bersaglio in modo dipendente dalla frazione di cellule ofCS-positive presenti. Al contrario, un ADC di controllo con un payload meno permeabile (MMAF) ha ucciso solo le cellule direttamente bersagliate e non ha prodotto un forte effetto di prossimità.
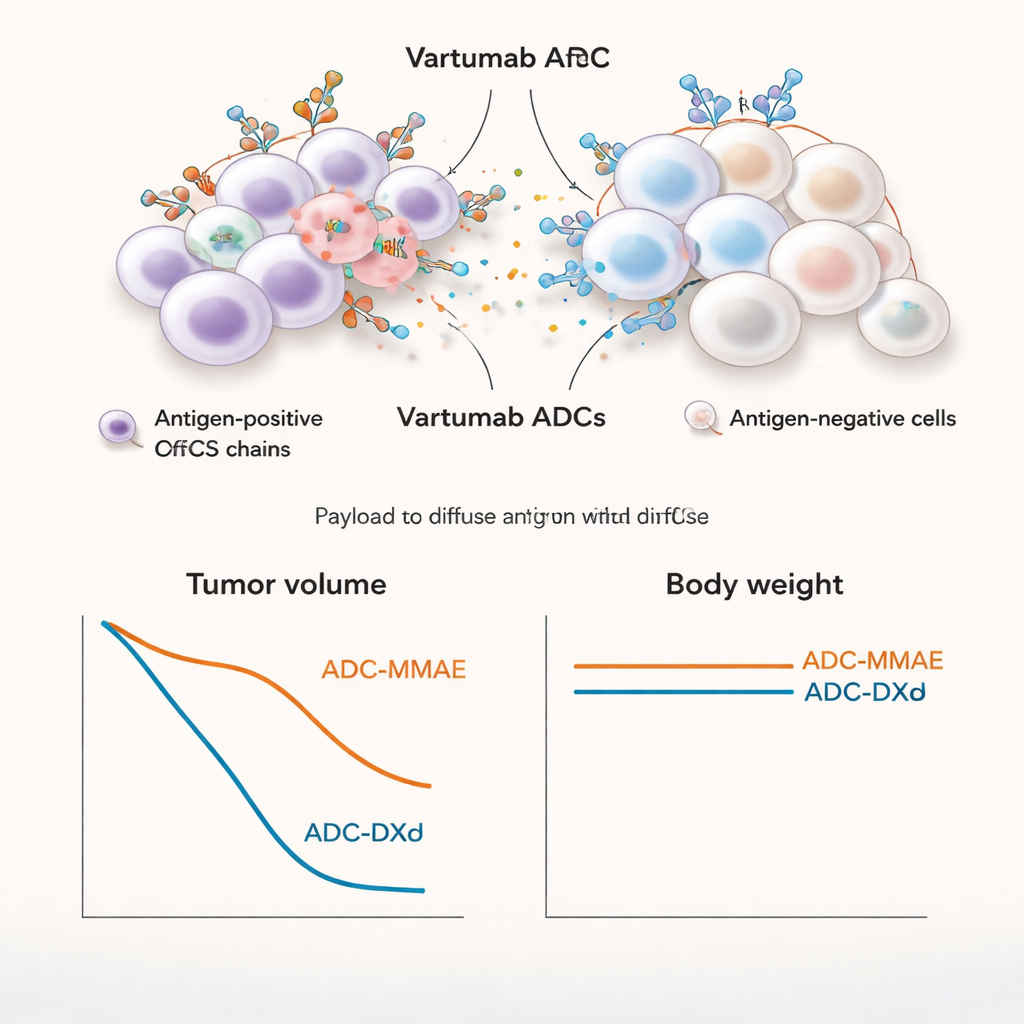
Forte riduzione tumorale con danni fuori bersaglio limitati
Passando a modelli murini di melanoma e cancro polmonare, gli ADC Vartumab si sono accumulati in modo consistente nei tumori mostrando livelli molto più bassi in altri organi. La versione con MMAE è risultata particolarmente potente: a dosi relativamente basse ha completamente fatto regredire tumori già stabiliti, incluso in un modello di cancro polmonare con livelli più bassi di ofCS. Anche la versione DXd ha prodotto una forte regressione tumorale, sebbene in genere abbia richiesto dosi più elevate. Quando il team ha confrontato MMAE con il non-bystander MMAF nei topi, solo l’ADC con MMAE capace di effetto di prossimità ha ottenuto una completa e duratura eliminazione del tumore, sottolineando l’importanza di uccidere sia le cellule tumorali sia le cellule stromali di supporto. Nei ratti, somministrazioni ripetute dell’ADC con MMAE fino a 5 mg/kg sono state ben tollerate, con peso corporeo, esami del sangue ed esami tissutali che hanno mostrato solo cambiamenti lievi e reversibili simili agli effetti noti di farmaci approvati correlati.
Cosa potrebbe significare per i pazienti
Per i non specialisti, il messaggio è che questo studio affina una promettente strategia di “cerca e distruggi” contro il cancro. Concentrandosi su ofCS — un marcatore ampiamente presente nei tumori ma raro nei tessuti normali — e usando payload che possono estendersi alle cellule vicine, gli ADC Vartumab attaccano non solo la massa tumorale visibile, ma anche il suo ambiente di supporto e le cellule tumorali nascoste che altrimenti potrebbero sfuggire. Il lavoro è ancora preclinico, ma suggerisce una strada verso farmaci futuri più mirati al tumore, efficaci in diversi tipi di cancro e potenzialmente in grado di evitare alcuni degli effetti collaterali più gravi della chemioterapia convenzionale.
Citazione: Skafte, A., Vidal-Calvo, E.E., Choudhary, S. et al. Preclinical profiling of antibody drug conjugates targeting oncofetal chondroitin sulfate. Cell Death Dis 17, 162 (2026). https://doi.org/10.1038/s41419-026-08420-x
Parole chiave: coniugati anticorpo-farmaco, condroitin solfato oncofetale, effetto di prossimità, terapia mirata contro il cancro, microambiente tumorale