Clear Sky Science · it
DNA-PKcs orchestra la senescenza indotta dalla deplezione di CTLA-4 nelle cellule tumorali
Trasformare l’interruttore della crescita del cancro in un segnale di stop
I farmaci oncologici basati sul sistema immunitario spesso puntano a una molecola chiamata CTLA-4, presente sulle cellule immunitarie, per aiutare l’organismo ad attaccare i tumori. Questo studio rivela una svolta sorprendente: CTLA-4 si trova anche all’interno delle cellule tumorali e può comportarsi come un aiuto nascosto per la crescita. Quando gli scienziati hanno rimosso deliberatamente questo CTLA-4 intracellulare dalle cellule di melanoma, le cellule tumorali hanno smesso di moltiplicarsi e sono entrate in uno stato di “pensionamento” a lungo termine noto come senescenza cellulare. Capire questo ruolo inaspettato apre nuove strade per rallentare o persino ridurre i tumori mirando a CTLA-4 all’interno delle cellule tumorali, non solo sulle cellule immunitarie.
Quando le cellule scelgono la pensione invece della crescita incontrollata
Le cellule normalmente si dividono, riparano i danni e—quando il danno è irreparabile—muoiono oppure entrano in senescenza, un arresto permanente della crescita. Le cellule senescenti tipicamente aumentano di dimensione, cambiano forma e producono marker specifici che gli scienziati possono rilevare in laboratorio. I ricercatori hanno osservato che quando riducevano CTLA-4 all’interno di cellule di melanoma murine e umane, le cellule diventavano più grandi, la loro proliferazione calava nettamente e aumentavano segnali classici di senescenza, incluse attività enzimatiche rilevabili con colorazioni specifiche e proteine come p16 e p21 che bloccano il ciclo cellulare. Questi cambiamenti sono stati osservati sia quando CTLA-4 è stato temporaneamente silenziato sia quando è stato eliminato in modo permanente con strumenti di editing genetico.
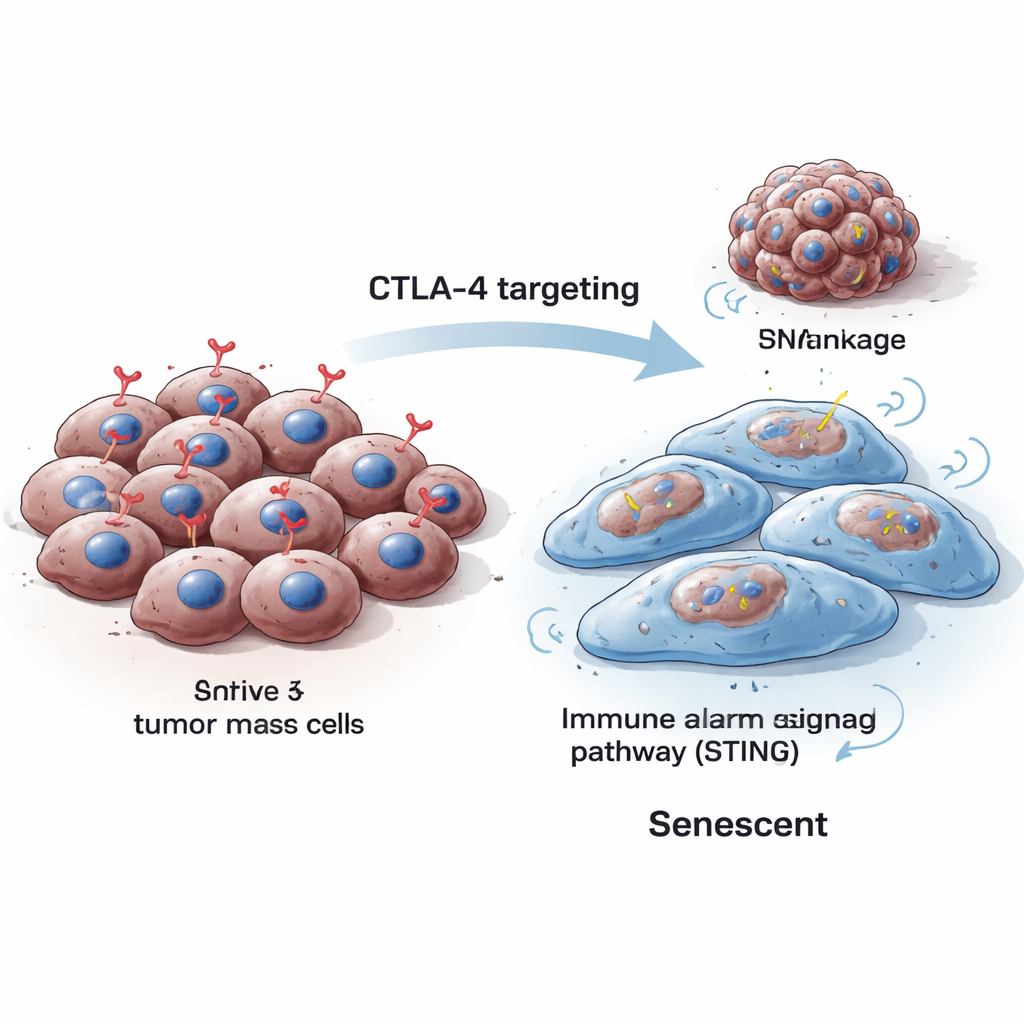
Crepe nel progetto genetico che portano a uno stallo
Per capire perché la perdita di CTLA-4 spinge le cellule tumorali verso la senescenza, il team ha esaminato come queste cellule gestiscono il loro DNA durante la divisione. Hanno scoperto che la deplezione di CTLA-4 riduceva i livelli di Aurora B, una proteina che aiuta i cromosomi a separarsi correttamente durante la divisione cellulare. Quando Aurora B diminuiva, le cellule sviluppavano instabilità genomica: apparivano piccoli corpi extra contenenti DNA detti micronuclei e aumentavano i marker di danno al DNA. Questo tipo di stress sul DNA è noto per spingere le cellule verso la senescenza anziché verso una crescita incontrollata. Importante, il ripristino di Aurora B ha contribuito a ridurre i micronuclei, collegando direttamente la perdita di CTLA-4 a una gestione difettosa dei cromosomi e al danno al DNA.
Il danno al DNA accende una rete di allarme interna
Il DNA rotto e dislocato nelle cellule private di CTLA-4 non è passato inosservato. Ha attivato DNA-PKcs, un sensore del danno al DNA, che a sua volta ha attivato la via STING, un sistema di allarme integrato che risponde al DNA estraneo all’interno delle cellule. Una volta che STING è stata attivata, ha segnalato molecole a valle, includendo TBK1 e IRF3, e ha anche potenziato un’altra via chiave per il controllo della crescita, la via AKT. Piuttosto che promuovere la crescita, questa segnalazione combinata ha infine aumentato p21, un forte freno del ciclo cellulare, rinforzando lo stato senescente. Quando gli scienziati hanno bloccato DNA-PKcs, l’attivazione di STING e le caratteristiche della senescenza sono state notevolmente ridotte, dimostrando che DNA-PKcs si trova al centro di questa catena di allarme.
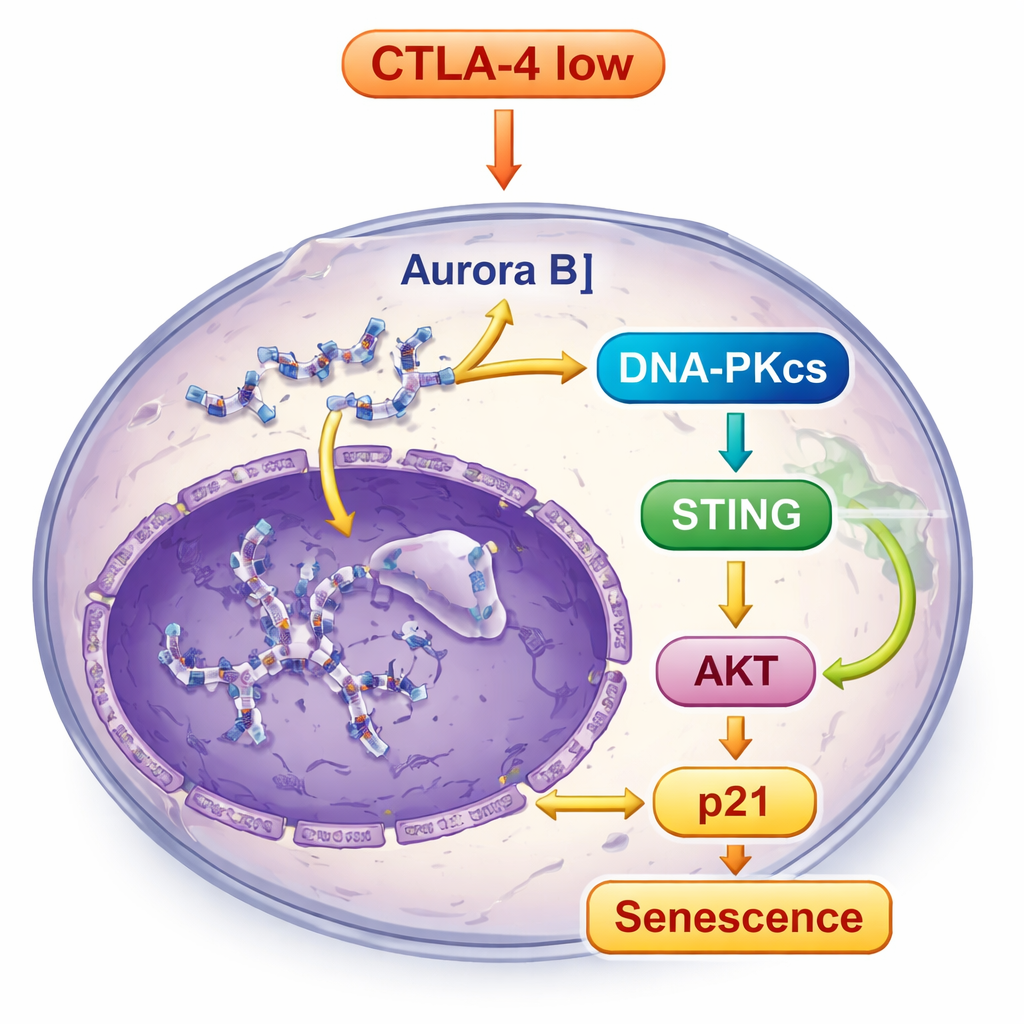
Dalla coltura cellulare ai tumori negli animali viventi
Le colture in laboratorio raccontano solo una parte della storia, quindi i ricercatori hanno verificato se la perdita di CTLA-4 avrebbe influenzato tumori reali nei topi. Hanno impiantato cellule di melanoma con o senza CTLA-4 su lati opposti degli stessi animali. I tumori privi di CTLA-4 crescevano più lentamente, pesavano meno ed erano di volume inferiore rispetto ai loro corrispettivi contenenti CTLA-4. Questi tumori deficienti in CTLA-4 mostravano inoltre una colorazione di senescenza più intensa e livelli più elevati di danno al DNA e attivazione della via STING. L’analisi di dati clinici di pazienti provenienti da grandi banche dati pubbliche ha ulteriormente supportato il collegamento: in diversi tipi di cancro, l’espressione di CTLA-4 tendeva a essere inversamente correlata con DNA-PKcs e altri componenti della riparazione del DNA, riecheggiando i risultati di laboratorio nella malattia umana.
Cosa significa per i futuri trattamenti del cancro
Nel complesso, lo studio mostra che CTLA-4 all’interno delle cellule tumorali le aiuta a mantenere la stabilità genetica e a continuare a dividersi. Quando CTLA-4 viene rimosso, i cromosomi diventano instabili, si accumulano rotture del DNA e una via di allarme interna—centrata su DNA-PKcs e STING—spinge le cellule a un arresto permanente della crescita. Per un lettore non specialista, questo significa che spegnere CTLA-4 nelle cellule tumorali spinge i tumori lontano da un comportamento pericoloso e a rapida crescita verso uno stato più sicuro di “pensione”. Queste intuizioni suggeriscono che le terapie future contro il cancro potrebbero essere progettate non solo per liberare il sistema immunitario bloccando CTLA-4 sulle cellule immunitarie, ma anche per disarmare direttamente i tumori colpendo CTLA-4 all’interno delle cellule tumorali e sfruttando la senescenza come un freno intrinseco alla crescita tumorale.
Citazione: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Parole chiave: senescenza cellulare, melanoma, CTLA-4, danno al DNA, via STING