Clear Sky Science · it
Mantenimento aberrante del fattore di trascrizione dello sviluppo PAX6 promuove la morte neuronale tramite la segnalazione JNK3
Perché questa ricerca è importante per la visione
Il glaucoma è una delle principali cause di cecità permanente, in gran parte perché le cellule nervose che trasmettono le informazioni visive dall’occhio al cervello muoiono lentamente. Molti trattamenti abbassano la pressione intraoculare, ma le persone possono comunque perdere la vista anche quando la pressione è ben controllata. Questo studio pone una domanda più profonda: cosa induce queste cellule gangliari retiniche a scegliere la morte quando sono sotto stress, e possiamo spegnere quella decisione a livello del controllo genico all’interno del nucleo cellulare?
Una retina stressata sotto attacco
Al centro del glaucoma e di malattie oculari correlate vi è la perdita lenta delle cellule gangliari retiniche (RGC), i neuroni di output dell’occhio. Queste cellule sono vulnerabili a molti tipi di stress, compresi livelli tossici del neurotrasmettitore glutammato, che sovraattiva i recettori NMDA e scatena un dannoso sovraccarico di calcio. I ricercatori hanno utilizzato un modello murino ben consolidato in cui una piccola quantità di NMDA viene iniettata nell’occhio, danneggiando selettivamente le RGC mentre gli altri strati retinici restano in gran parte intatti. Hanno confermato che questo trattamento non modificava la pressione intraoculare, ma provocava segni tipici di morte cellulare programmata nelle RGC, come il rilascio di citocromo c dai mitocondri e la comparsa di nuclei TUNEL-positivi.
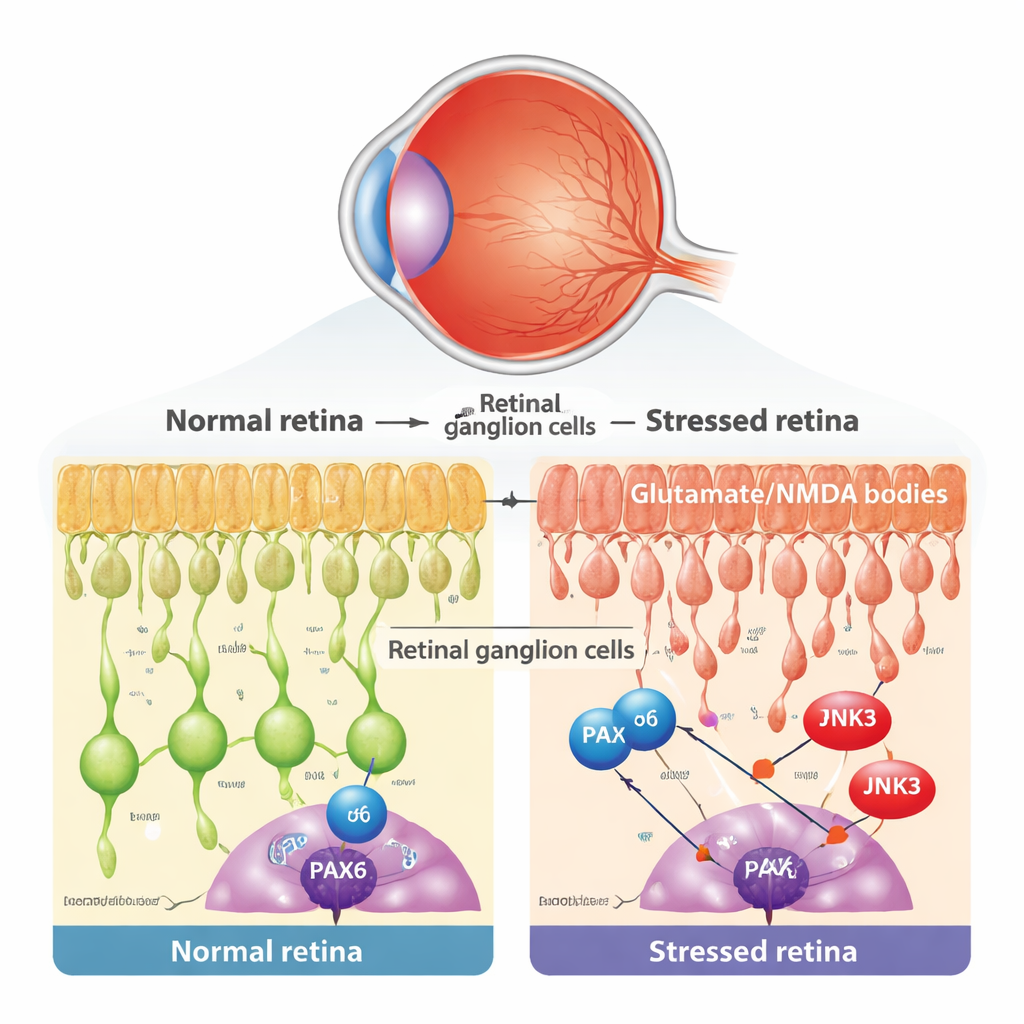
Un gene dello sviluppo che rifiuta di andare in pensione
Durante lo sviluppo precoce, un regolatore genico chiamato PAX6 agisce come un architetto maestro dell’occhio, guidando la nascita e il wiring delle diverse cellule retiniche. La saggezza convenzionale dice che tali programmi di sviluppo si spengono in gran parte nell’età adulta. Rianalizzando dati di RNA sequencing a singola cellula provenienti da retine di topo e umane, il gruppo ha scoperto che PAX6 è in realtà mantenuto in modo forte e selettivo nelle RGC mature e in certi interneuroni. Mediante colorazioni microscopiche, hanno mostrato che nello strato dove risiedono le RGC, PAX6 è prevalentemente presente nelle cellule gangliari piuttosto che nelle vicine cellule amacrine. Ciò ha sollevato una possibilità intrigante: nella malattia adulta, un vecchio programma di sviluppo potrebbe essere riutilizzato e trasformarsi in un motore di degenerazione.
Da guardiano a carnefice: PAX6 cambia ruolo
Per verificare se PAX6 aiuta le RGC a sopravvivere o a morire sotto stress, gli scienziati hanno utilizzato un approccio simile alla terapia genica. Hanno somministrato un vettore virale contenente un piccolo RNA che silenzia specificamente PAX6 nella retina, quindi hanno esposto gli occhi all’NMDA. Rispetto agli occhi trattati di controllo, le retine con deplezione di PAX6 presentavano molte meno RGC apoptotiche e molto meno danno mitocondriale, indicando che PAX6 è necessario per la piena manifestazione della morte cellulare in questo modello. L’RNA sequencing su scala genomica ha rivelato che molti geni pro-morte, in particolare quelli coinvolti nel danno mitocondriale e nell’attivazione delle caspasi, venivano fortemente indotti dall’NMDA nei topi normali ma risultavano attenuati quando PAX6 era silenziato. In altre parole, PAX6 contribuisce ad attivare una rete di geni che spingono le RGC oltre il limite.
La chinasi dello stress che inverte l’interruttore PAX6
Come fa lo stress ad attivare PAX6 senza aumentare la sua quantità? Il gruppo si è concentrato su JNK3, un enzima sensibile allo stress presente soprattutto nei neuroni. In condizioni di danno da NMDA, JNK3 si spostava nel nucleo delle RGC e si associava fisicamente a PAX6. Esperimenti biochimici “in provetta” con proteine purificate hanno dimostrato che JNK3 può aggiungere direttamente gruppi fosfato a PAX6, e questa reazione veniva bloccata da un inibitore di JNK. Nei topi privi del gene Jnk3, l’NMDA non produceva più lo stesso pattern di fosforilazione di PAX6. Mappature della cromatina (ChIP-seq) e saggi mirati di legame al DNA hanno rivelato che, sotto stress, il PAX6 fosforilato, insieme a JNK3, si lega più fortemente alle regioni regolatorie di geni pro-apoptotici chiave come Bax e Gadd45a, potenziandone l’attività. Quando PAX6 veniva silenziato o JNK3 rimosso geneticamente, questo legame e l’attivazione dei geni pro-morte corrispondenti risultavano fortemente ridotti.
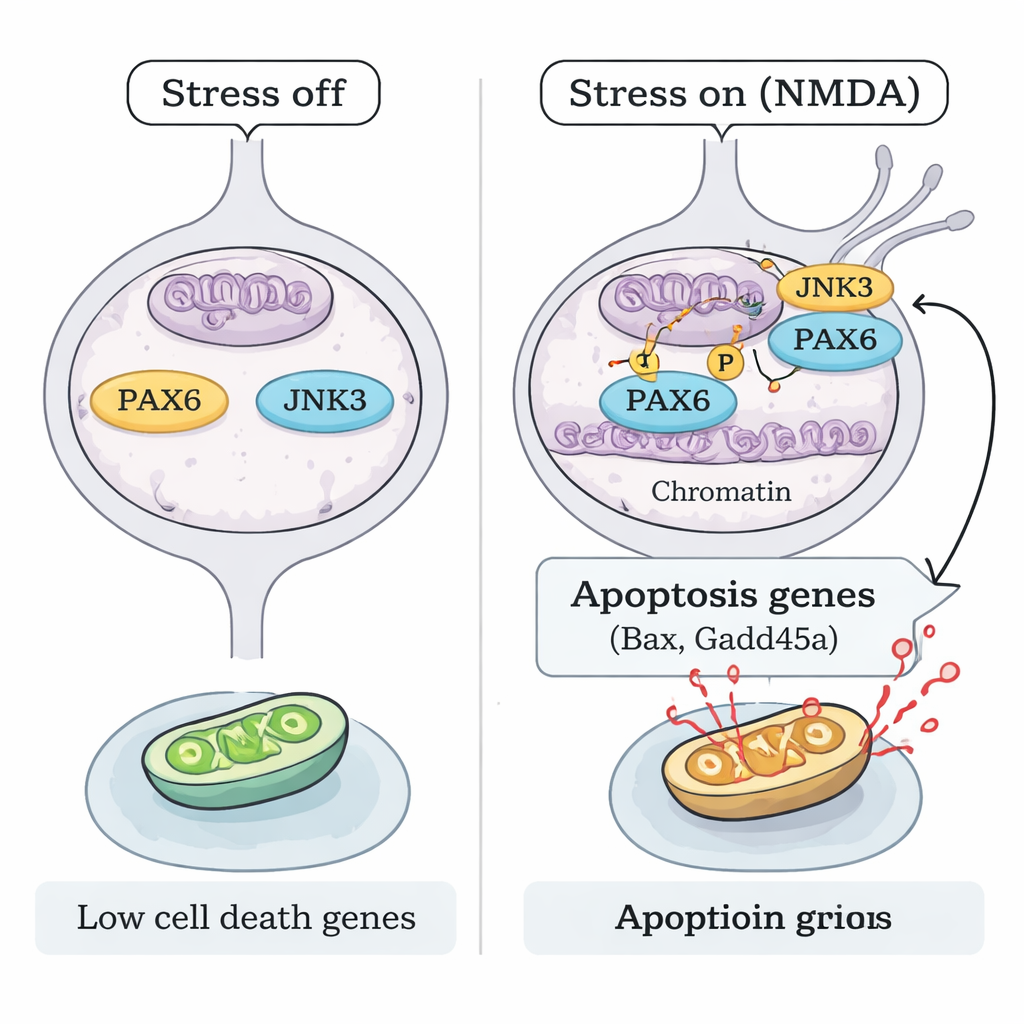
Spegnere il programma di morte per proteggere la vista
Infine, i ricercatori si sono chiesti se bloccare questo asse JNK3–PAX6 sia sufficiente a proteggere le cellule critiche per la visione. Sia nei topi con silenziamento di PAX6 sia nei topi privi di JNK3, le RGC risultarono significativamente preservate dopo l’esposizione a NMDA, con meno cellule morenti e una struttura retinica più sana. Questo porta a un modello meccanicistico chiaro: sotto stress eccitotossico, JNK3 fosforila il PAX6 persistentemente espresso, convertendolo da costruttore dello sviluppo in un potente attivatore di un programma genico di morte cellulare nelle RGC adulte. Interrompere quel legame—silenziando PAX6 o disabilitando JNK3—mantiene vive molte di queste cellule neuronali. Per i pazienti, questo lavoro suggerisce che future terapie per il glaucoma potrebbero andare oltre l’abbassamento della pressione intraoculare e mirare direttamente agli interruttori genetici che decidono se i neuroni retinici vivono o muoiono.
Citazione: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Parole chiave: glaucoma, cellule gangliari retiniche, PAX6, JNK3, neurodegenerazione