Clear Sky Science · it
Sec8: un nuovo regolatore positivo di RIG-I nella difesa anti‑virus a RNA
Come le nostre cellule riconoscono i virus furtivi
Molti virus pericolosi, inclusi l'influenza e virus animali emergenti, trasportano il loro materiale genetico sotto forma di RNA. Le nostre cellule si affidano a sistemi d'allarme interni per individuare rapidamente questi invasori e avviare una risposta antivirale. Questo studio esplora una proteina cellulare poco conosciuta chiamata Sec8 e mostra che essa svolge discretamente un ruolo centrale nel mantenere uno dei nostri sensori virali chiave, RIG‑I, vivo e attivo abbastanza a lungo da proteggerci.
Un allarme cellulare sotto minaccia
RIG‑I è un “allarme antifurto” molecolare che perlustra l'interno delle cellule alla ricerca di frammenti di RNA virale. Quando rileva RNA sospetto, cambia conformazione, si attiva e invia segnali che in ultima istanza scatenano gli interferoni di tipo I—molecole d'avvertimento potenti che aiutano le cellule vicine a resistere all'infezione e attivano le difese immunitarie. Poiché un allarme iperattivo può provocare infiammazione dannosa o malattie autoimmuni, le cellule regolano strettamente i livelli di RIG‑I. Diverse altre proteine possono etichettare RIG‑I per la distruzione attaccando piccole catene di ubiquitina, indirizzandolo al “tritacarne” cellulare chiamato proteasoma. Fino a oggi non era chiaro quali fattori cellulari aggiuntivi proteggessero RIG‑I dall'essere distrutto prematuramente, specialmente durante un'infezione attiva da virus a RNA.
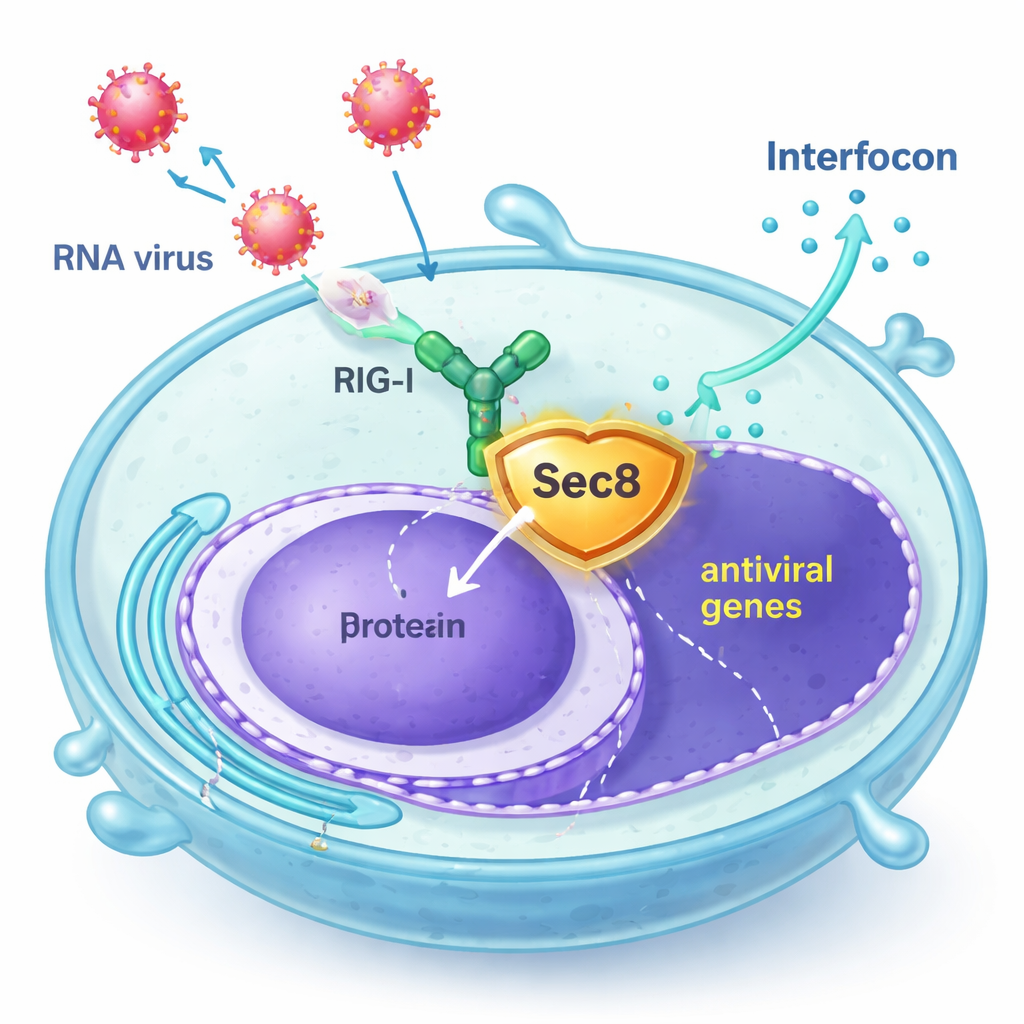
Sec8 interviene come guardia del corpo
Gli autori hanno scoperto che Sec8, noto soprattutto come parte di un complesso di otto proteine che aiuta le vescicole secretorie a fondersi con la superficie cellulare, in realtà potenzia la segnalazione antivirale. In linee cellulari umane e in cellule immunitarie primarie di topo, l'aumento dei livelli di Sec8 ha portato a una maggiore attivazione dei geni correlati agli interferoni dopo infezione con virus a RNA come il virus della stomatite vescicolare (VSV) e il virus di Sendai, o dopo esposizione a RNA virale sintetico. Al contrario, la riduzione di Sec8 ha diminuito la produzione di interferone e dei geni stimolati dall'interferone, lasciando le cellule meno in grado di contrastare la replicazione virale. Questi risultati suggeriscono che Sec8 agisca non solo nella secrezione, ma anche come regolatore positivo nella via di allarme antivirale.
Bloccare il tritacarne cellulare
Approfondendo, i ricercatori hanno rilevato che Sec8 non aumenta l'espressione genica di RIG‑I; invece, impedisce che la proteina RIG‑I venga degradata. Quando Sec8 veniva rimosso, i livelli di RIG‑I calavano più rapidamente, e questa perdita poteva essere prevenuta da farmaci che bloccano il proteasoma, coinvolgendo così la macchina di riciclaggio proteico della cellula. Il team ha identificato un'altra proteina, STUB1, come un importante “etichettatore” che attacca un tipo specifico di catena di ubiquitina (collegamento K48) a RIG‑I su un amminoacido chiamato lisina 190. Questa etichetta segnala RIG‑I per la distruzione. Sec8 interferisce con questo processo in due modi: compete fisicamente con STUB1 per il legame alla stessa regione di attivazione su RIG‑I e riduce la quantità di STUB1 che la cellula produce in primo luogo.
Sec8, p53 e il controllo dell'etichettatore
Per spiegare come Sec8 riduca la produzione di STUB1, gli autori hanno esaminato la regolazione genica. Hanno individuato un breve tratto di DNA che funge da nucleo attivante (promotore) del gene STUB1 e hanno mostrato che la famosa proteina oncosoppressore p53 si lega a questa regione e aumenta i livelli di STUB1. Sec8 attenua sia la quantità sia la fosforilazione attivante di p53, perciò p53 non può più promuovere efficacemente la produzione di STUB1. Quando p53 è stato bloccato o STUB1 è stato silenziato, gli effetti dannosi della perdita di Sec8 sulla produzione di interferone e sulla crescita virale sono stati in gran parte invertiti. Questo colloca Sec8 in cima a una catena regolatoria che va da p53 a STUB1 e infine alla stabilità di RIG‑I.
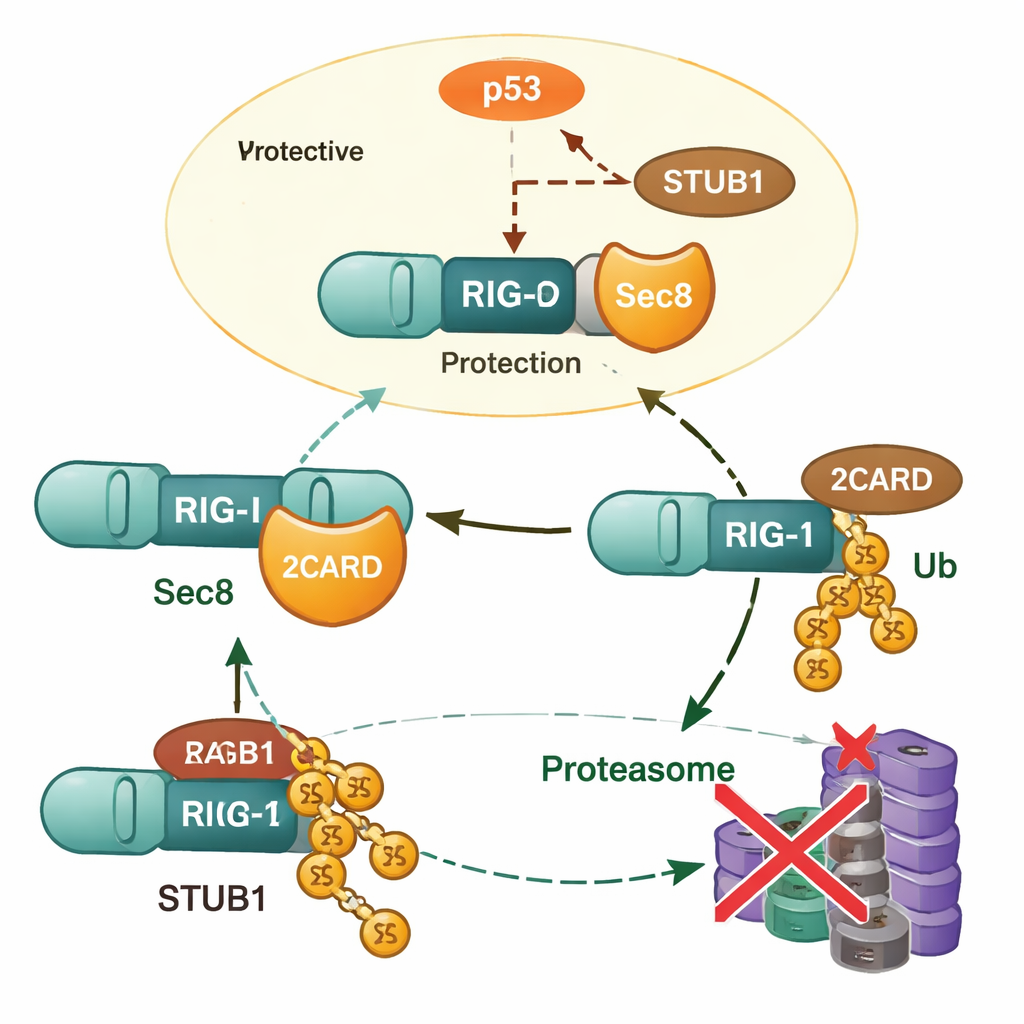
Dalla piastra di Petri agli organismi viventi
Il gruppo ha quindi testato l'importanza di Sec8 in topi ingegnerizzati per essere privi del gene Sec8 specificamente in alcune cellule immunitarie. Dopo infezione con VSV, questi animali hanno prodotto meno interferone, presentato quantità maggiori di virus in organi come milza, fegato e polmoni, e mostrato danni polmonari più gravi, maggiore perdita di peso e sopravvivenza ridotta rispetto ai topi di controllo. Questi risultati in vivo hanno confermato che Sec8 non è un attore minore ma un protettore significativo contro le infezioni da virus a RNA in un organismo intero.
Perché questo è importante per terapie future
In termini semplici, questo studio dimostra che Sec8 agisce come una guardia del corpo per il sensore antivirale RIG‑I. Mantenendo sotto controllo la proteina “etichettatrice” STUB1 e proteggendo direttamente RIG‑I dall'essere inviato al tritacarne cellulare, Sec8 consente alle cellule di montare una risposta interferonica tempestiva e di controllare meglio i virus a RNA. Comprendere questo asse p53–STUB1–RIG‑I descritto di recente apre la strada a future strategie antivirali che stabilizzino RIG‑I o imitino le azioni protettive di Sec8, potenzialmente rafforzando le nostre difese contro un'ampia gamma di infezioni virali a base di RNA.
Citazione: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Parole chiave: immunità innata, virus a RNA, RIG-I, ubiquitinazione, segnalazione dell'interferone