Clear Sky Science · it
La trasmissione del lattato da cellule tumorali ipossiche promuove la senescenza dei macrofagi e la polarizzazione M2 tramite l’asse DNMT1‑NHE7 accelerando la progressione del cancro endometriale
Perché privare i tumori di ossigeno conta
Il cancro endometriale, che origina dal rivestimento dell’utero, sta diventando più comune in tutto il mondo. Molti tumori avanzati sono difficili da trattare perché recidivano, si diffondono o resistono alle terapie standard. Questo studio esamina cosa accade all’interno di questi tumori quando restano a corto di ossigeno — una caratteristica comune dei tumori a rapida crescita — e mostra come un semplice prodotto di scarto, il lattato, possa riprogrammare le cellule immunitarie vicine per favorire la crescita tumorale invece di combatterla.
Bassa ossigenazione: i tumori diventano fabbriche di lattato
Man mano che le cellule del cancro endometriale si moltiplicano, l’apporto di sangue non riesce a soddisfare la richiesta, creando aree a basso contenuto di ossigeno, o ipossia. Le cellule reagiscono accendendo un regolatore principale chiamato HIF1A che riorganizza il loro metabolismo energetico. Invece di fare affidamento principalmente su processi energetici efficienti, le cellule aumentano la glicolisi, un processo rapido ma dispendioso che produce grandi quantità di lattato. I ricercatori hanno analizzato i dati tumorali di centinaia di pazienti e hanno rilevato che livelli più alti di HIF1A erano associati a una maggiore attività di molti geni legati alla glicolisi e di trasportatori che espellono il lattato dalle cellule tumorali. I pazienti i cui tumori mostravano più HIF1A tendevano ad avere un esito peggiore, suggerendo che questo cambiamento metabolico è strettamente legato a una malattia più aggressiva.
Come i rifiuti tumorali rimodellano cellule immunitarie “utili”
I macrofagi sono cellule immunitarie che possono attaccare i tumori o sostenerli, a seconda del loro stato. In questo lavoro, il gruppo ha dimostrato che sotto ipossia le cellule del cancro endometriale rilasciano molto più lattato nell’ambiente circostante. Questo lattato viene esportato tramite un trasportatore chiamato MCT3 sulle cellule tumorali e poi importato nei macrofagi attraverso un altro trasportatore, MCT1. Una volta all’interno, il lattato spinge i macrofagi lontano da una modalità difensiva verso il cosiddetto stato M2, associato alla riparazione tissutale, alla soppressione dell’infiammazione e, sfortunatamente, al sostegno della crescita tumorale. In esperimenti di laboratorio, i macrofagi esposti a fluidi tumorali ricchi di lattato mostravano più marcatori del tipo M2, e il fluido che secernevano a sua volta favoriva la crescita, la motilità e l’invasività delle cellule tumorali. 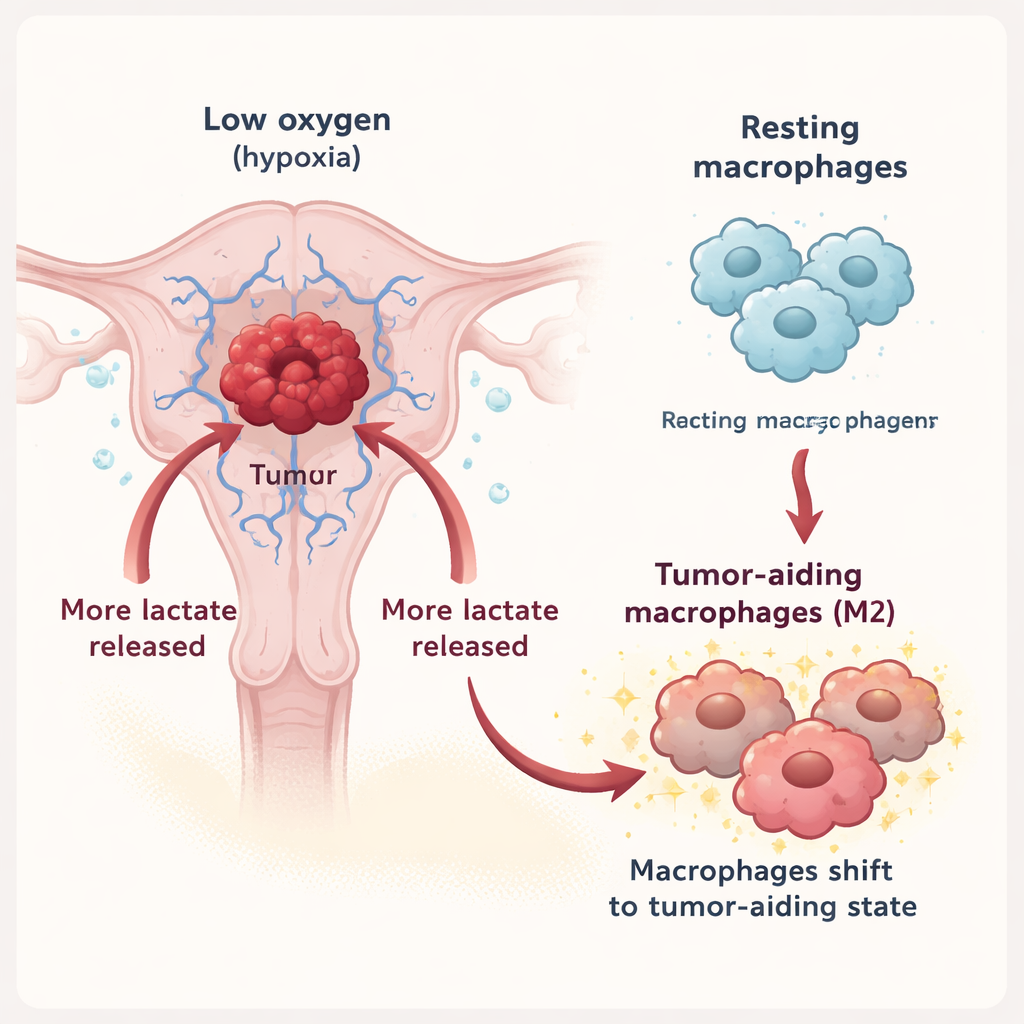
Un interruttore epigenetico che silenzia una “valvola del pH” cellulare
Lo studio prosegue rivelando l’interruttore molecolare all’interno dei macrofagi che collega il lattato derivato dal tumore a questo comportamento dannoso. Il lattato non si limita a circolare; può modificare le proteine istoniche nel nucleo — un’etichetta chimica nota come lattilazione — che influenza quali geni vengono attivati o silenziati. I ricercatori hanno scoperto che il lattato aumenta una specifica modifica istonica nella regione di controllo del gene DNMT1, elevandone l’attività. DNMT1 è un enzima che aggiunge gruppi metile al DNA e può silenziare i geni. Uno dei suoi bersagli in questo contesto è NHE7, una proteina che contribuisce a regolare l’acidità all’interno di alcuni compartimenti cellulari. Quando DNMT1 è potenziato, aumenta la metilazione del gene NHE7, riducendone l’espressione. La diminuzione di NHE7 altera l’equilibrio del pH interno e attiva una via di segnalazione nota come via MAPK. Questa via, a sua volta, spinge i macrofagi verso lo stato M2 favorevole al tumore e verso una forma di invecchiamento cellulare chiamata senescenza, che li fissa in una modalità cronica e pro‑tumorale.
Dalla reazione a catena molecolare a tumori a crescita più rapida
Per verificare se questa catena di eventi abbia rilevanza negli organismi viventi, gli scienziati hanno creato modelli murini in cui cellule di cancro endometriale umano venivano coltivate insieme a macrofagi di tipo umano. Quando è stato fornito lattato extra, i tumori sono cresciuti di più, hanno mostrato più cellule in divisione e contenevano un maggior numero di macrofagi di tipo M2 e senescenti con alto DNMT1 e basso NHE7. Sorprendentemente, quando i macrofagi sono stati ingegnerizzati per sovraesprimere NHE7, questo ha attenuato l’effetto potenziante del lattato: i tumori erano più piccoli, presentavano più cellule in morte e contenevano meno macrofagi M2 e senescenti. Bloccare l’enzima DNMT1 o la via MAPK ha anche indebolito la capacità del lattato di riprogrammare i macrofagi, rafforzando l’idea che queste molecole formino un asse connesso. 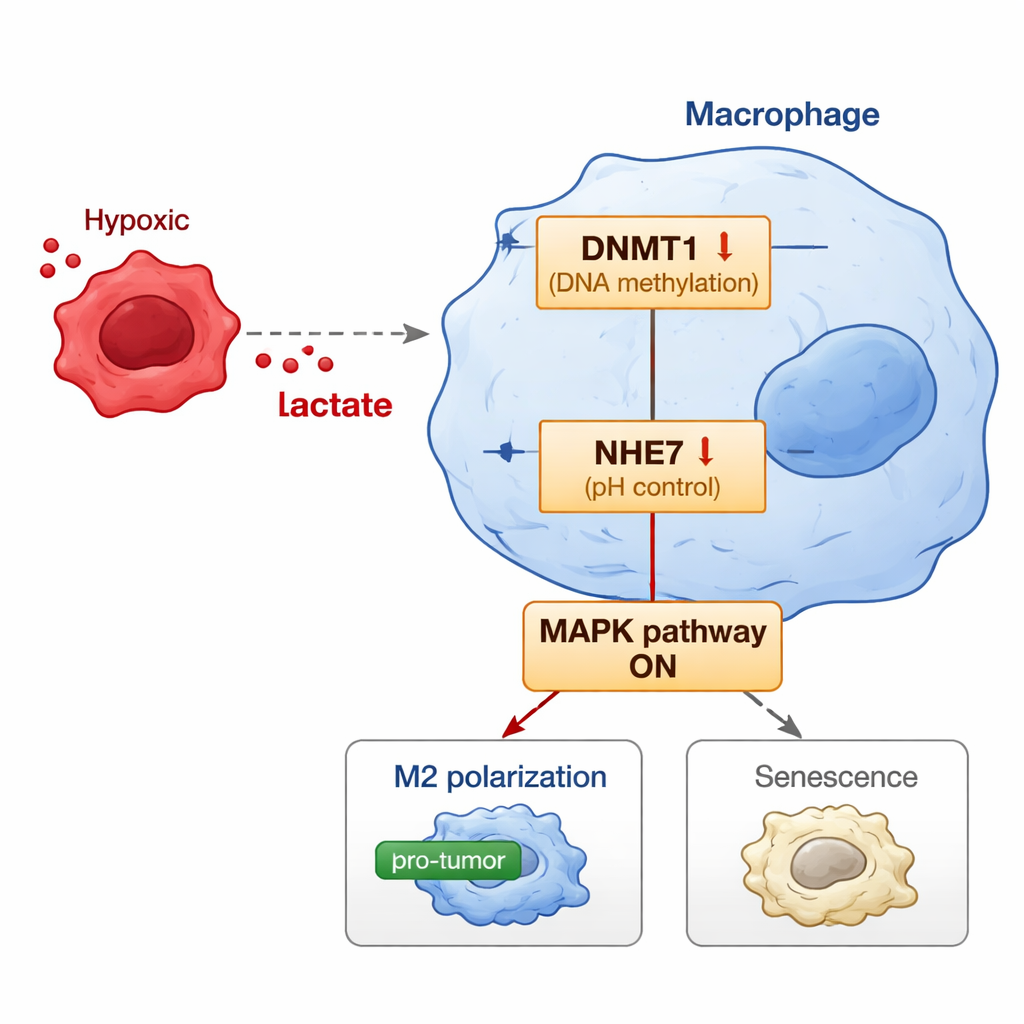
Trasformare gli stratagemmi del tumore in bersagli terapeutici
Per i non specialisti, il messaggio chiave è che i tumori endometriali possono sfruttare la bassa ossigenazione e il lattato — un tempo considerati meri residui cellulari — per “lavare il cervello” delle cellule immunitarie vicine e farle diventare alleate del tumore. Lo fanno attraverso una staffetta epigenetica: il lattato potenzia DNMT1, che silenzia NHE7, il quale a sua volta attiva segnali che bloccano i macrofagi in uno stato invecchiato e favorevole al tumore. Interferendo con qualunque passaggio di questa catena lattato–DNMT1–NHE7–MAPK, potrebbe essere possibile ripristinare una risposta immunitaria più anti‑tumorale e rallentare la crescita del cancro. Questo lavoro indica possibili terapie future che non mirano solo alle cellule tumorali direttamente, ma che re‑educano anche le cellule immunitarie circostanti che il tumore ha messo dalla sua parte.
Citazione: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Parole chiave: cancro endometriale, microambiente tumorale, metabolismo del lattato, polarizzazione dei macrofagi, regolazione epigenetica