Clear Sky Science · it
Oltre il metabolismo: esplorare le implicazioni regolatorie e terapeutiche del lattato e della lattilazione nella morte cellulare regolata nei tumori
Perché un “rifiuto” dello zucchero è importante per il cancro
Per decenni il lattato — la sostanza che fa bruciare i muscoli sovraccarichi — è stato considerato un rifiuto cellulare. Questa recensione mostra che nel cancro il lattato è tutt’altro che scarto. Agisce come carburante, come segnale chimico e persino come interruttore che può decidere se le cellule tumorali vivono o muoiono. Comprendere questo ruolo nascosto potrebbe aprire nuove strade per indurre le cellule cancerose ad autodistruggersi risparmiando i tessuti sani.
La scorciatoia zuccherina che riscrive le cellule tumorali
Le cellule tumorali sono note per la loro “voglia di dolce”. Anche quando l’ossigeno è abbondante, preferiscono degradare rapidamente il glucosio in lattato invece di ossidarlo completamente nei mitocondri, uno spostamento noto come effetto Warburg. Questa strategia permette ai tumori di generare energia e mattoni biologici ad alta velocità. Il conseguente flusso di lattato viene espulso tramite trasportatori speciali, modellando un microambiente tumorale acido e ricco di nutrienti che sostiene la crescita e aiuta i tumori ad adattarsi a stress come la carenza di ossigeno o la chemioterapia.
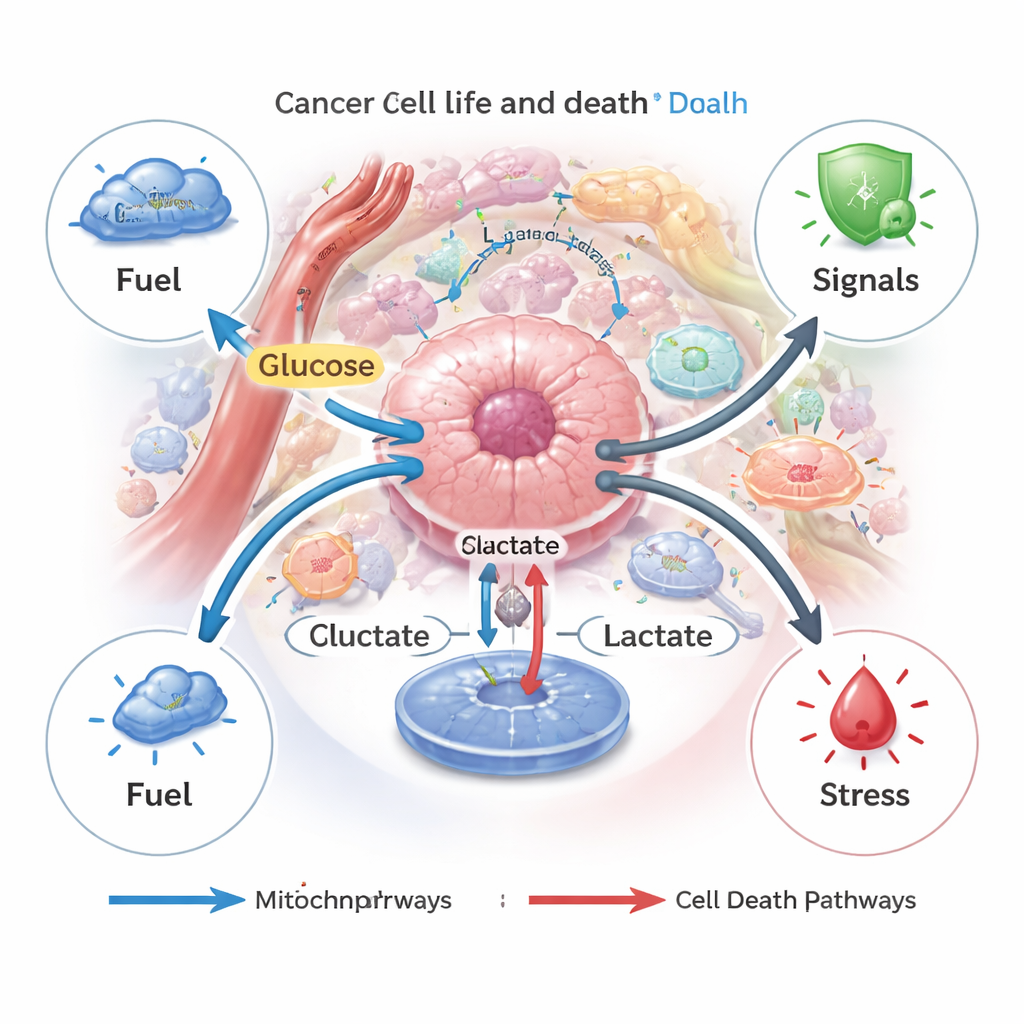
Il lattato come regolatore di diversi tipi di morte cellulare
La morte cellulare nei nostri tessuti è in genere strettamente controllata, contribuendo a rimuovere cellule danneggiate o pericolose. Le cellule tumorali spesso sfuggono a questi programmi. Gli autori descrivono come il lattato possa sia bloccare sia indurre diverse vie di morte regolata — apoptosi ("suicidio" cellulare), autofagia (autodigestione), ferroptosi (danno delle membrane mediato dal ferro), piroptosi (esplosione infiammatoria) e cuproptosi (collasso indotto dal rame). Quando le cellule cancerose producono o importano quantità moderate di lattato, tendono a usarlo come carburante e segnale di sopravvivenza, attivando percorsi che le proteggono da chemioterapia, carenza di nutrienti o farmaci mirati. Ma quando il lattato si accumula all’interno delle cellule, per esempio se la sua esportazione è bloccata, lo stress acido risultante e il danno mitocondriale possono girare l’interruttore e spingere le cellule verso apoptosi o ferroptosi.
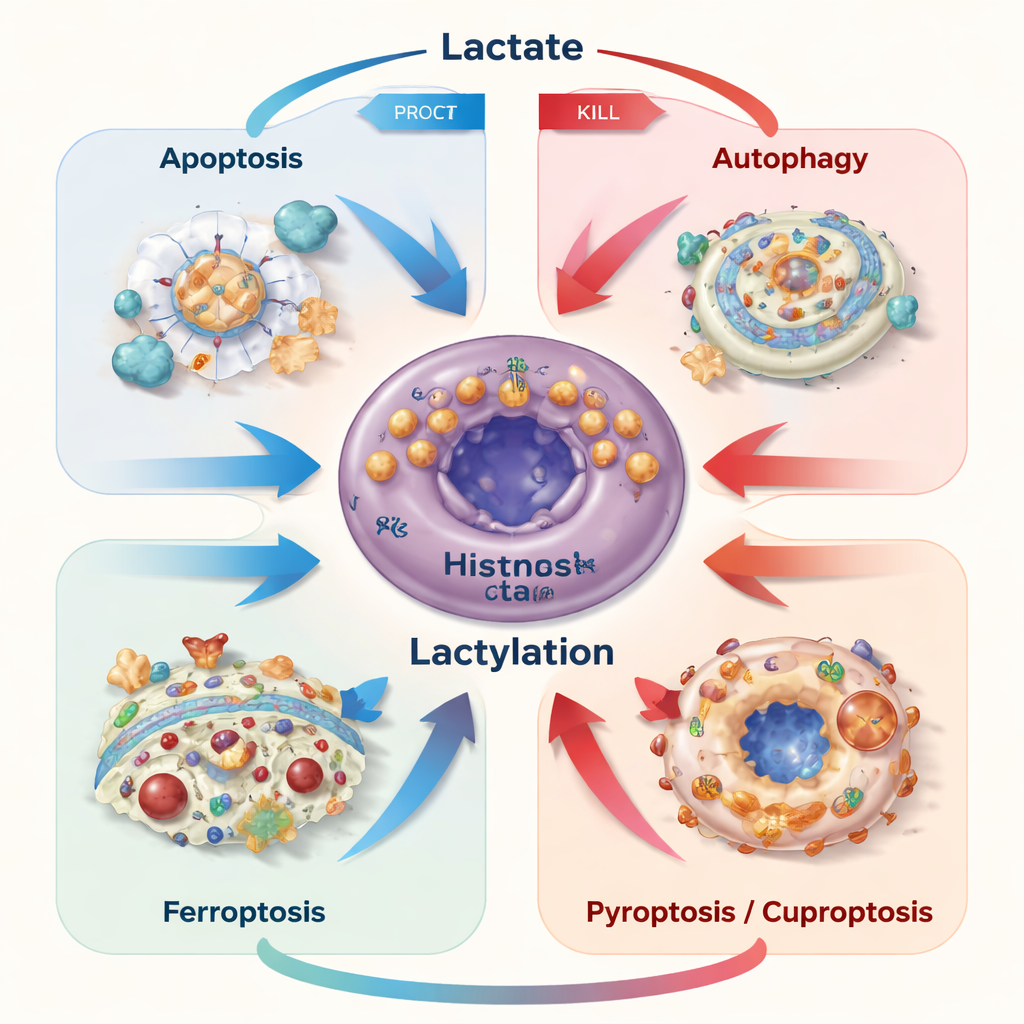
Lattilazione: quando il lattato scrive sulle proteine
Una scoperta recente sorprendente è che il lattato può essere convertito in un piccolo tag chimico e attaccato ai residui di lisina delle proteine, una modificazione nota come lattilazione. Enzimi fungono da “scrittori” e “cancellatori” di questi tag, decorando sia gli istoni associati al DNA sia molte altre proteine. Questi marchi cambiano quali geni vengono attivati, come si comportano gli enzimi e quanto sono stabili i regolatori chiave. Nel cancro, la lattilazione affina l’equilibrio tra sopravvivenza e autodistruzione. Può, per esempio, aumentare proteine che bloccano l’apoptosi, potenziare il riciclo tramite autofagia, proteggere le cellule dalla ferroptosi stringendo il controllo del ferro e incrementando gli antiossidanti, o alterare nuove forme di morte come la cuproptosi cambiando il modo in cui le cellule gestiscono proteine sensibili al rame.
Una conversazione a doppio senso tra metabolismo e programmi di morte
La relazione non è unidirezionale: le vie di morte cellulare rimodellano anche il modo in cui i tumori utilizzano lo zucchero e producono lattato. Quando i mitocondri sono danneggiati durante l’apoptosi iniziale o la mitofagia (rimozione selettiva dei mitocondri), le cellule spesso ricorrono alla glicolisi veloce, aumentando la produzione di lattato. Le cellule di supporto circostanti, come i fibroblasti associati al cancro, possono subire un riadattamento simile e diventare fabbriche di lattato che alimentano le cellule tumorali vicine. Altri tipi di morte, come la ferroptosi, tendono a sopprimere la glicolisi e quindi ad abbassare i livelli di lattato. Il risultato è un ciclo di retroazione dinamico in cui metabolismo e meccanismi di morte si aggiustano continuamente l’un l’altro mentre il tumore evolve e risponde al trattamento.
Trasformare una debolezza in una strategia terapeutica
Poiché lattato e lattilazione possono proteggere o uccidere le cellule cancerose a seconda del contesto, gli autori sostengono che le terapie non devono limitarsi a bloccare semplicemente la produzione di lattato. Invece, i trattamenti futuri potrebbero deviare selettivamente i flussi di lattato, modulare i suoi trasportatori o mirare a specifici marchi di lattilazione per spingere le cellule tumorali oltre il punto di non ritorno riattivando al contempo le cellule immunitarie antitumorali che sono attualmente paralizzate dall’ambiente acido. Sistemi intelligenti di somministrazione dei farmaci e nanomedicine che rispondono ai livelli locali di lattato o pH stanno emergendo come modi per applicare questa precisione. In termini semplici, il messaggio dell’articolo è che ciò che una volta sembrava scarto metabolico è in realtà una potente manopola di controllo sul destino delle cellule tumorali — e imparare a girare correttamente quella manopola potrebbe rendere le terapie esistenti molto più efficaci.
Citazione: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Parole chiave: lattato, lattilazione, morte delle cellule tumorali, metabolismo tumorale, ferroptosi