Clear Sky Science · it
Impronte funzionali della carenza di ricombinazione omologa nel cancro alla prostata rivelate dalla frammentazione del ctDNA e dall’accessibilità dei fattori di trascrizione
Perché è importante per i pazienti oncologici
Molti uomini con cancro alla prostata avanzato potrebbero beneficiare di farmaci che sfruttano le vulnerabilità nei meccanismi di riparazione del DNA dei loro tumori. Tuttavia oggi i medici spesso non riescono a identificare chi risponderà, perché i test richiedono solitamente biopsie difficili e si concentrano su un numero limitato di geni. Questo studio mostra come un semplice prelievo di sangue possa essere trasformato in un quadro ricco e multilivello di queste debolezze nella riparazione del DNA, guidando potenzialmente scelte terapeutiche più precise e meno invasive.
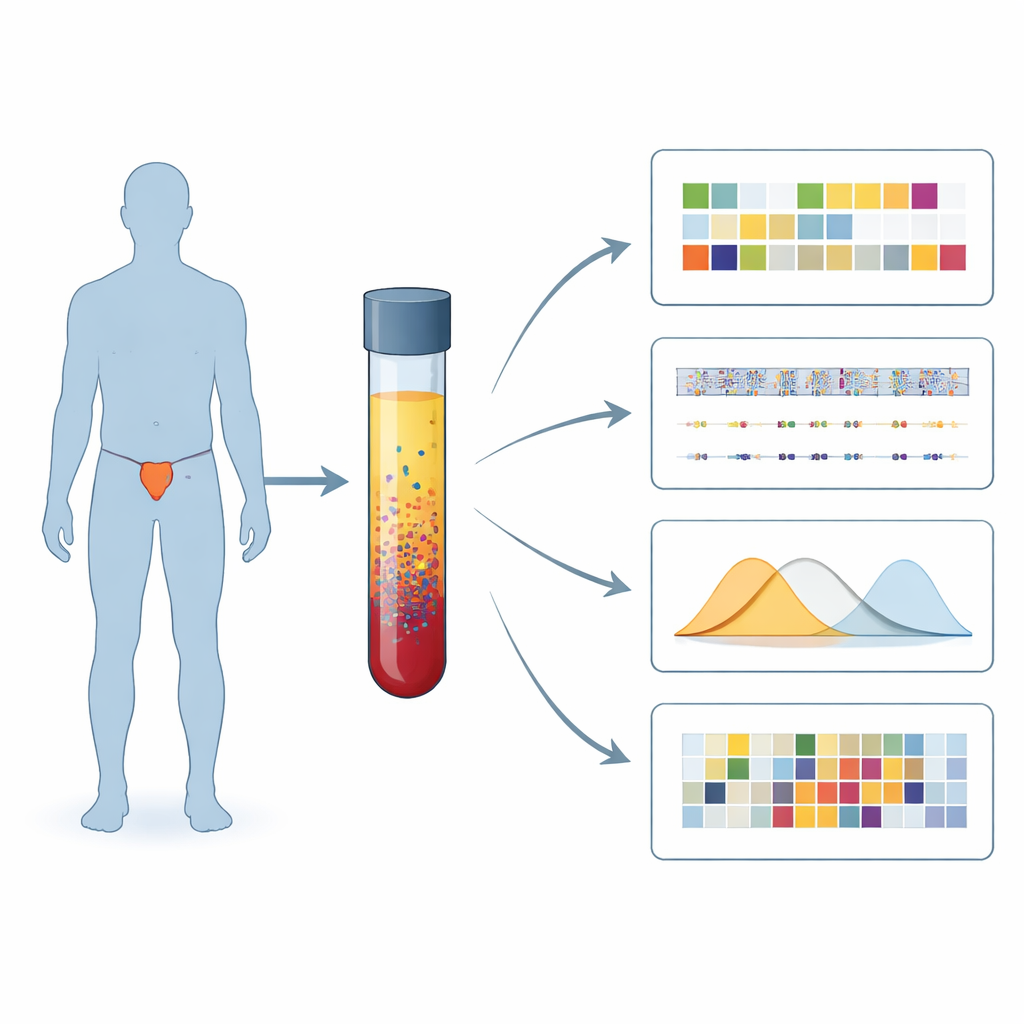
Un nuovo modo di leggere i segnali del cancro dal sangue
I ricercatori si sono concentrati su un problema di riparazione specifico chiamato carenza di ricombinazione omologa, o HRD, che rende i tumori particolarmente vulnerabili a farmaci come gli inibitori PARP e ad alcune chemioterapie. Invece di fare affidamento su campioni tumorali prelevati da ossa o prostata, hanno analizzato frammenti di DNA tumorale presenti nel flusso sanguigno, noti come DNA tumorale circolante. Da 375 uomini con carcinoma prostatico metastatico hanno selezionato 106 i cui campioni di sangue contenevano sufficiente DNA tumorale per uno studio approfondito e hanno quindi applicato diversi test complementari sugli stessi campioni di plasma.
Oltre le singole mutazioni geniche
In primo luogo, hanno sequenziato un pannello di geni chiave per la riparazione del DNA, inclusi noti protagonisti come BRCA2, BRCA1 e PALB2, insieme ad altri geni che determinano quanto aggressivi diventino i tumori prostatici. BRCA2 è emerso come il gene di riparazione più frequentemente alterato e spesso compariva insieme alla perdita di altre salvaguardie importanti come PTEN e RB1. Ma il team ha anche esaminato cambiamenti su larga scala nella struttura dei cromosomi a livello dell’intero genoma, usando il sequenziamento dell’intero genoma a bassa profondità per calcolare un punteggio di instabilità genomica. I tumori con geni BRCA danneggiati, o con punteggi elevati, mostravano genomi fortemente riorganizzati e risultavano associati a una sopravvivenza complessiva peggiore, sottolineando che grandi cambiamenti strutturali possono essere altrettanto informativi quanto mutazioni specifiche.
Impronte della mancata riparazione nei pattern mutazionali
In un sottoinsieme di pazienti, gli scienziati hanno approfondito ulteriormente sequenziando tutte le regioni codificanti per le proteine per leggere il dettaglio dei pattern di mutazioni accumulate nel tempo. Alcune combinazioni di sostituzioni di basi e piccole inserzioni o delezioni si comportano come impronte digitali dei processi che le hanno generate. Hanno riscontrato che le classiche firme associate a HRD, come quella chiamata SBS3 e un pattern di indel noto come ID6, erano arricchite nei tumori con difetti nei geni di riparazione e con alta instabilità genomica. Altre firme indicavano problemi separati, come il malfunzionamento della riparazione degli mismatches o un sottotipo distinto guidato da CDK12, mettendo in evidenza che differenti guasti nei meccanismi di riparazione del DNA lasciano cicatrici riconoscibili nel genoma.
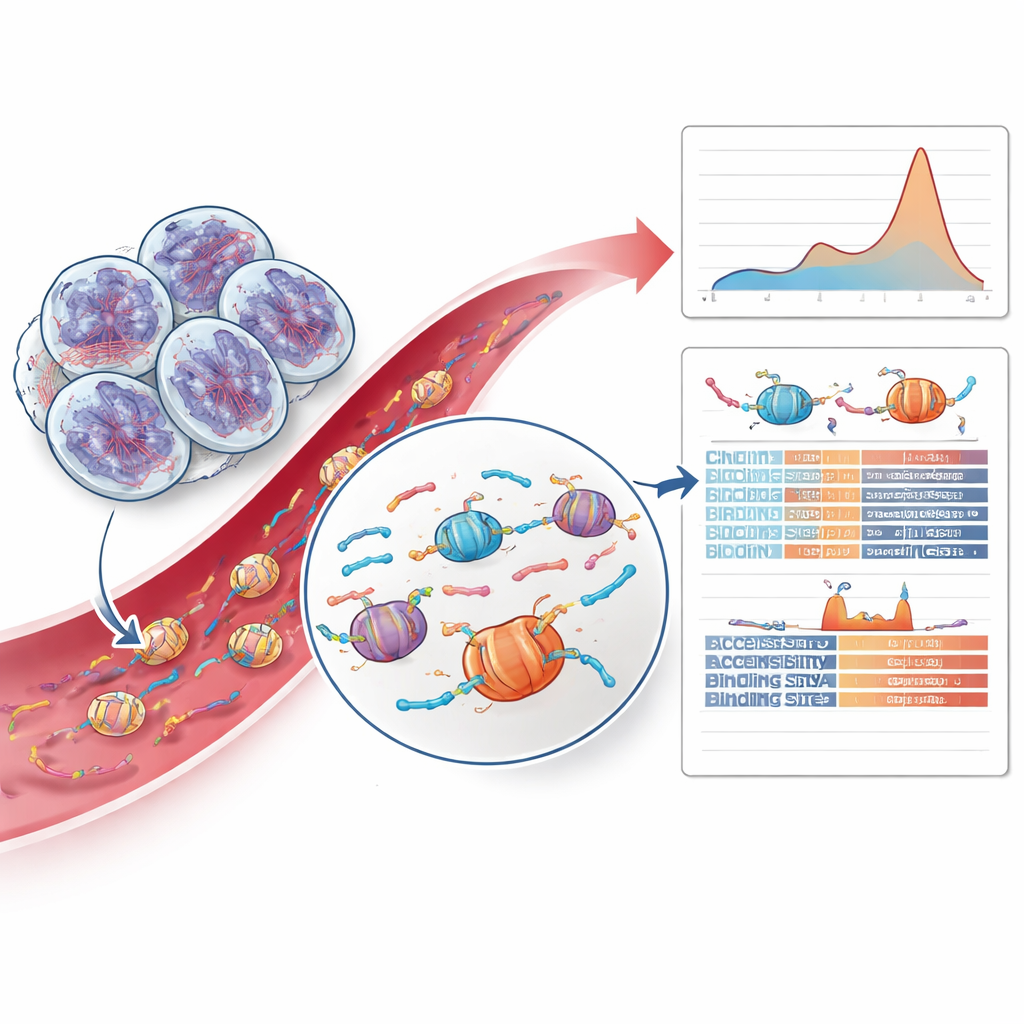
Decodificare i pattern dei frammenti di DNA e gli indizi sulla cromatina
La parte più innovativa del lavoro è andata oltre le mutazioni e ha esaminato come i frammenti di DNA tumorale vengano tagliati. Quando le cellule muoiono, il loro DNA viene tagliato intorno a pacchetti proteici chiamati nucleosomi, creando frammenti con lunghezze e pattern terminali caratteristici. Il team ha scoperto che i tumori con HRD mostravano un eccesso relativo di frammenti leggermente più lunghi corrispondenti a due nucleosomi, uno spostamento non osservato in altri tumori prostatici o nei controlli sani. Addestrando un modello di machine learning prudente sulle lunghezze dei frammenti e sulle caratteristiche delle estremità, sono riusciti a identificare i casi HRD positivi dal sangue con un’accuratezza promettente. Hanno anche esplorato quanto siano accessibili diverse regioni del genoma intorno ai siti di legame per fattori di trascrizione — proteine che controllano l’attività genica — e hanno riscontrato che certi siti di legame per zinc finger risultavano meno accessibili nei tumori HRD, suggerendo cambiamenti più profondi, legati alla riparazione, nell’organizzazione della cromatina.
Cosa può significare per i pazienti
Insieme, questi strati di informazione — dalle mutazioni geniche specifiche e dai grandi rimescolamenti cromosomici ai sottili spostamenti nelle dimensioni dei frammenti di DNA e nell’accessibilità della cromatina — formano un quadro più completo della debolezza nella riparazione del DNA nel cancro alla prostata. Per un lettore non esperto, il messaggio chiave è che un campione di sangue analizzato con cura può rivelare non solo se un gene noto come BRCA2 è mutato, ma se un tumore si comporta come se avesse un difetto grave nella riparazione, anche quando i test abituali risultano normali. Se convalidato in gruppi di pazienti più ampi e diversi, questo approccio multimodale basato sul sangue potrebbe aiutare i medici a identificare in modo più affidabile chi è probabile che tragga beneficio dagli inibitori PARP o dai farmaci a base di platino, monitorare i cambiamenti nel tempo e, in ultima analisi, personalizzare la terapia con un test semplice e ripetibile.
Citazione: Vlachos, G., Moser, T., Lazzeri, I. et al. Functional footprints of homologous recombination deficiency in prostate cancer revealed by ctDNA fragmentation and transcription factor accessibility. Br J Cancer 134, 949–960 (2026). https://doi.org/10.1038/s41416-025-03301-0
Parole chiave: cancro alla prostata, biopsia liquida, riparazione del DNA, DNA tumorale circolante, inibitori PARP