Clear Sky Science · it
Paesaggi microambientali immunosoppressivi nel cancro gastrico con alta espressione di VISTA
Perché le difese dell’organismo a volte falliscono contro il cancro dello stomaco
I trattamenti oncologici moderni fanno sempre più affidamento sul risveglio del sistema immunitario per poter attaccare i tumori. Tuttavia, in molte persone con carcinoma gastrico avanzato questi potenti farmaci funzionano poco o perdono efficacia. Questo studio esplora una ragione importante: una molecola freno chiamata VISTA che rimodella l’ambiente locale attorno al tumore, trasformando le cellule immunitarie da combattenti in spettatori o persino in collaboratori del cancro. Comprendere questo interruttore nascosto potrebbe aprire la strada a immunoterapie più precise ed efficaci.
Un freno nascosto nel quartiere tumorale
Gli autori si sono concentrati su VISTA, una proteina presente principalmente su alcuni globuli bianchi che risiedono dentro e intorno ai tumori. VISTA funge da segnale di stop per le risposte immunitarie. Mentre altri freni come PD-1 e PD-L1 sono già bersagliati da farmaci approvati, il ruolo di VISTA nel carcinoma gastrico era poco chiaro. Per investigare, il team ha analizzato tessuti di 172 pazienti usando una colorazione multicolore avanzata per mappare molti tipi cellulari contemporaneamente. Hanno inoltre impiegato sequenziamento dell’RNA a singola cellula e trascrittomica spaziale su set più piccoli di campioni per esaminare quali cellule esprimono VISTA, cosa fanno queste cellule e dove si collocano esattamente nel paesaggio tumorale. 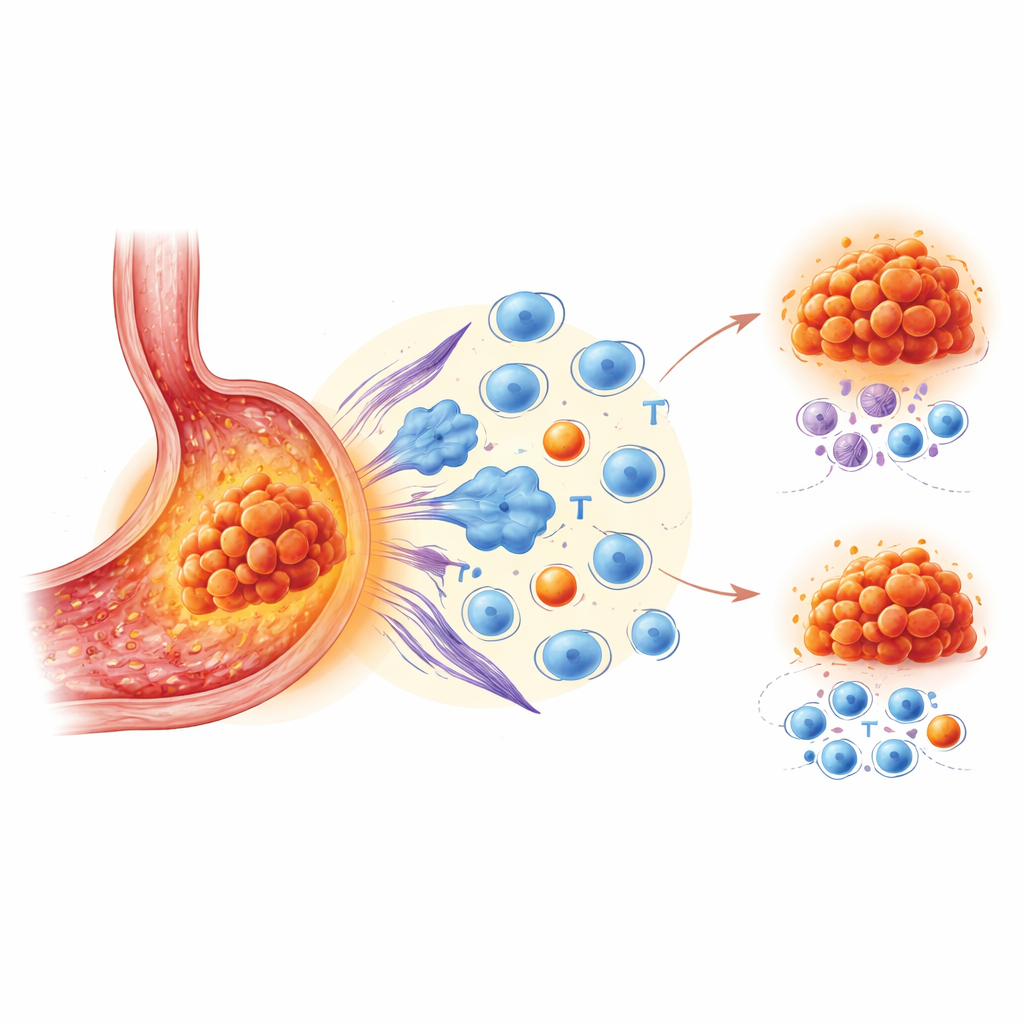
Quando VISTA è alta, il sistema immunitario è smorzato
Confrontando tumori con livelli alti rispetto a bassi di VISTA, i ricercatori hanno trovato un pattern coerente. I tumori ricchi di VISTA erano circondati da cellule immunitarie, ma non del tipo che scatenano un attacco efficace. Invece si osservava un accumulo di cellule T citotossiche esauste che avevano perso la loro efficacia, cellule T regolatorie che attenuano le risposte immunitarie, cellule di supporto che formano tessuto cicatriziale dette fibroblasti, e macrofagi orientati verso uno stato che favorisce il tumore. I pazienti i cui tessuti tumorali contenevano più VISTA hanno avuto intervalli più brevi prima del peggioramento della malattia dopo l’immunoterapia, anche tenendo conto di altri fattori clinici. In altre parole, un quartiere ricco di VISTA appariva affollato al microscopio ma funzionava come una zona “immunosilente” o soppressiva.
I macrofagi come mediatori chiave
Approfondendo, gli scienziati si sono focalizzati su monociti e macrofagi—cellule immunitarie che possono sia inghiottire il cancro sia proteggerlo. A livello di singola cellula, il gene che codifica VISTA (chiamato VSIR) risultava particolarmente attivo in diversi sottogruppi di macrofagi, in particolare in quelli che presentano efficacemente frammenti di proteine tumorali sulla loro superficie e in quelli con caratteristiche dei cosiddetti macrofagi M2, associati alla riparazione tissutale. Usando una ricostruzione computazionale della timeline di sviluppo cellulare, il team ha osservato l’accensione di VISTA mentre le cellule passavano da monociti precoci a macrofagi più maturi che si raggruppavano attorno alle cellule tumorali. La mappatura spaziale ha confermato che i macrofagi VISTA-positivi tendevano a trovarsi vicino alle cellule tumorali, e i pazienti i cui tumori contenevano più di queste cellule proprio in quelle posizioni hanno avuto esiti peggiori dopo il trattamento con inibitori dei checkpoint immunitari. 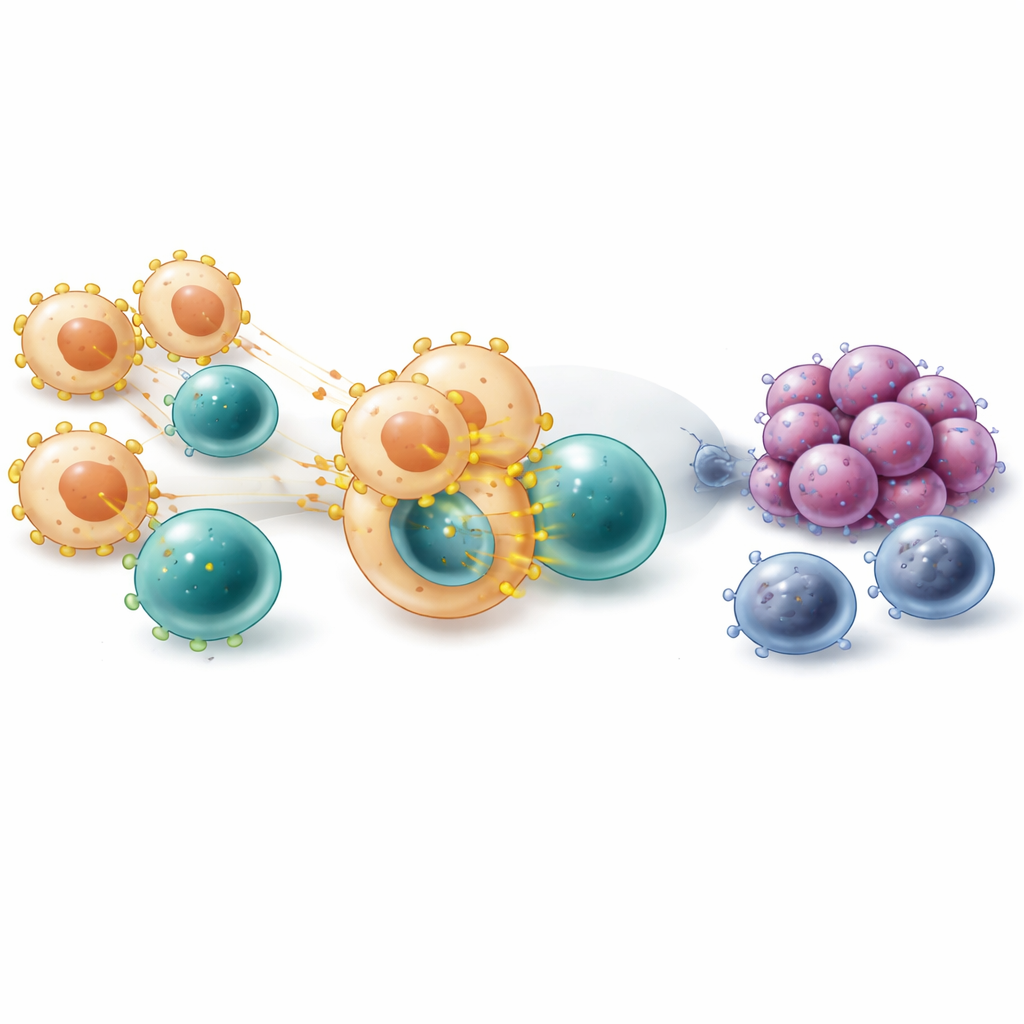
Come le cellule VISTA-positive logorano le cellule T
Lo studio ha anche esplorato come i macrofagi che esprimono VISTA comunicano con le cellule T. Mappe di comunicazione costruite dai dati di espressione genica suggeriscono che questi macrofagi interagiscono frequentemente con le cellule T tramite coppie molecolari come LGALS9 e PTPRC, e tramite molecole coinvolte nella presentazione di frammenti tumorali alle cellule T. Questa presentazione costante può, nel tempo, spingere le cellule T da uno stato attivo iniziale a uno stato di stimolazione cronica ed esaurimento, caratterizzato da molteplici segnali inibitori sulla loro superficie. Nei campioni in cui i macrofagi mostravano una maggiore espressione di VSIR, si osservavano più cellule T regolatorie e più cellule T citotossiche esauste, rafforzando l’idea che i macrofagi VISTA-positivi contribuiscano all’esaurimento immunitario piuttosto che a un attacco netto ed efficace.
Cosa potrebbe significare per i trattamenti futuri
Complessivamente, il lavoro delinea VISTA come un interruttore centrale che aiuta i tumori gastrici a costruire una nicchia immunosoppressiva, soprattutto tramite macrofagi specializzati che sia presentano materiale tumorale sia inviano segnali inibitori alle cellule T. Per i pazienti, ciò suggerisce che un’alta espressione di VISTA segna una forma di resistenza agli attuali farmaci immunoterapici che mirano solo a PD-1 o PD-L1. Bloccare VISTA—possibilmente in combinazione con gli inibitori dei checkpoint esistenti—potrebbe rivitalizzare le cellule T e riportare l’equilibrio verso il controllo del tumore. Pur richiedendo ulteriori studi di laboratorio e clinici, questa ricerca offre una roadmap per progettare nuove combinazioni terapeutiche e per identificare quali pazienti hanno maggiori probabilità di beneficiarne.
Citazione: Luo, Y., Peng, H., Yao, Q. et al. Immunosuppressive immune microenvironment landscapes in VISTA-high gastric cancer. Br J Cancer 134, 1066–1079 (2026). https://doi.org/10.1038/s41416-025-03290-0
Parole chiave: carcinoma gastrico, microambiente tumorale, checkpoint immunitario, macrofagi, esaurimento delle cellule T