Clear Sky Science · it
Spettro e funzioni dei canali ionici e dei trasportatori negli osteoclasti
Perché le nostre ossa hanno bisogno di minuscoli guardiani
Il nostro scheletro sembra solido e immutabile, ma è costantemente demolito e ricostruito. Cellule specializzate chiamate osteoclasti agiscono come la squadra di demolizione, dissolvendo l’osso vecchio perché ne possa formarsi di nuovo. Questo articolo di revisione esplora un cast nascosto di proteine microscopiche “guardiane” — canali ionici e trasportatori — che consentono agli atomi carichi e ai nutrienti di entrare e uscire dagli osteoclasti. Capendo come questi piccoli cancelli controllano la degradazione ossea, gli scienziati sperano di ideare trattamenti migliori per l’osteoporosi e altre malattie ossee.
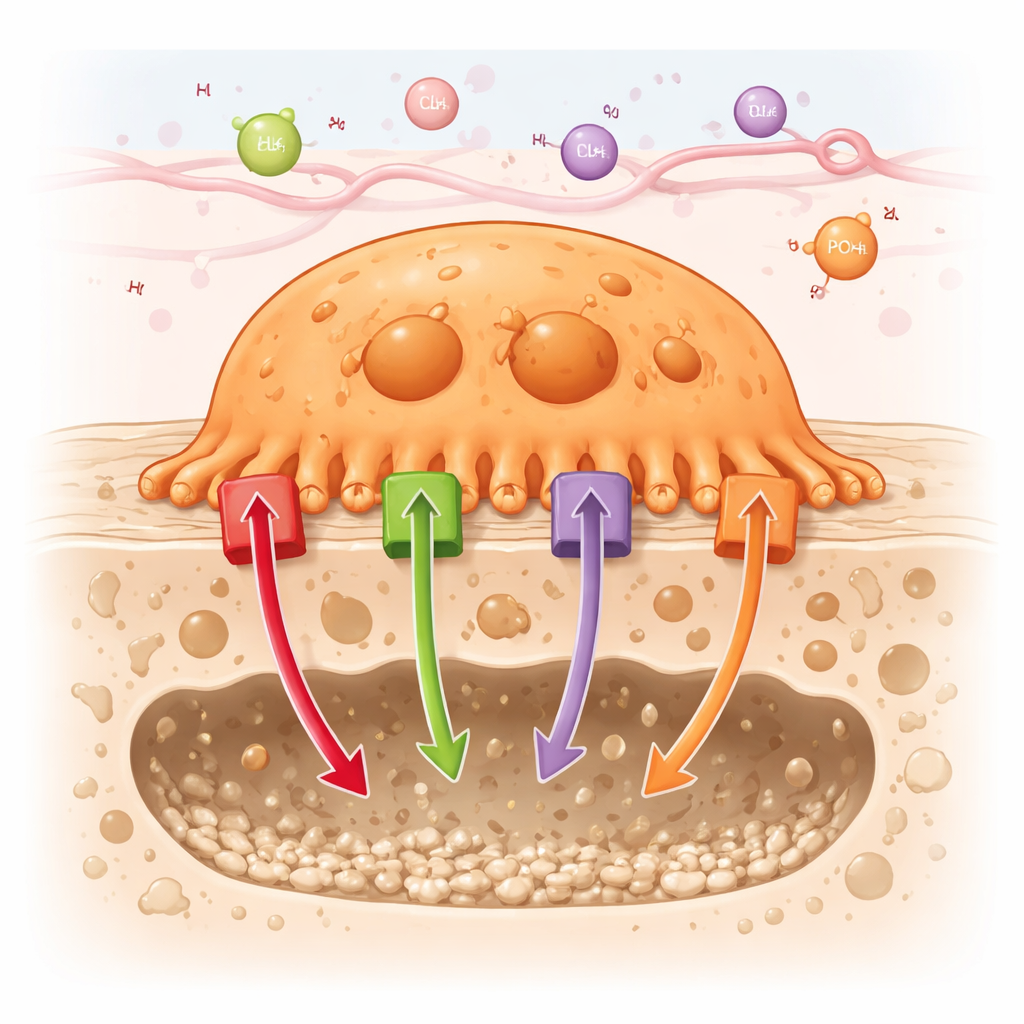
Come le cellule che “mangiano” l’osso compiono il loro lavoro
Gli osteoclasti lavorano aderendo saldamente alla superficie ossea e creando una tasca sigillata dove possono dissolvere i minerali e digerire le proteine in sicurezza. Per rendere questa piccola “camera di digestione” estremamente acida, gli osteoclasti pompano grandi quantità di protoni (ioni idrogeno) nella tasca. Allo stesso tempo, spostano altri ioni — come cloruro, calcio e fosfato — attraverso le loro membrane e compartimenti interni. L’articolo esamina circa 90 diversi canali e trasportatori presenti negli osteoclasti e li raggruppa in sei famiglie, tra cui pompe alimentate dall’energia (ATPasi), canali per cationi e anioni, trasportatori accoppiati, vettori per nutrienti e trasportatori ATP‑binding cassette (ABC).
Acido, sale ed energia: la macchina centrale
Due sistemi proteici emergono come centrali per il riassorbimento osseo. Primo, pompe vacuolari per i protoni note come V‑ATPasi spingono attivamente i protoni nella tasca di riassorbimento, rendendola sufficientemente acida da sciogliere il minerale osseo e attivare enzimi proteolitici. Subunità specifiche della V‑ATPasi, come a3, d2 e diverse componenti di V1, sono arricchite al bordo rugoso dell’osteoclasto e nei lisosomi, e difetti genetici in queste subunità possono indebolire l’osso o causarne un inspessimento anomalo. Secondo, uno scambiatore cloro‑protone chiamato ClC‑7, che si associa a una proteina denominata OSTM1, porta ioni cloruro nella stessa area. Questo bilancia la carica elettrica e permette il pompaggio continuo di protoni. Quando ClC‑7 è mutato, umani e topi sviluppano osteopetrosi, una condizione caratterizzata da ossa troppo dense ma fragili, illustrando quanto sia essenziale il corretto flusso ionico per la salute scheletrica normale.
Calcio, fosfato e altri protagonisti di supporto
Oltre alla produzione di acidità, gli osteoclasti dipendono da una gestione finemente regolata del calcio e del fosfato. Una rete di canali e pompe per il calcio nella membrana cellulare, nel reticolo endoplasmatico, nei lisosomi e nei mitocondri genera “oscillazioni” di calcio ritmiche che attivano geni chiave per la formazione e la fusione degli osteoclasti. Trasportatori al bordo rugoso e sul lato opposto della cellula muovono calcio e fosfato dall’osso dissolto, riciclandoli all’interno della cellula o restituendoli al flusso sanguigno. Altri metalli e minerali — come manganese, magnesio, zinco, rame e ferro — sono anch’essi regolati da trasportatori specializzati e influenzano quanto vigorosamente gli osteoclasti riassorbano l’osso. Per esempio, il ferro e alcune forme di morte cellulare legate al ferro possono aumentare o ridurre l’attività degli osteoclasti, mentre i trasportatori dello zinco tendono a limitare la perdita ossea eccessiva.
Controllo del traffico dentro la cellula
I canali ionici non sono confinati alla membrana esterna. Molti si trovano su compartimenti interni come lisosomi, endosomi, apparato di Golgi e mitocondri, creando una rete di trasporto stratificata. Questi cancelli interni aiutano a regolare il pH nelle vescicole digestive, la produzione di energia nei mitocondri e il movimento di enzimi e detriti. La revisione evidenzia come più sistemi di canali lavorino insieme: gli scambiatori sodio‑idrogeno regolano l’acidità interna, i cotrasportatori potassio‑cloruro contribuiscono a mantenere il potenziale di membrana e l’equilibrio del cloruro, e i canali purinergici e meccanosensibili traducono segnali chimici o meccanici in cambiamenti del riassorbimento osseo. I trasportatori di nutrienti per glucosio, amminoacidi, nucleosidi e vitamina C supportano inoltre l’elevata domanda energetica e biosintetica degli osteoclasti attivamente riassorbenti.
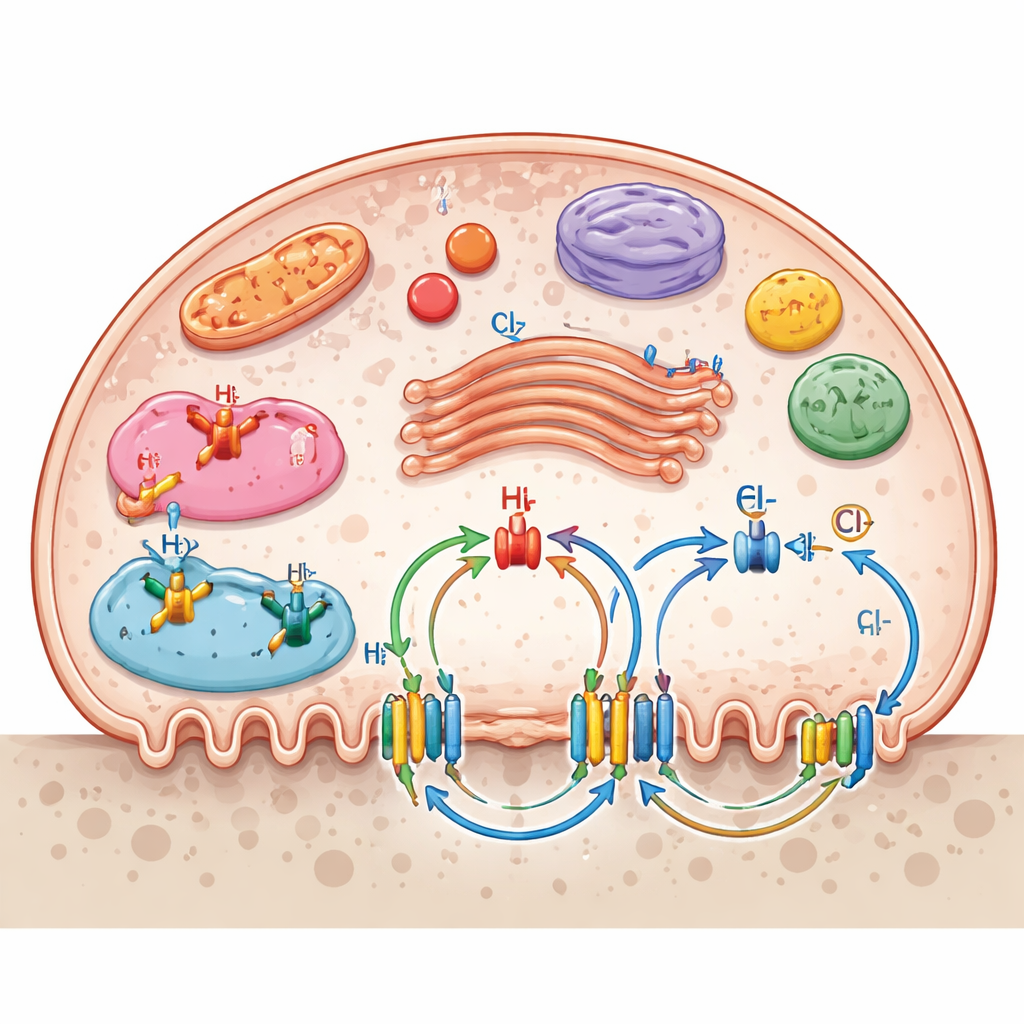
Dalla biologia di base a nuovi trattamenti
Poiché molte patologie ossee nascono quando gli osteoclasti sono sovra‑ o sottoattivi, i canali e i trasportatori che guidano il loro comportamento sono bersagli farmacologici attraenti. Gli autori rivedono composti esistenti ed esperimenti che bloccano V‑ATPasi, canali TRP del calcio, scambiatori di cloro, recettori purinergici e altri trasportatori, oltre a idee più recenti come la perturbazione di specifiche interazioni tra subunità o l’uso di nanoparticelle mirate per somministrare farmaci direttamente all’osso. Sottolineano che molte di queste proteine si trovano anche in altri tessuti, quindi ottenere una vera specificità per gli osteoclasti resta una sfida. Tuttavia, man mano che strumenti genomici e di imaging rivelano meglio dove risiedono questi canali e come interagiscono, la mappa ionica in espansione degli osteoclasti promette di fornire terapie più precise per l’osteoporosi, la perdita ossea infiammatoria e le rare malattie ossee genetiche.
Citazione: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Parole chiave: osteoclasti, canali ionici, riassorbimento osseo, V-ATPase, osteoporosi