Clear Sky Science · it
PRMT6 è necessario per l’avvio e l’amplificazione dell’infiammazione indotta dai macrofagi nell’ossificazione eterotopica aumentando l’espressione di CCL2
Quando la guarigione esagera
Talvolta, dopo una grave ferita o un intervento chirurgico, il corpo cerca di riparare così intensamente che arriva a creare nuovo tessuto osseo dove non dovrebbe esserci. Questa condizione dolorosa, nota come formazione ossea non desiderata nei tessuti molli, può immobilizzare le articolazioni, complicare le amputazioni e rendere difficili i movimenti quotidiani. Le terapie attuali sono limitate e spesso non riescono a prevenire le ricadute. Questo studio individua un interruttore precoce chiave nel sistema immunitario che collega il trauma a questa formazione ossea anomala — e mette in evidenza una breve ma critica finestra temporale in cui un trattamento mirato potrebbe interrompere il processo prima che inizi. 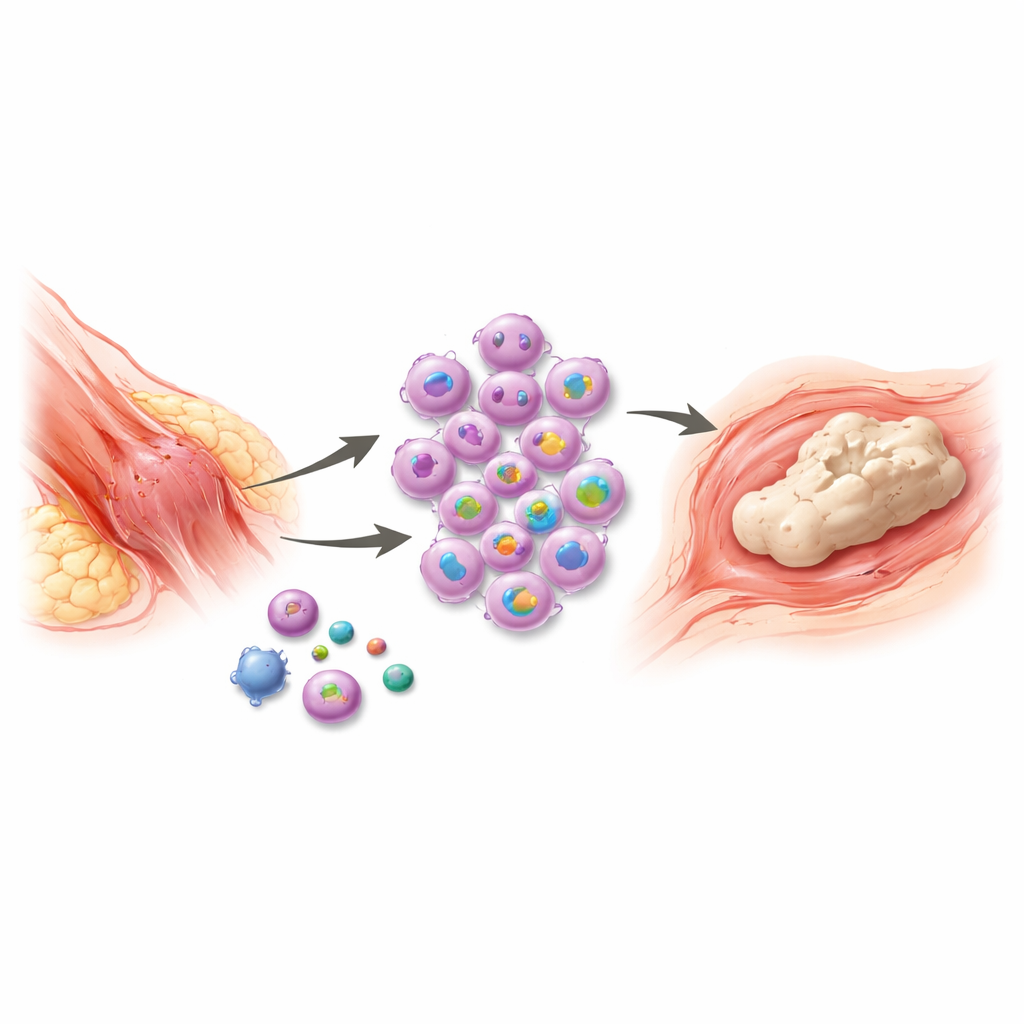
Il problema dell’osso nel posto sbagliato
Dopo traumi importanti, come ustioni, fratture o interventi ortopedici, alcuni pazienti sviluppano isole di osso all’interno di muscoli, tendini e altri tessuti molli. Il nuovo osso si forma attraverso un processo simile allo sviluppo osseo normale, iniziando con l’infiammazione e concludendosi con tessuto maturo e mineralizzato. Sebbene i medici sappiano che le cellule immunitarie chiamate macrofagi sono centrali in questa risposta, il controllo passo dopo passo di come accendono e mantengono l’infiammazione non era chiaro. In mancanza di questa conoscenza, terapie come farmaci antiinfiammatori, radioterapia o rimozione chirurgica tardiva trattano per lo più le conseguenze, non la causa, e la recidiva è comune.
Il mediatore chiave dell’infiammazione
Usando un modello murino che combina una lesione al tendine con una ustione — che imita da vicino il trauma grave nell’uomo — i ricercatori hanno seguito cosa accade nel sito della lesione nel tempo. Hanno osservato un rapido accumulo di macrofagi nei primi giorni dopo l’infortunio, che poi persisteva durante la formazione dell’osso anomalo. Quando queste cellule sono state eliminate, l’osso in eccesso è quasi scomparso e i tessuti circostanti mostravano molta meno alterazione dei vasi sanguigni e delle cellule di sostegno. Un’analisi genica approfondita dei tessuti lesionati ha evidenziato una molecola in questi macrofagi che spiccava: PRMT6, un’enzima che modifica le proteine e contribuisce a controllare quali geni vengono attivati.
Una manopola molecolare per l’infiammazione
Il gruppo ha scoperto che i livelli di PRMT6 nei macrofagi aumentavano rapidamente dopo la lesione e in risposta a segnali di pericolo e componenti batterici in laboratorio. I topi privi di PRMT6, o nei quali PRMT6 era ridotto selettivamente solo nei macrofagi, avevano molti meno macrofagi nel sito della lesione e sviluppavano molto meno osso anomalo. Importante, i tendini lesionati in questi animali guarivano in realtà meglio, con un tessuto più ordinato e meno formazione di cicatrice. Ciò indica che PRMT6 non è necessario per la riparazione sana, ma agisce piuttosto come una manopola che amplifica un’infiammazione dannosa. Quando i ricercatori hanno bloccato PRMT6 con un farmaco, l’effetto si osservava solo se somministrato precocemente — durante le prime settimane dopo la lesione. Iniziare il trattamento più tardi aveva scarso effetto, rivelando una finestra terapeutica ristretta ma potente. 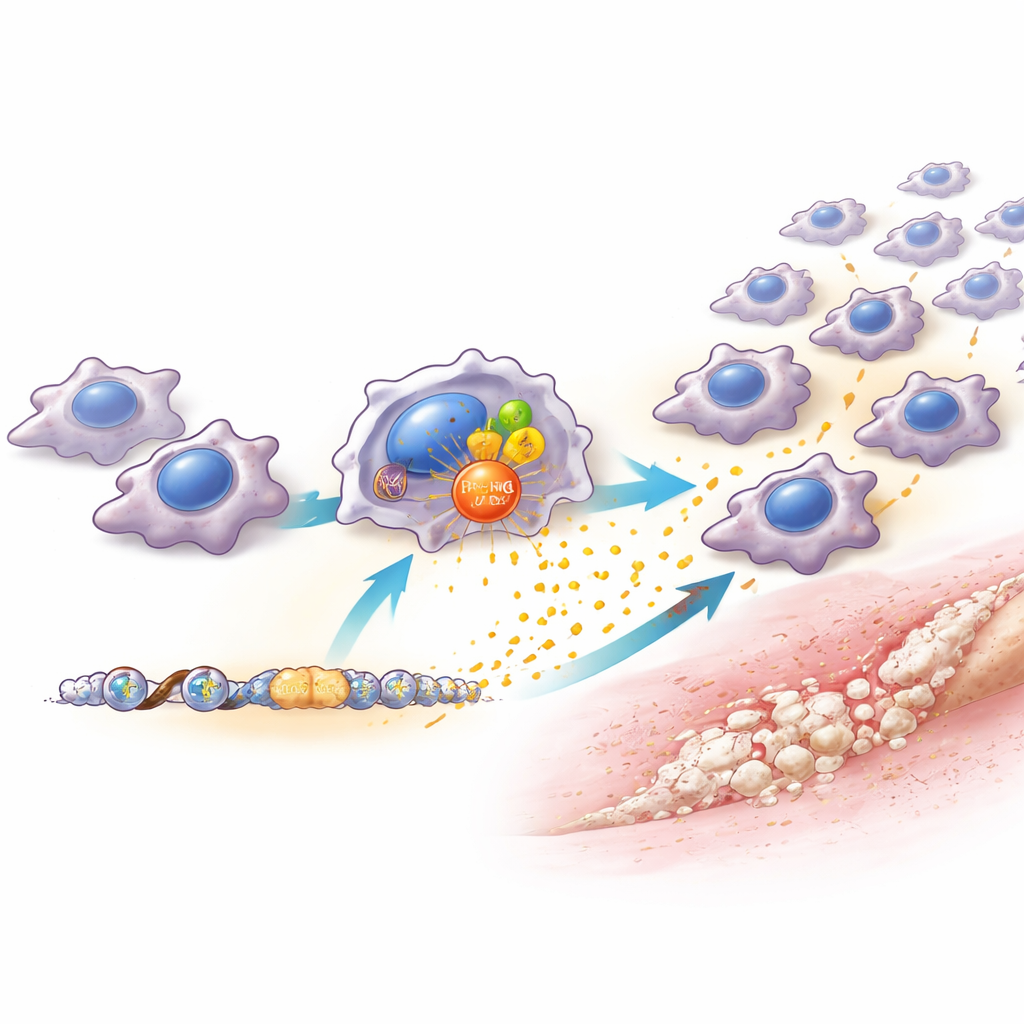
Come un segnale attira molte cellule immunitarie
Per capire come PRMT6 eserciti questo effetto, gli scienziati hanno studiato i macrofagi in dettaglio. In assenza di PRMT6, queste cellule producevano quantità molto inferiori di diversi chemoattrattanti, in particolare di una molecola chiamata CCL2, che normalmente richiama più monociti e macrofagi dal flusso sanguigno verso i tessuti lesionati. PRMT6 contribuisce ad attivare il gene CCL2 in due modi: si associa al noto regolatore dell’infiammazione NF-κB e marca chimicamente le proteine che impacchettano il DNA nelle vicinanze per rendere quel gene più facilmente leggibile. Di conseguenza, i macrofagi con alti livelli di PRMT6 secernono più CCL2, attirando altri macrofagi e costruendo un “centro infiammatorio” che sostiene vasi sanguigni e cellule progenitrici osteogeniche. Quando CCL2 è stato ridotto specificamente solo nei macrofagi, l’esito ha imitato da vicino la perdita di PRMT6 — meno macrofagi, nicchie infiammatorie più deboli e meno osso in eccesso. Il reintegro di CCL2 ha parzialmente ripristinato sia l’afflusso di macrofagi sia la formazione ossea anomala.
Un’opportunità mirata per prevenire l’osso indesiderato
Nel complesso, lo studio dimostra che PRMT6 nei macrofagi agisce come un amplificatore epigenetico precoce: potenzia un segnale chimico chiave che recluta più cellule immunitarie, le quali a loro volta guidano la formazione di osso dove non dovrebbe esserci. Poiché bloccare PRMT6 solo durante la fase infiammatoria iniziale ha ridotto nettamente l’osso indesiderato preservando la normale guarigione del tendine — e migliorando persino l’organizzazione tissutale — questa via rappresenta una strategia promettente. In linea di principio, un breve ciclo ben temporizzato di terapia mirata contro PRMT6 dopo trauma o intervento chirurgico importante potrebbe prevenire la disabilità a lungo termine dovuta all’osso ectopico, senza compromettere la naturale capacità del corpo di ripararsi.
Citazione: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Parole chiave: ossificazione eterotopica, macrofagi, infiammazione, regolazione epigenetica, segnalazione CCL2