Clear Sky Science · it
C/EBPβ determina la trascrizione di FSHβ dopo la menopausa e il blocco della via AEP/C/EBPβ allevia l’osteoporosi
Perché questa ricerca conta per la vita dopo la menopausa
Molte donne sentono dire che la diminuzione degli estrogeni è il principale responsabile della fragilità ossea dopo la menopausa. Questo studio aggiunge un nuovo tassello al quadro: un altro ormone, l’ormone follicolo‑stimolante (FSH), e una coppia di proteine nel cervello e nell’osso—C/EBPβ e AEP—agiscono insieme per accelerare la perdita ossea. Ancora più interessante, i ricercatori mostrano nei topi che bloccare questa via con una compressa sperimentale può proteggere le ossa con la stessa efficacia di un farmaco approvato per l’osteoporosi.
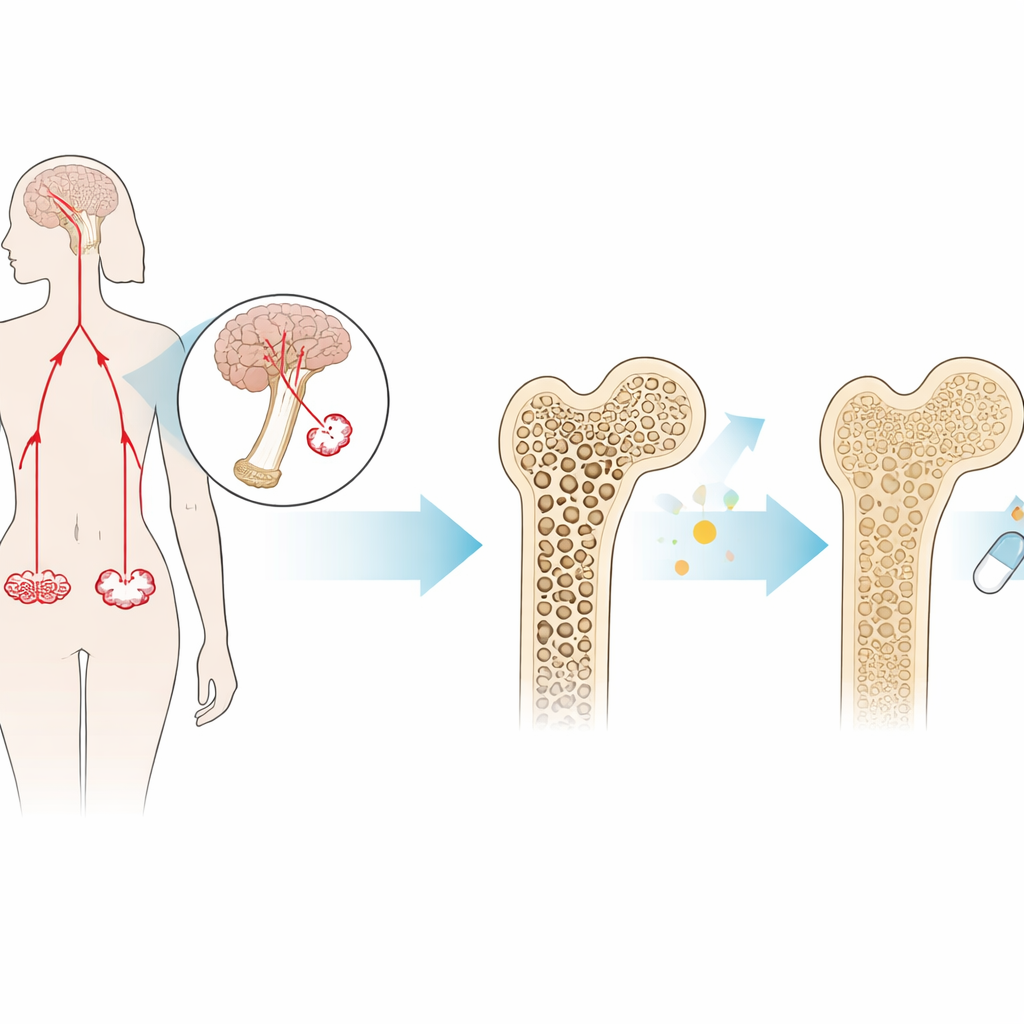
Un ormone meno noto ma con grande impatto sull’osso
FSH è prodotto nell’ipofisi ed è noto soprattutto per il suo ruolo nella fertilità. Nelle donne che si avvicinano alla menopausa, i livelli di FSH aumentano bruscamente diversi anni prima dell’ultima mestruazione. Oltre al ruolo riproduttivo, l’FSH può agire direttamente sull’osso: si lega ai recettori sulle cellule che riassorbono l’osso (osteoclasti), spingendole a consumare l’osso più rapidamente di quanto venga ricostruito. Lavori precedenti hanno mostrato che i topi privi di FSH o del suo recettore sono protetti dalla perdita ossea, anche quando gli estrogeni sono bassi. Ciò suggeriva che l’FSH stesso, e non solo la carenza di estrogeni, può guidare l’osteoporosi postmenopausale.
Il comando nell’ipofisi
Il nuovo studio si concentra su C/EBPβ, una proteina che si lega al DNA e attiva o spegne i geni. Gli autori hanno scoperto che C/EBPβ si lega direttamente alla regione di controllo del gene della subunità beta dell’FSH—the parte dell’ormone che ne determina l’identità—e ne aumenta la produzione nell’ipofisi. In colture di cellule ipofisarie, aumentare C/EBPβ ha incrementato l’FSH, mentre silenziare C/EBPβ lo ha ridotto, soprattutto quando le cellule erano stimolate dal segnale riproduttivo cerebrale, il GnRH. Nei topi ovariectomizzati, che imitano la menopausa rimuovendo le ovaie produttrici di estrogeni, gli animali con C/EBPβ ridotto hanno prodotto molta meno FSH nell’ipofisi e nel sangue. Questi esperimenti rivelano C/EBPβ come un interruttore chiave che determina quanto l’FSH aumenta dopo il calo degli estrogeni.
Un anello auto‑alimentante e un nuovo bersaglio farmacologico
C/EBPβ controlla anche un’altra proteina chiamata AEP, un enzima che taglia e può attivare o inattivare altre molecole. Nel cervello, una catena C/EBPβ–AEP è stata collegata a danni simili all’Alzheimer. Qui il gruppo ha indagato se la stessa catena influenzi l’FSH e l’osso. Nei topi privi di AEP, i livelli sia di C/EBPβ sia di FSH sono diminuiti nell’ipofisi e la perdita ossea dopo la rimozione delle ovaie è stata ridotta. Bloccare AEP con una piccola molecola, chiamata #11a, ha prodotto un effetto simile: dopo mesi di trattamento, i topi ovariectomizzati avevano FSH più basso, ossa più forti alle scansioni ad alta risoluzione e meno cellule riassorbenti ossee iperattive. Un’altra classe di composti—attivatori di TrkB che attenuano indirettamente AEP—ha aiutato le cellule ossee in coltura ma non è riuscita ad abbassare l’FSH negli animali, soprattutto perché il recettore bersaglio è scarso nell’ipofisi. Questo contrasto ha rafforzato la conclusione che inibire direttamente AEP è un modo più potente per spegnere l’asse C/EBPβ–FSH alla sua fonte.
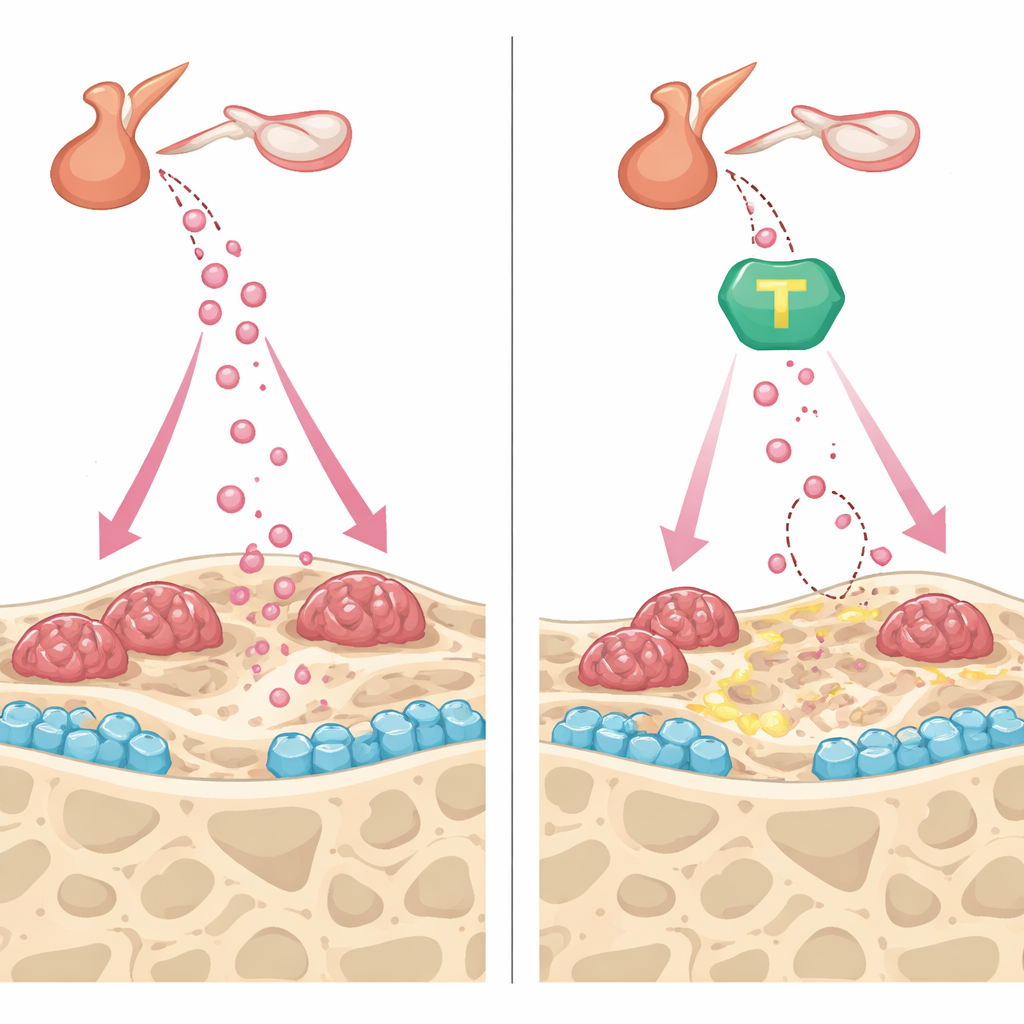
Proteggere l’osso da due angolazioni
Oltre ad abbassare l’FSH, #11a e l’attivatore di TrkB CF3CN hanno mostrato benefici complementari all’interno dell’osso stesso. Nelle colture di cellule che formano osso, entrambi i composti hanno accelerato la maturazione e la deposizione di minerale, in parte preservando la fibronectina, una proteina strutturale che AEP normalmente taglia, e aumentando segnali pro‑osso come l’osteoprotegerina. Nelle cellule che riassorbono l’osso, i farmaci hanno attenuato gli effetti di un segnale chiave di riassorbimento, riducendo il numero di grandi cellule multinucleate e la loro capacità di scavare fossette nelle fette di osso. Nei topi vivi, sia #11a sia CF3CN hanno frenato l’elevato ricambio osseo scatenato dalla rimozione delle ovaie, stabilizzando la densità e la microarchitettura ossea. Colpisce che, confrontando #11a direttamente con il teriparatide, un iniettabile approvato dalla FDA che costruisce osso, la compressa sperimentale eguagliò la capacità del teriparatide di ripristinare il volume e la resistenza ossea in questo modello.
Cosa potrebbe significare per la cura futura dell’osteoporosi
Per un non specialista, la conclusione è che questo lavoro identifica una via con doppia funzione che collega l’infiammazione associata alla menopausa all’aumento dell’FSH e al danno osseo, e mostra che mirare ad AEP può interrompere questa catena. Nei topi, un inibitore orale di AEP non solo riduce l’eccesso di FSH che alimenta la perdita ossea, ma sposta direttamente l’equilibrio all’interno dell’osso verso la formazione piuttosto che la degradazione. Pur richiedendo ancora la verifica negli esseri umani, questi risultati suggeriscono che i futuri trattamenti per l’osteoporosi potrebbero andare oltre la semplice sostituzione degli estrogeni o la stimolazione della formazione ossea e invece silenziare questo circuito ormonale ed enzimatica appena mappato che guida la fragilità ossea postmenopausale.
Citazione: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Parole chiave: osteoporosi postmenopausale, ormone follicolo-stimolante, via C/EBPβ AEP, rimodellamento osseo, terapia mirata agli ormoni