Clear Sky Science · it
La formazione di cicatrici fibrotiche indotta da TGF-β limita il recupero dopo lesione del midollo spinale
Perché le cicatrici nel midollo spinale sono importanti
Quando il midollo spinale subisce un grave danno, molte persone restano con paralisi permanente o perdita di sensibilità perché le fibre nervose danneggiate non riescono a ricrescere. Questo studio pone una domanda semplice ma cruciale: che cosa, esattamente, ostacola questa ricrescita — e possiamo rimuovere la barriera in modo sicuro? Scoprendo come si forma un particolare tipo di cicatrice all’interno del midollo lesionato, gli autori indicano una nuova via per aiutare il sistema nervoso a ripararsi.
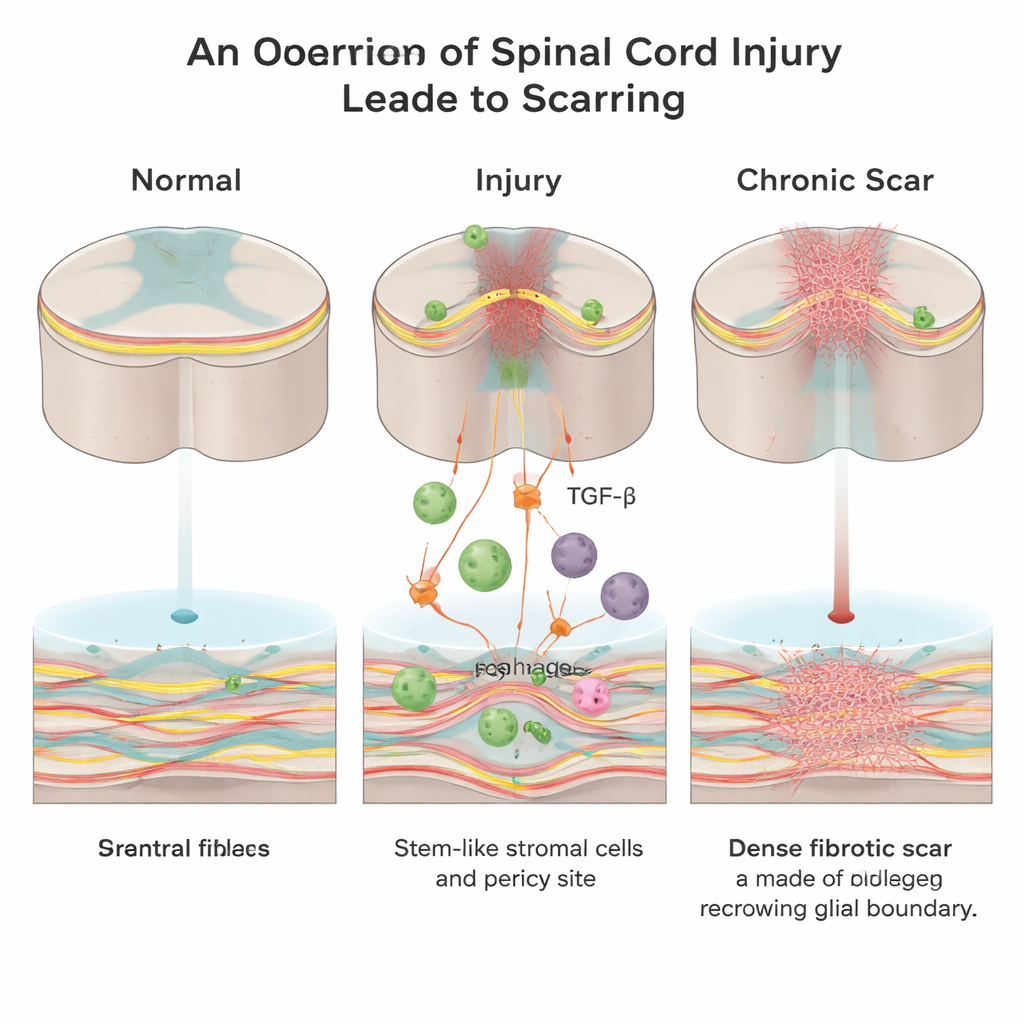
Un muro nascosto all’interno della lesione
Dopo una lesione del midollo spinale, il corpo si attiva per sigillare la ferita. Si formano due principali tipi di tessuto cicatriziale: una cicatrice “gliale” prodotta dalle cellule di supporto chiamate astrociti, e una cicatrice “fibrotica” ricca di collagene, fibronectina e cellule fibroblastiche. Se la cicatrice gliale può avere ruoli protettivi, la cicatrice fibrotica crea una barriera fisica e chimica densa che le fibre nervose in crescita non riescono facilmente a superare. Fino a oggi, gli scienziati sapevano molto meno su come appare questo nucleo fibrotico e quali segnali ne guidano la formazione.
Il ruolo delle cellule immunitarie e di un potente segnale
Lavorando su topi adulti, i ricercatori si sono concentrati su una molecola di segnalazione chiamata fattore di crescita trasformante‑beta (TGF‑β), che coordina la riparazione delle ferite in tutto il corpo ed è spesso iperattiva nelle malattie fibrotiche. Hanno scoperto che, dopo la lesione del midollo, le cellule immunitarie infiltranti note come macrofagi diventano una fonte principale di TGF‑β1 attivo nella sede della lesione. Questa ondata di TGF‑β1 recluta cellule stromali/mesenchimali locali e cellule associate ai vasi chiamate periciti e le spinge a trasformarsi in fibroblasti — proprio le cellule che depositano la cicatrice fibrotica ricca di collagene.
Abbassare il segnale per aprire un passaggio
Per verificare se questa via causa davvero cicatrici dannose, il team ha usato diversi trucchi genetici nei topi. Quando hanno rimosso i macrofagi, o eliminato il gene del TGF‑β1 solo nelle cellule di linea macrofagica, la quantità di tessuto fibrotico nel midollo lesionato è diminuita nettamente, e più fibre nervose e vie contenenti serotonina sono riuscite a attraversare la zona della lesione. Allo stesso modo, eliminare il recettore del TGF‑β specificamente nei periciti ha ridotto la loro risposta al TGF‑β, portato a meno accumulo di collagene e migliorato movimento e sensibilità nei test comportamentali. È importante notare che i periciti e le cellule simil‑staminali correlate erano ancora presenti, ma avevano meno probabilità di diventare fibroblasti formatori di cicatrice.
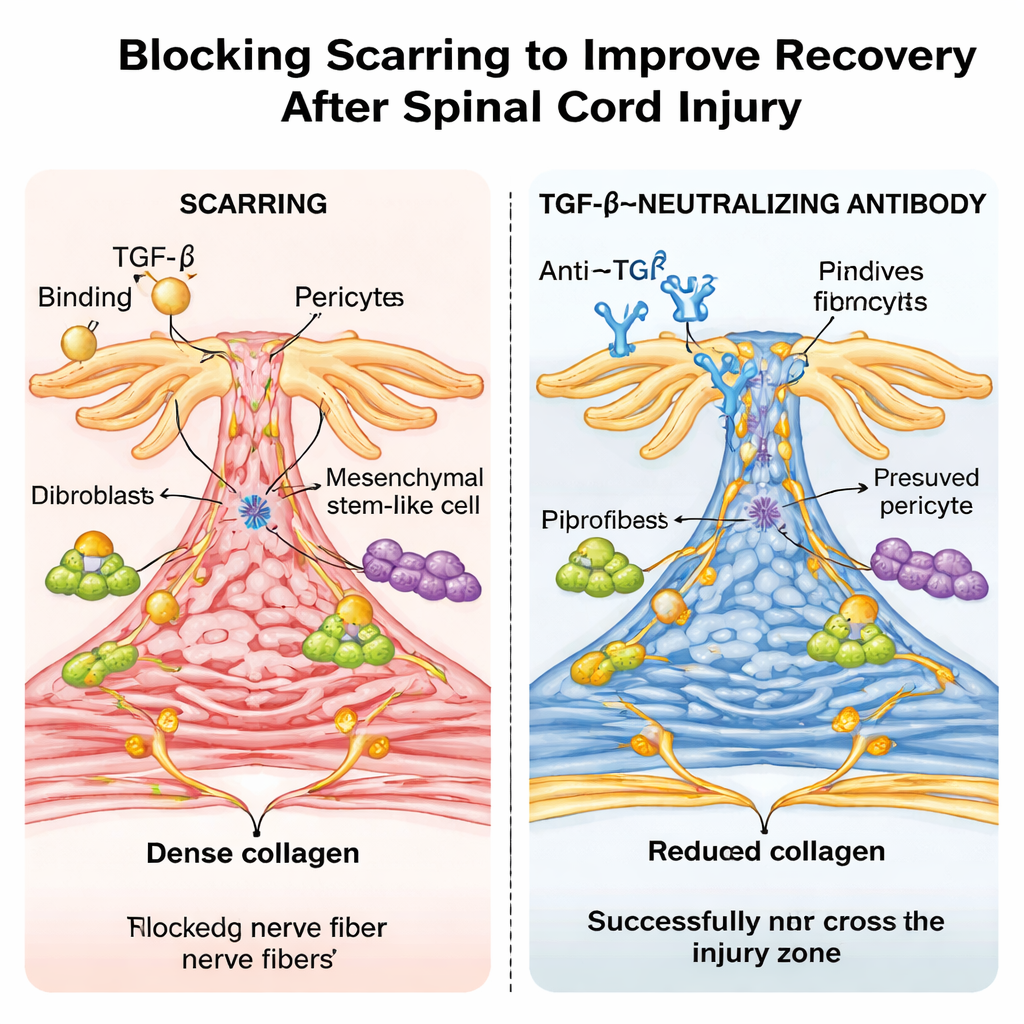
Un anticorpo simile a un farmaco e un sorprendente effetto dell’età
I ricercatori hanno quindi provato un approccio più clinicamente rilevante: trattare topi ordinari con un anticorpo di laboratorio che neutralizza il TGF‑β. Dosi ripetute dopo la lesione hanno abbassato i livelli di TGF‑β attivo nel sangue e nel midollo, ridotto la cicatrice fibrotica e permesso alle fibre nervose di collegare la lesione in modo più efficace, con evidenti miglioramenti nella deambulazione e nella funzione sensoriale. Il sequenziamento dell’RNA a singola cellula ha confermato che i geni rispondenti al TGF‑β erano fortemente attivi nei tipi cellulari formatori di cicatrice nei topi non trattati e venivano attenuati dall’anticorpo. Sorprendentemente, quando lo stesso tipo di schiacciamento del midollo spinale è stato eseguito nei topi neonati, gli animali guarivano quasi senza cicatrici fibrotiche, non mostravano attivazione rilevabile del TGF‑β nel sito della lesione e recuperavano un movimento quasi normale — assomigliando alla riparazione senza cicatrice osservata in alcuni animali non mammiferi.
Che cosa potrebbe significare per i trattamenti futuri
Nel complesso, i risultati suggeriscono che l’attivazione eccessiva del TGF‑β dopo una lesione del midollo spinale devia le cellule riparative utili verso la costruzione di una rigida parete fibrotica che blocca la ricrescita nervosa e il recupero funzionale. Impedendo questa sovra‑attivazione — sia mirando alla produzione di TGF‑β nei macrofagi, bloccando il suo recettore su periciti e cellule stromali, o usando un anticorpo neutralizzante — potrebbe essere possibile ridurre la cicatrice dannosa preservando o addirittura migliorando tipi di risposta tissutale più benefici. Sebbene la traduzione di queste strategie negli esseri umani richiederà studi accurati per evitare effetti collaterali, questo lavoro mette in evidenza la cicatrizzazione fibrotica guidata da TGF‑β come una barriera centrale e potenzialmente farmacologicamente modulabile alla riparazione del midollo spinale.
Citazione: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Parole chiave: lesione del midollo spinale, cicatrice fibrotica, TGF-beta, macrofagi, rigenerazione nervosa