Clear Sky Science · it
Le vescicole extracellulari derivate dai macrofagi sinoviali infiammatori aggravano le lesioni cartilaginee con un meccanismo di smistamento selettivo da parte di FMRP nell’osteoartrite
Perché l’infiammazione articolare conta per il dolore al ginocchio
Molti vedono l’osteoartrite come un semplice «consumo» delle articolazioni legato all’età, ma prove crescenti mostrano che un’infiammazione a basso grado all’interno dell’articolazione può spingere silenziosamente la malattia in avanti. Questo studio pone una domanda precisa: come comunicano le cellule immunitarie del rivestimento articolare con le cellule della cartilagine, e si può interrompere questa conversazione per proteggere le articolazioni? Le risposte rivelano un minuscolo sistema di corrieri molecolari che peggiora il danno — ma offre anche nuove strade per diagnosticare e trattare l’osteoartrite.
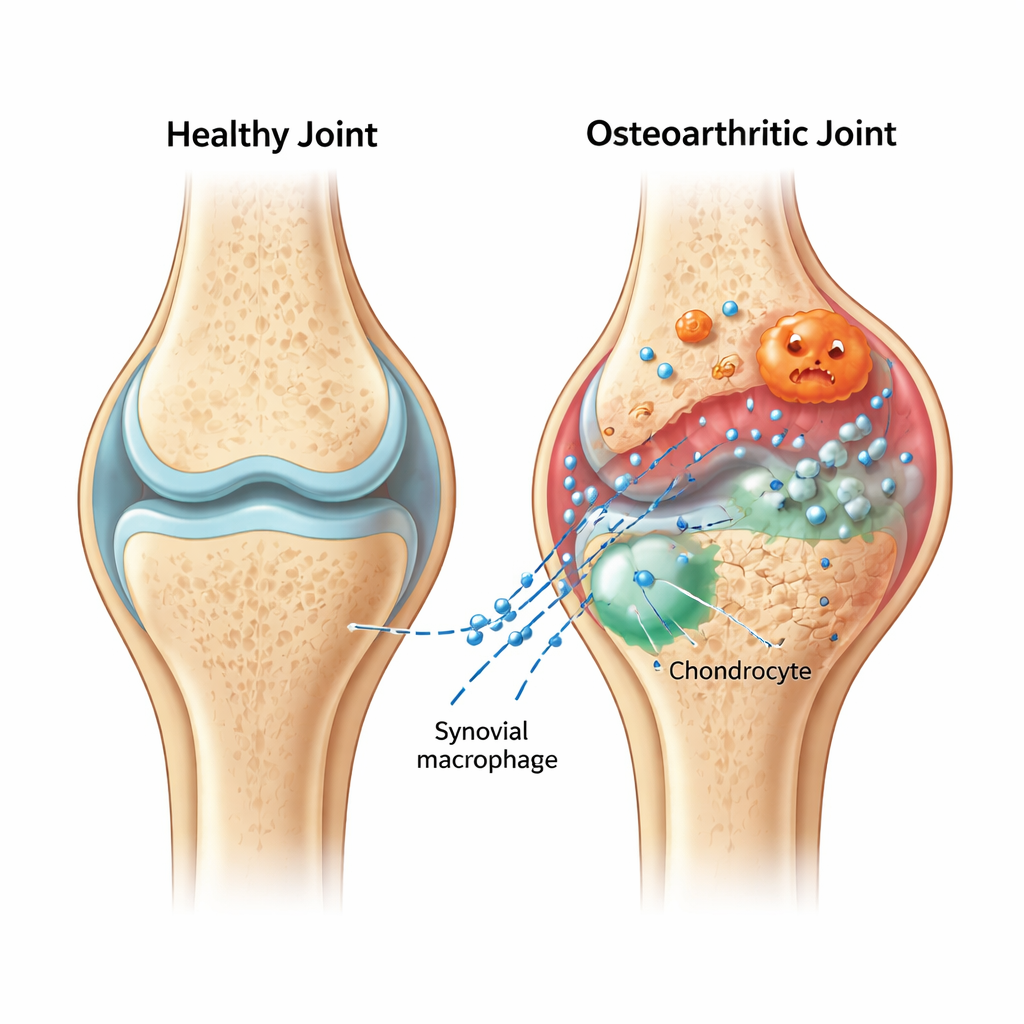
Pacchetti minuscoli che portano cattive notizie
All’interno di un ginocchio artrosico, il morbido rivestimento sinoviale si infiamma e si riempie di cellule immunitarie chiamate macrofagi. Gli autori si sono concentrati sulla versione «infiammatoria» di queste cellule — i macrofagi pro-infiammatori — e sulle microscopiche bolle che rilasciano, note come vescicole extracellulari. Queste vescicole funzionano come pacchetti sigillati che trasportano molecole tra le cellule. In ratti con osteoartrite indotta chirurgicamente, il gruppo ha dimostrato che le vescicole provenienti da macrofagi infiammati prendono di mira la cartilagine e aggravano il danno: la superficie normalmente liscia e ammortizzante diventava più ruvida e sottile, le proteine chiave della cartilagine diminuivano mentre aumentavano gli enzimi di degradazione.
Come l’infiammazione spegne l’autopulizia della cartilagine
Le cellule della cartilagine, o condrociti, fanno affidamento su un processo di manutenzione chiamato autofagia per riciclare componenti usurati e rimanere sane nel tempo. Confrontando i geni attivati nella cartilagine esposta a vescicole infiammatorie rispetto a una soluzione salina innocua, i ricercatori hanno osservato evidenti segnali di soppressione delle vie dell’autofagia. Al microscopio elettronico, la cartilagine dei giunti trattati con vescicole conteneva molte meno delle tipiche vescicole di riciclo. In colture cellulari, i condrociti esposti a vescicole di macrofagi formarono anche meno autofagosomi e autolisosomi, confermando che la loro macchina di autopulizia veniva spenta proprio mentre il danno si accumulava.
Un singolo microRNA capovolge un interruttore critico
Approfondendo, il team ha esaminato i piccoli regolatori di RNA imballati all’interno delle vescicole di macrofagi. Una molecola, miR‑155‑5p, è emersa come particolarmente rilevante: risultava arricchita nelle vescicole di animali con osteoartrite e nei tessuti articolari umani affetti da osteoartrite, soprattutto nella sinovia. Esperimenti hanno mostrato che il miR‑155‑5p trasportato dalle vescicole entra nei condrociti e prende di mira direttamente una proteina chiamata GSK‑3β, che normalmente contribuisce a frenare una via di controllo della crescita nota come mTORC1. Quando GSK‑3β viene soppressa, mTORC1 diventa iperattiva e l’autofagia diminuisce, lasciando i condrociti meno capaci di fronteggiare lo stress. Bloccare miR‑155‑5p con un «antagomiR» progettato nei ratti ha ripristinato l’autofagia, preservato la struttura cartilaginea e ridotto i segni di osteoartrite, mentre topi ingegnerizzati privi di miR‑155 nei loro macrofagi svilupparono una malattia più lieve e meno sinovite.
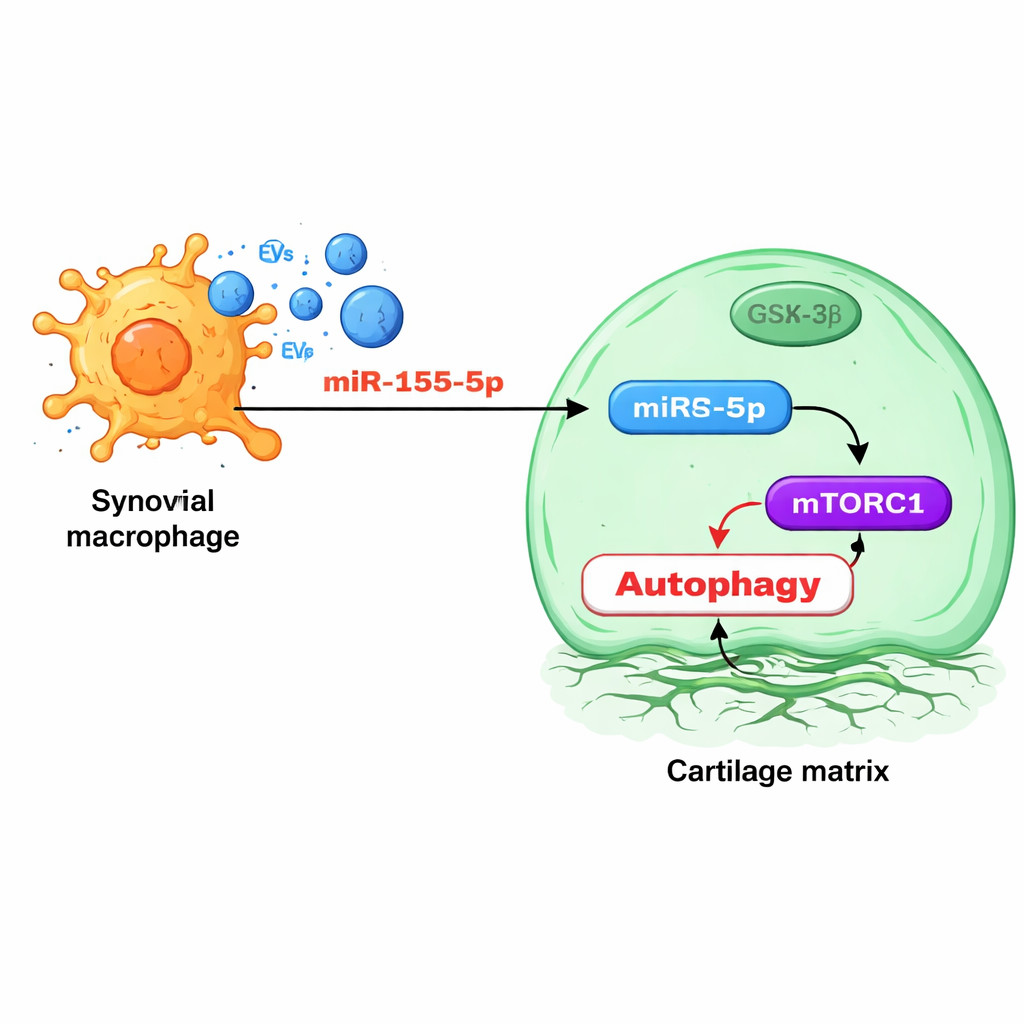
Smistamento e indirizzamento del segnale dannoso
Curiosamente, lo studio ha rilevato che i macrofagi usano una proteina legante l’RNA specifica, FMRP, per caricare selettivamente miR‑155‑5p nelle vescicole. Quando i livelli di FMRP aumentavano, le vescicole trasportavano più miR‑155‑5p e danneggiavano maggiormente i condrociti; quando FMRP diminuiva, le vescicole diventavano meno tossiche e l’autofagia dei condrociti riprendeva. I livelli di FMRP nelle vescicole circolanti nel sangue aumentavano con la progressione dell’osteoartrite sia nei ratti sia nei pazienti umani, suggerendo che questa proteina, o le vescicole che la contengono, potrebbe servire come marcatore sierico dell’attività di malattia senza ricorrere a immagini o procedure invasive.
Una terapia senza cellule che raggiunge le cellule giuste
Sfruttando queste intuizioni meccanicistiche, i ricercatori hanno messo a punto una potenziale terapia usando vescicole derivate da cellule stromali adipose, un tipo di cellule simili a cellule staminali presenti nel tessuto adiposo. Hanno «decorato» queste vescicole con un piccolo peptide che funziona come un dispositivo di richiamo per i macrofagi pro-infiammatori e le hanno caricate con antagomiR‑155‑5p. Nei ratti con osteoartrite, iniezioni ripetute di queste vescicole mirate ridussero l’infiammazione sinoviale, indirizzarono i macrofagi verso uno stato più «riparatore», abbassarono i livelli di miR‑155‑5p nell’articolazione, ripristinarono GSK‑3β e migliorarono la struttura e la composizione della cartilagine più efficacemente rispetto a vescicole non mirate. Applicate a campioni di tessuto sinoviale umano in laboratorio, le vescicole ingegnerizzate ridussero anche i marcatori infiammatori e aumentarono i segnali anti-infiammatori.
Cosa significa per le persone con osteoartrite
Questo lavoro riformula l’osteoartrite come una malattia guidata non solo dall’usura meccanica, ma da un dialogo molecolare tra cellule infiammate del rivestimento articolare e la cartilagine. I macrofagi pro-infiammatori inviano vescicole cariche di miR‑155‑5p, che attenuano i sistemi di auto-riparazione dei condrociti attraverso la via GSK‑3β/mTORC1 e accelerano la degradazione tissutale. Bloccare questo segnale — sia geneticamente che con vescicole terapeutiche mirate — ha permesso ai ricercatori di ridurre sia l’infiammazione sia il danno cartilagineo in modelli animali e in tessuti umani. Pur restando molto lavoro da fare prima che tali strategie raggiungano la clinica, lo studio evidenzia nuove possibilità: esami del sangue basati sul contenuto delle vescicole per monitorare la malattia e terapie precise, senza cellule, che attenuano l’infiammazione dannosa aiutando nel contempo la cartilagine a proteggersi.
Citazione: Zhao, S., Wang, J., Xue, M. et al. Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis. Bone Res 14, 26 (2026). https://doi.org/10.1038/s41413-025-00502-4
Parole chiave: osteoartrite, vescicole extracellulari, macrofagi, cartilagine, microRNA-155