Clear Sky Science · it
Meccanismi di fuga immunitaria e progressi terapeutici nelle neoplasie ematologiche associate a virus
Virus e tumori nascosti nel sangue
La maggior parte di noi pensa ai virus come cause di malattie a breve termine come raffreddore o influenza. Ma una manciata di virus può stabilirsi silenziosamente nell’organismo per lunghi periodi e, anni dopo, contribuire all’insorgenza di gravi tumori del sangue come linfomi e leucemie. Questo articolo di revisione riunisce le conoscenze attuali su come questi virus eludano le difese immunitarie e su come queste informazioni stiano aprendo la strada a trattamenti più mirati e meno tossici.
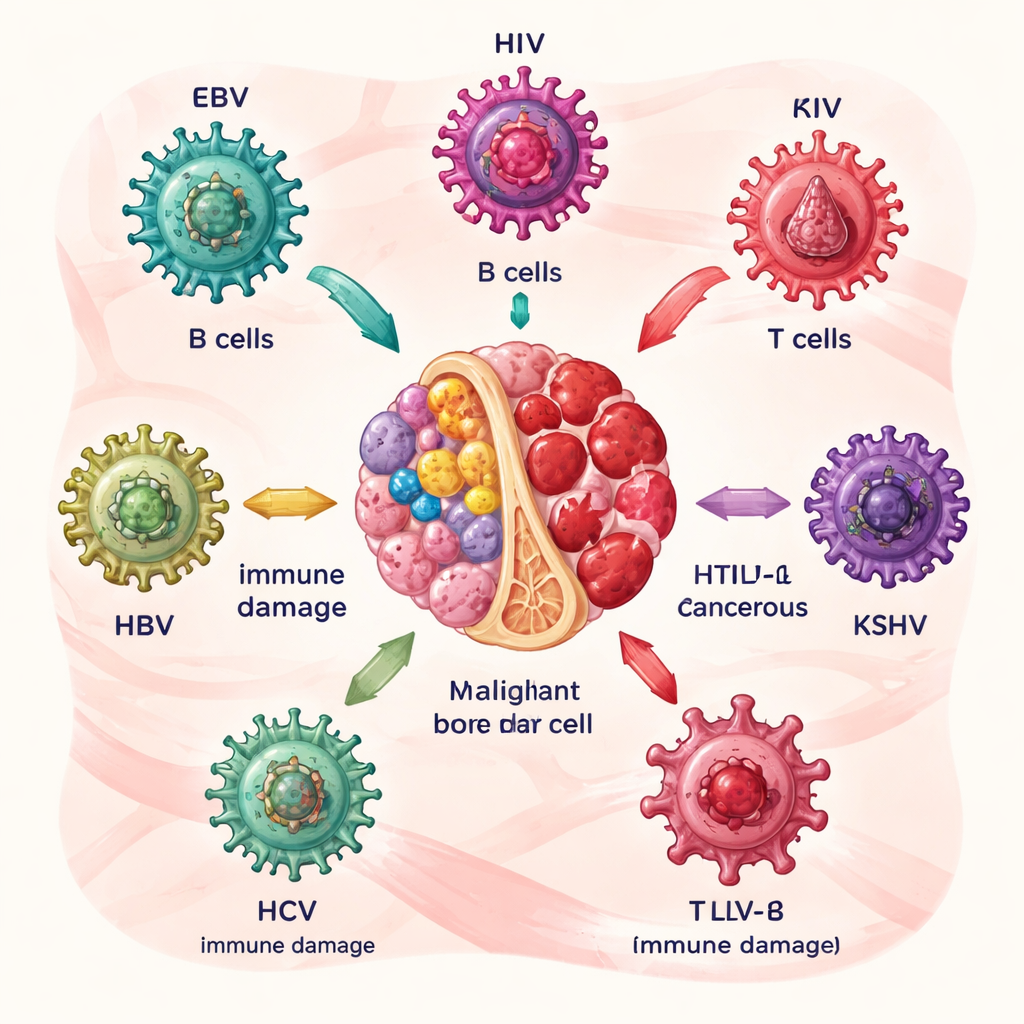
Come certi virus preparano il terreno per il cancro ematologico
Gli autori descrivono innanzitutto sei principali colpevoli: virus di Epstein–Barr (EBV), virus dell’immunodeficienza umana (HIV), virus della leucemia a cellule T umane di tipo 1 (HTLV‑1), herpesvirus associato al sarcoma di Kaposi (KSHV) e i virus dell’epatite B e C (HBV e HCV). Ognuno colpisce cellule del sangue o del sistema immunitario a modo suo. EBV e HCV disturbano principalmente i linfociti B, le cellule produttrici di anticorpi; HTLV‑1 attacca le cellule T; HIV indebolisce l’intero sistema immunitario; KSHV favorisce la crescita anomala di alcune cellule bianche; e HBV e HCV possono annidarsi in linfociti e cellule staminali. Nel corso degli anni, proteine virali spingono le cellule infette a moltiplicarsi, a sfuggire alla morte cellulare programmata e ad accumulare danni al DNA, aumentando gradualmente il rischio di linfomi e malattie correlate.
Come le cellule tumorali imparano a nascondersi dal sistema immunitario
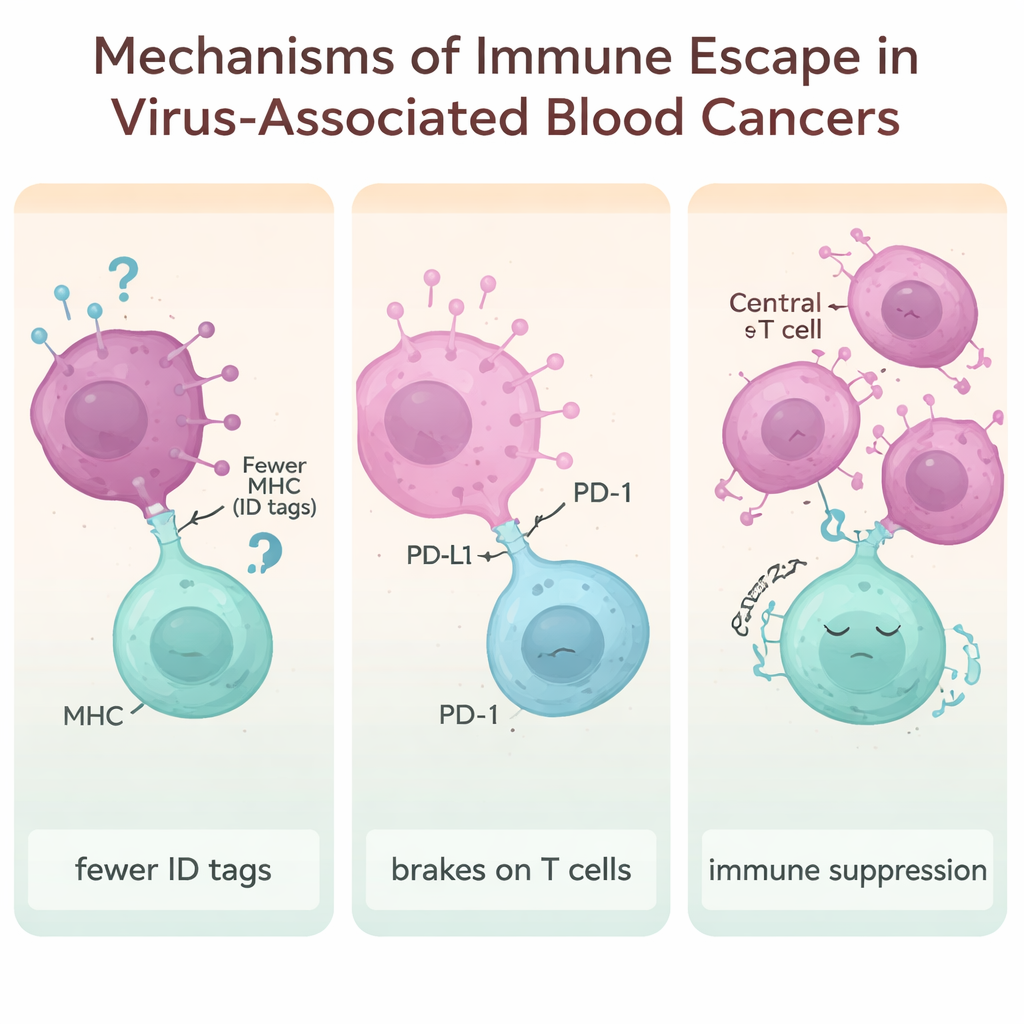
Un tema centrale dell’articolo è la «fuga immunitaria»: i trucchi che i tumori indotti da virus usano per rimanere invisibili o intoccabili per le nostre difese. Una strategia consiste nel ridurre i “badge d’identità” molecolari (detti molecole MHC) sulla superficie cellulare che le cellule T normalmente scandagliano per rilevare il pericolo. Proteine virali di EBV, HTLV‑1, HIV e HBV possono abbassare questi segnali identificativi, rendendo le cellule fuori controllo meno riconoscibili e meno soggette ad attacco. Un altro espediente è sfruttare i «freni» immunitari come PD‑1, PD‑L1, CTLA‑4, LAG‑3 e TIM‑3. Quando questi checkpoint sono iperattivi, le cellule T diventano esauste e poco efficaci. Molti linfomi associati a virus presentano livelli molto elevati di questi freni, in particolare nei tumori legati a EBV e HBV.
Cellule immunitarie trasformate da combattenti in pacificatori
La revisione mette in luce anche una strategia più sottile: rimodellare l’ambiente immunitario in modo che favorisca il tumore. Le cellule T regolatorie – un sottogruppo di cellule T che normalmente previene infiammazioni eccessive – possono essere ampliate e attivate da infezioni virali persistenti. Segnali come le citochine immunitarie IL‑10 e TGF‑β favoriscono la moltiplicazione di queste cellule regolatorie e la loro capacità di sopprimere le cellule T “killer” vicine. In infezioni croniche come HTLV‑1, HBV e HIV, questo squilibrio crea una bolla protettiva intorno alle cellule tumorali emergenti, rendendo ancora più difficile per l’organismo montare una risposta efficace.
Nuove tattiche terapeutiche basate sui punti deboli virali
Con una comprensione più chiara di questi meccanismi, i ricercatori stanno sviluppando terapie che mirano specificamente alla macchina virale o al paesaggio immunitario distorto. Piccole molecole sono in fase di progettazione per bloccare proteine virali chiave di EBV e HTLV‑1, o addirittura segnalarle per la degradazione all’interno della cellula. Gli inibitori dei checkpoint immunitari – anticorpi che rilasciano i freni PD‑1/PD‑L1 o CTLA‑4 – sono testati in diversi linfomi correlati a virus, spesso in combinazione con chemioterapia standard. Virus oncolitici, ingegnerizzati per infettare selettivamente e far esplodere le cellule tumorali stimolando al contempo una nuova risposta immunitaria, stanno entrando nelle prime sperimentazioni cliniche. Allo stesso tempo, approcci più complessi come infusioni di cellule T specifiche per il virus, terapia CAR‑T e vaccini terapeutici mirano a ricostruire o rieducare il sistema immunitario per riconoscere bersagli virali e cellule tumorali in modo più efficace e duraturo.
Cosa significa questo per i pazienti e per le cure future
Tutto considerato, l’articolo sostiene che le neoplasie ematologiche associate a virus non sono semplicemente tumori ordinari con un virus attaccato. Sono malattie la cui esistenza dipende da una lunga lotta tra virus, cellule ematiche e sistema immunitario. Capendo esattamente come i virus aiutino le cellule tumorali a nascondersi e prosperare, i medici possono progettare combinazioni di terapie più intelligenti che bloccano le vie di fuga, risvegliano le cellule immunitarie esauste e eliminano direttamente le cellule infette da virus. Sebbene molte di queste strategie siano ancora in sperimentazione clinica, indicano un futuro in cui i pazienti con questi tumori complessi potrebbero ricevere terapie più personalizzate ed efficaci e, in alcuni casi, ottenere un controllo duraturo o addirittura la guarigione.
Citazione: Li, T., Wang, C., Xiao, Q. et al. Immune escape mechanisms and therapeutic advances in virus-associated hematological malignancies. Blood Cancer J. 16, 24 (2026). https://doi.org/10.1038/s41408-026-01453-7
Parole chiave: linfoma associato a virus, fuga immunitaria, terapia con inibitori dei checkpoint immunitari, CAR-T e terapia con cellule T, vaccini terapeutici contro il cancro