Clear Sky Science · it
L’espressione astrocitaria di APOE3-Christchurch attenua la patologia da amiloide-β nel cervello di topi 5xFAD
Perché questa variante cerebrale conta
La malattia di Alzheimer viene spesso descritta come un accumulo inarrestabile di aggregati proteici dannosi nel cervello. Eppure un piccolo numero di persone sembra sorprendentemente resistente, mantenendo funzioni cognitive intatte nonostante portino rischi genetici elevati. Questo studio si concentra su una di queste varianti protettive in un gene comune per la gestione del colesterolo, ponendosi una domanda pratica: se forniamo al cervello più di questa versione protettiva — nello specifico proveniente dalle cellule di supporto chiamate astrociti — possiamo rendere meno dannosi i cambiamenti simili all’Alzheimer?
Una variante genica protettiva sotto i riflettori
Il lavoro si concentra su una versione rara del gene APOE, denominata APOE3-Christchurch. In un caso clinico notevole, una donna portatrice di una potente mutazione responsabile di Alzheimer a esordio precoce è rimasta intellettivamente preservata per decenni in più rispetto a quanto previsto, e questa variante APOE sembra essere stata una ragione chiave. Studi precedenti sugli animali suggerivano che APOE3-Christchurch può rallentare la diffusione di un altro marcatore della malattia, la proteina tau. Ma la sua influenza sull’amiloide-beta, la proteina che forma le placche tipiche del cervello affetto da Alzheimer, non era ancora del tutto chiara. I ricercatori hanno voluto verificare come questa variante si comporti quando è espressa specificamente dagli astrociti, le cellule a forma di stella che nutrono e proteggono i neuroni.
Testare la variante in un topo simile all’Alzheimer
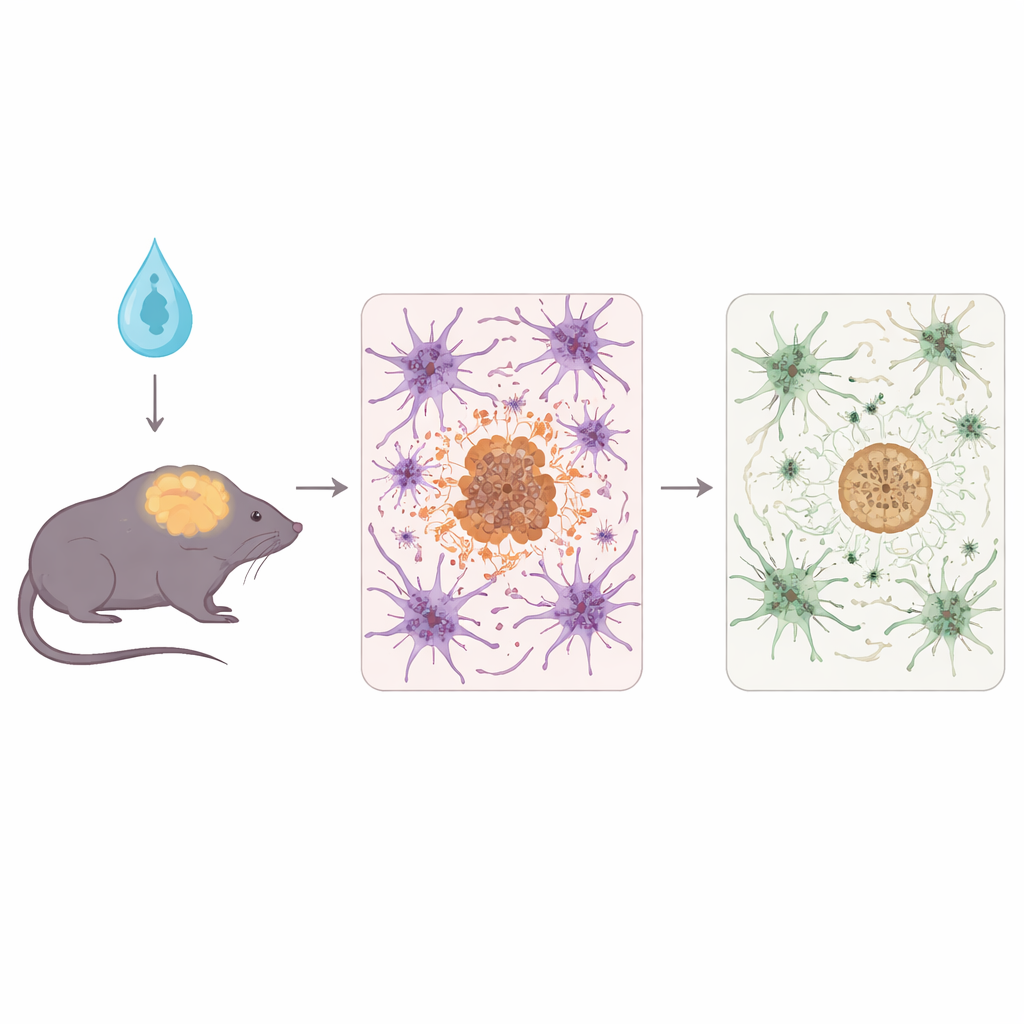
Per indagare questo aspetto, il team ha usato i topi 5xFAD, un modello ben noto che sviluppa rapidamente un forte accumulo di amiloide e danni cerebrali associati. Poco dopo la nascita, i topi hanno ricevuto un vettore virale innocuo che induceva i loro astrociti a produrre la normale APOE3 umana, la versione protettiva APOE3-Christchurch o una proteina di controllo neutra. Gli scienziati hanno quindi esaminato gli animali a uno stadio avanzato della malattia, analizzando il tessuto cerebrale con test biochimici, microscopia a fluorescenza e sequenziamento dell’RNA per valutare come fossero alterati amiloide, fibre nervose vicine e risposte immunitarie.
Rendere le placche meno tossiche, non solo meno numerose
Entrambe le forme di APOE prodotte dagli astrociti hanno ridotto il carico complessivo di placche amiloidi e i segni di danno intorno a queste placche rispetto ai controlli. Ma APOE3-Christchurch ha mostrato alcuni perfezionamenti importanti. Ha spostato l’amiloide verso placche più compatte, sferiche e fibrillari e ha abbassato i livelli di alcune forme solubili e oligomeriche di amiloide-beta — specie ritenute particolarmente tossiche per le sinapsi. I neuriti, le sottili proiezioni delle cellule nervose in prossimità delle placche, mostravano meno deformazione e lesione quando era presente APOE3-Christchurch. Parallelamente, le cellule immunitarie del cervello chiamate microglia e gli stessi astrociti erano, nel complesso, meno reattivi, e le analisi del trascrittoma hanno rivelato un attenuarsi di vie immunitarie e di stress proteico, suggerendo un ambiente più calmo e meno ostile per i neuroni.
Indizi da colture cellulari e attività genica
Per confermare che questi effetti non fossero limitati ai topi, il team ha anche impiegato astrociti derivati da cellule staminali umane ingegnerizzate per portare o APOE3 o la variante Christchurch. Gli astrociti con APOE3-Christchurch hanno secreto più proteina APOE e il loro mezzo condizionato ha ridotto la formazione di oligomeri di amiloide-beta in un sistema sperimentale controllato in provetta. Nei cervelli dei topi, l’espressione di APOE3-Christchurch ha modificato reti geniche coinvolte nel ripiegamento proteico, nello stress cellulare e nella segnalazione immunitaria, e ha ridotto i livelli di proteine legate alle risposte di stress e alla gestione lipidica disordinata. Nel complesso, queste linee di evidenza suggeriscono che APOE3-Christchurch non si limita a cambiare la quantità di amiloide: ne altera la forma e la reazione delle cellule cerebrali ad essa.
Cosa potrebbe significare per futuri trattamenti
Pur essendo gli effetti protettivi osservati qui modesti piuttosto che miracolosi, risultano altamente informativi. Lo studio mostra che potenziare APOE3-Christchurch specificamente negli astrociti può rendere i depositi di amiloide più compatti e apparentemente meno tossici, ridurre il danno nervoso vicino e ridurre i segnali infiammatori e di stress, anche senza eliminare completamente l’amiloide. Per il lettore non specialistico, il messaggio chiave è che non tutte le placche sono ugualmente dannose: rimodellarle e neutralizzarle può essere importante tanto quanto rimuoverle. Questi risultati supportano l’idea che terapie ispirate ad APOE3-Christchurch — forse somministrate tramite terapia genica o con farmaci che ne imitino il comportamento — potrebbero aiutare il cervello a convivere più serenamente con l’amiloide e, potenzialmente, rallentare o attenuare l’evoluzione della malattia di Alzheimer.
Citazione: Raulin, AC., Alnobani, A., Rodriguez-Martinez, P. et al. Astrocytic APOE3-Christchurch expression ameliorates brain amyloid-β pathology in 5xFAD mice. Transl Psychiatry 16, 224 (2026). https://doi.org/10.1038/s41398-026-04002-9
Parole chiave: Malattia di Alzheimer, APOE3-Christchurch, amiloide-beta, astrociti, terapia genica