Clear Sky Science · it
MicroRNA-132/212 modula negativamente la ricompensa da oppioidi colpendo il trasportatore della dopamina nell’area tegmentale ventrale
Perché questa ricerca conta nella vita quotidiana
Gli antidolorifici oppioidi e farmaci correlati possono alleviare il dolore ma comportano anche un serio rischio di dipendenza. Questo studio esplora i meccanismi del sistema di ricompensa cerebrale per identificare piccoli interruttori genetici che influenzano quanto intensamente gli oppioidi risultino gratificanti. Comprendendo questi interruttori, gli scienziati sperano di progettare terapie più intelligenti che allevino il dolore o limitino la dipendenza senza dirottare i circuiti del piacere del cervello.
Piccole molecole con grande influenza
Il nostro cervello si affida a una sostanza chimica chiamata dopamina per segnalare il piacere e motivarci a cercare esperienze gratificanti, dal cibo gustoso alle droghe che creano dipendenza. Forza e durata di questo segnale sono controllate in parte da una proteina chiamata trasportatore della dopamina, che agisce come un aspirapolvere, risucchiando la dopamina nelle cellule nervose. Gli autori si sono concentrati su due pezzi molto piccoli di materiale genetico, microRNA-132 e microRNA-212, che possono ridurre la produzione di proteine specifiche. Studi precedenti avevano collegato questi microRNA all’uso di cocaina e allo stress. Qui il gruppo ha chiesto se essi influenzino anche la risposta cerebrale agli oppioidi, in particolare alla morfina.
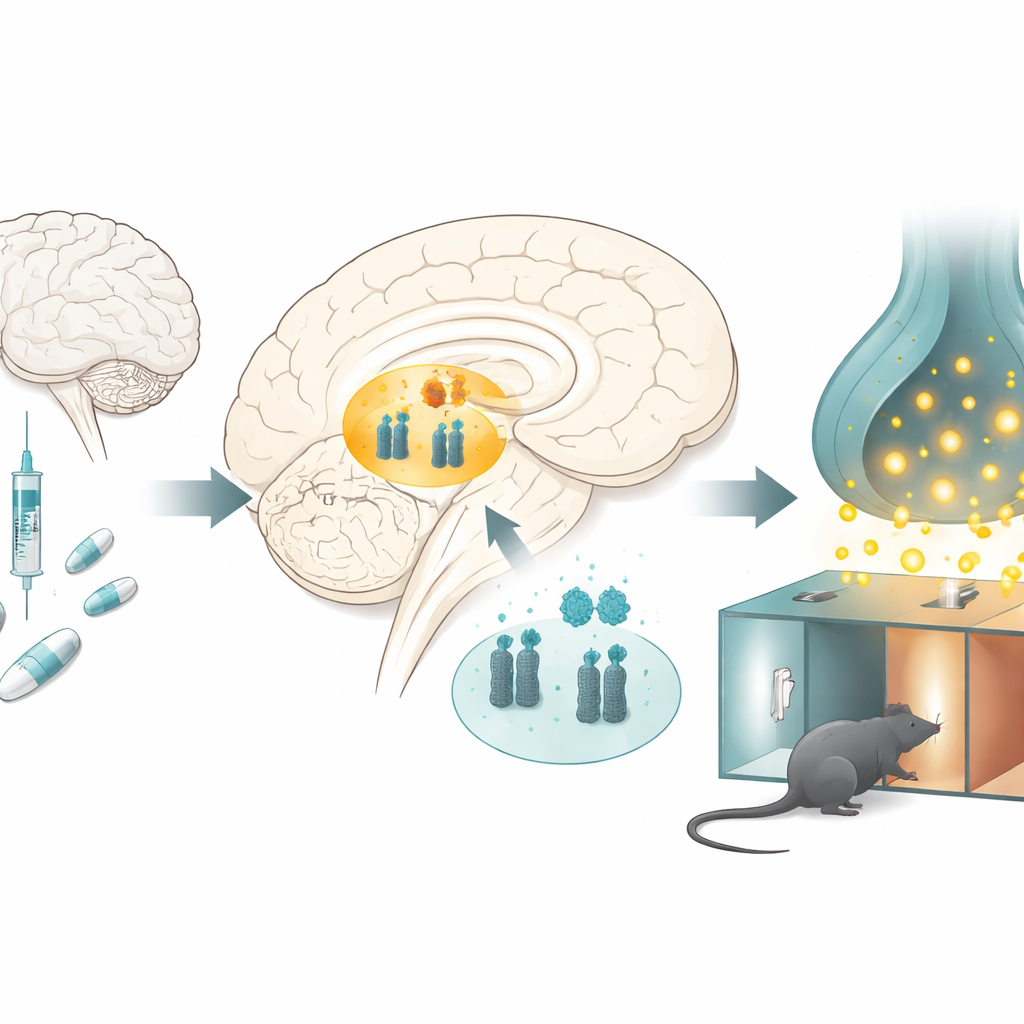
Come gli oppioidi cambiano il centro della ricompensa cerebrale
I ricercatori hanno studiato ratti sottoposti a dosi ripetute di morfina in un classico test della ricompensa, in cui gli animali imparano a preferire una stanza associata al farmaco. Dopo diversi giorni, i ratti trattati con morfina trascorrevano più tempo nella camera associata alla morfina, mostrando che la droga era diventata gratificante. Quando gli scienziati hanno esaminato una regione chiave della ricompensa profonda nel cervello, l’area tegmentale ventrale, hanno trovato uno schema netto: i livelli di microRNA-132 e microRNA-212 erano ridotti, mentre i livelli del trasportatore della dopamina erano aumentati. Cambiamenti simili sono comparsi anche quando i ratti ricevevano morfina senza il compito di apprendimento contestuale, suggerendo che l’esposizione cronica alla droga di per sé sposti questo equilibrio molecolare.
Individuare un collegamento molecolare diretto
Per verificare se questi microRNA controllano effettivamente il trasportatore della dopamina, il team ha utilizzato cellule umane di tipo nervoso in coltura. Potenziando artificialmente microRNA-132 o microRNA-212, hanno osservato una diminuzione sia del messaggio genetico sia della proteina del trasportatore. L’inibizione dei microRNA ha provocato l’effetto opposto. Hanno poi costruito un costrutto reporter in cui un enzima che produce luce era legato alla coda regolatoria del trasportatore. L’aggiunta dei microRNA ha attenuato il segnale luminoso, ma questo effetto è scomparso quando poche basi chiave nel sito di legame sono state mutate. Nel complesso, questi esperimenti dimostrano che microRNA-132 e microRNA-212 si legano direttamente al messaggio del trasportatore e ne sopprimono la produzione.
Dalle molecole ai livelli di dopamina e al comportamento
Successivamente i ricercatori hanno chiesto come questo controllo molecolare si manifesti nelle cellule cerebrali vive. In neuroni coltivati, l’aumento dei microRNA riduceva la captazione della dopamina, mentre il loro blocco aumentava la rimozione della dopamina. Quando hanno aumentato o diminuito artificialmente i livelli del trasportatore della dopamina, l’influenza dei microRNA è salita o scesa di conseguenza, confermando che il trasportatore è il principale mediatore. Nei ratti viventi, potenziare microRNA-132 nell’area tegmentale ventrale ha aumentato i livelli di dopamina che si riversavano nelle regioni connesse, riflettendo una minore attività del trasportatore. A livello comportamentale, usare strumenti virali per assorbire ("sponge") microRNA-132 o microRNA-212 in questa regione cerebrale ha reso i ratti più inclini ad apprendere una preferenza per la morfina, insieme a livelli più alti del trasportatore. Al contrario, forzare l’espressione di microRNA-132 nella stessa area ha ridotto i livelli del trasportatore e attenuato la preferenza per la morfina in animali maschi, femmine e adolescenti, senza influenzare il movimento o il godimento di ricompense naturali come l’acqua zuccherata.
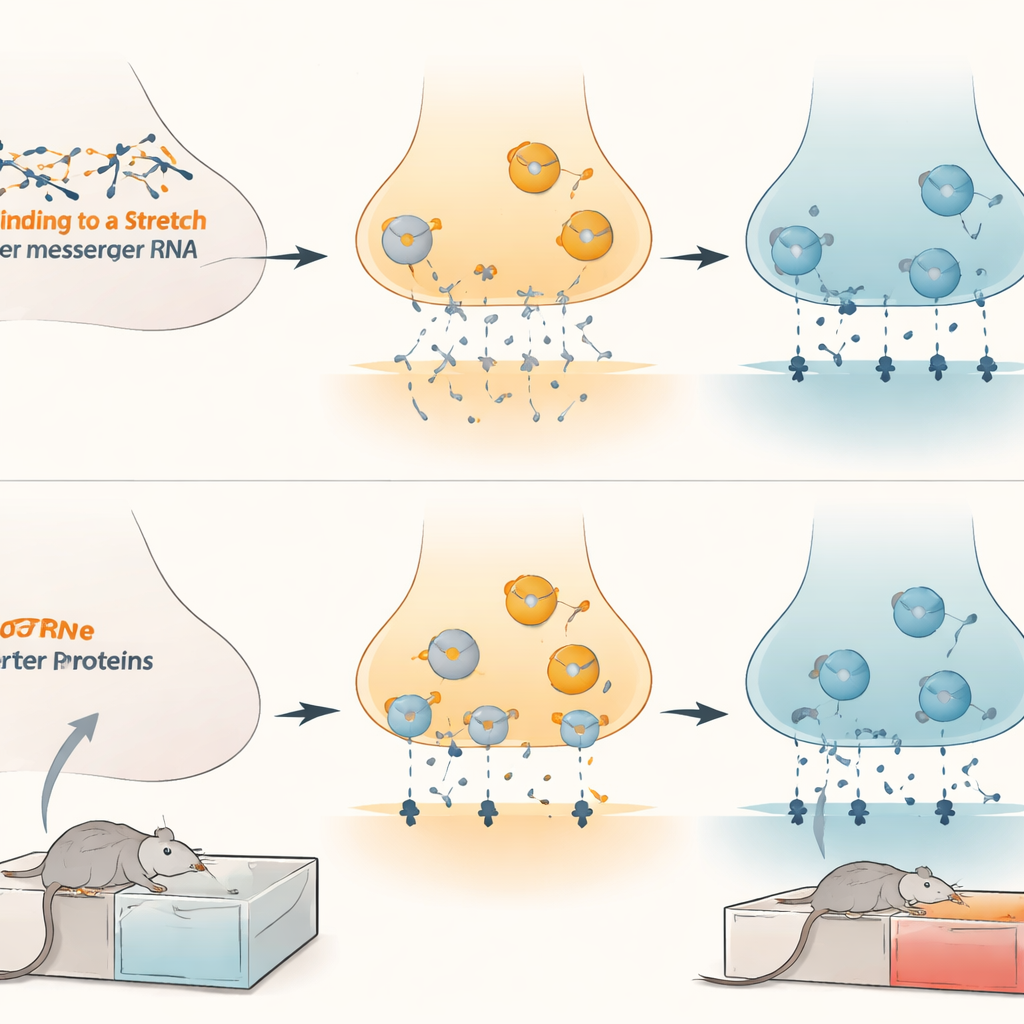
Implicazioni per il trattamento della dipendenza da oppioidi
Questi risultati rivelano un sistema di freno finemente regolato all’interno del circuito della ricompensa cerebrale: microRNA-132 e microRNA-212 tengono sotto controllo il trasportatore della dopamina, modellando quanto intensamente gli oppioidi siano percepiti come gratificanti. La morfina cronica sembra sollevare questo freno abbassando i livelli dei microRNA, permettendo al trasportatore di aumentare e contribuendo a consolidare i segnali di ricompensa associati alla droga. Ripristinare o imitare l’azione di questi microRNA specificamente nell’area tegmentale ventrale potrebbe attenuare la presa della ricompensa da oppioidi senza deprimere in modo generalizzato il piacere o il movimento. Sebbene rimanga molto lavoro prima che tali strategie possano essere testate nell’uomo, questo studio indica una nuova strada altamente mirata per futuri trattamenti che affrontino la dipendenza a livello delle regolazioni molecolari intrinseche del cervello.
Citazione: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Parole chiave: dipendenza da oppioidi, trasportatore della dopamina, microRNA-132, area tegmentale ventrale, ricompensa da morfina