Clear Sky Science · it
Basse concentrazioni di oligomeri di amiloide‑beta inducono sinaptogenesi caratteristica del lieve deterioramento cognitivo e alterano il proteoma de novo
Primi cambiamenti che possono segnalare problemi di memoria
Prima che la malattia di Alzheimer privi le persone della memoria, il cervello attraversa una fase intermedia sfumata nota come lieve deterioramento cognitivo. In questa fase i problemi cognitivi sono percettibili ma la vita quotidiana spesso prosegue. In modo paradossale, alcune regioni cerebrali mostrano in questo stadio più, e non meno, connessioni tra i neuroni. Questo studio indaga se piccole quantità di una molecola tossica legata all’Alzheimer possano guidare questa ondata di nuove connessioni e se un farmaco già sperimentato in pazienti oncologici possa attenuare questi cambiamenti molto precoci.
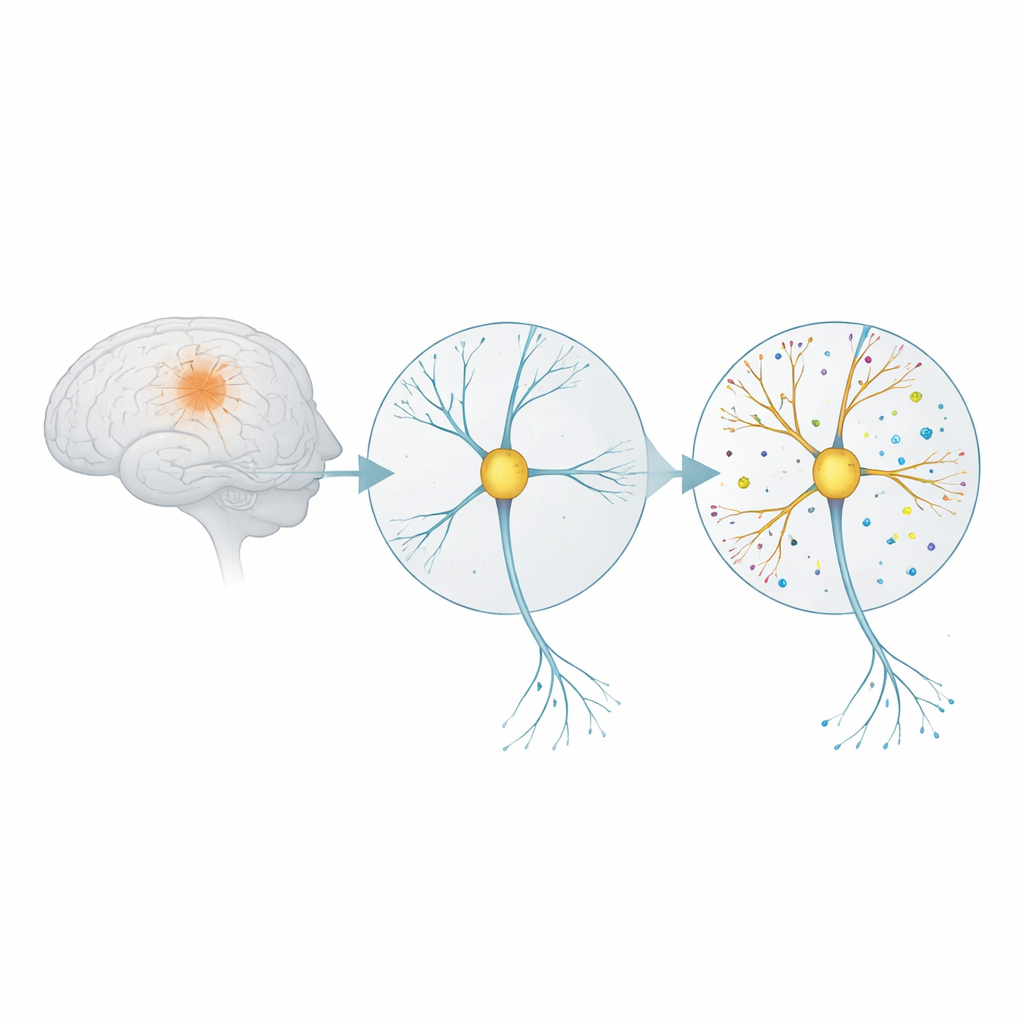
Come reagiscono le connessioni cerebrali a un fattore tossico
La malattia di Alzheimer è strettamente associata a piccoli aggregati di un frammento proteico chiamato amiloide‑beta. Nella sua forma di oligomero, questo frammento è particolarmente dannoso per le sinapsi — i punti di contatto attraverso cui i neuroni comunicano. I ricercatori hanno coltivato cellule cerebrali di ratto in coltura fino a formare reti mature, quindi le hanno esposte per cinque giorni a una bassa dose di oligomeri di amiloide‑beta. Hanno inoltre valutato cosa succedeva aggiungendo un composto chiamato eFT508, che blocca un enzima di segnalazione (MNK) coinvolto nell’avvio della produzione proteica nelle cellule. Questo assetto è stato pensato per imitare gli stadi molto precoci della malattia, prima che si verifichi una morte cellulare diffusa.
Osservare dettagli nascosti delle nuove sinapsi
Per esaminare come cambiavano le connessioni, il team ha utilizzato la “microscopia di espansione”, una tecnica che gonfia fisicamente le cellule fissate in un gel morbido in modo che le strutture minute siano visibili con maggior dettaglio. Hanno marcato le fibre nervose e entrambi i lati della sinapsi con sonde fluorescenti e le hanno ricostruite in 3D. L’esposizione all’amiloide‑beta ha provocato un evidente incremento del numero di sinapsi lungo i rami dei neuroni. In particolare si osservava un aumento delle singole bouton — contatti semplici uno a uno — e di spine “multi‑innervate” poco comuni, dove più fibre entranti convergono su un singolo sito ricevente. Questi schemi assomigliano agli aumenti sinaptici riportati in persone con lieve deterioramento cognitivo. In presenza di eFT508, il numero di sinapsi è tornato verso valori normali, suggerendo che il farmaco potrebbe contrastare questa iper‑crescita iniziale.
Le nuove proteine cambiano, anche quando il totale non varia
Le sinapsi si rimodellano costantemente producendo e degradando proteine. Il gruppo ha quindi analizzato quali proteine venivano sintetizzate di novo durante e dopo l’esposizione all’amiloide‑beta. Hanno fornito ai neuroni un amminoacido artificiale innocuo che viene incorporato nelle proteine appena sintetizzate, quindi hanno usato reazioni chimiche “click” e spettrometria di massa per estrarre e identificare queste molecole. Sorprendentemente, la quantità totale di nuova proteina prodotta non è cambiata dopo diversi giorni di amiloide‑beta a bassa dose, né con né senza eFT508. Ma esaminando quali proteine specifiche venivano sintetizzate, il quadro era molto diverso: sono state rilevate oltre mille proteine neo‑sintetizzate e molte decine di esse sono aumentate o diminuite in risposta all’amiloide‑beta. Molte erano coinvolte nella comunicazione sinaptica, nell’impalcatura interna della cellula, nei mitocondri produttori di energia, nei sistemi di smaltimento dei rifiuti e nel controllo della qualità proteica.
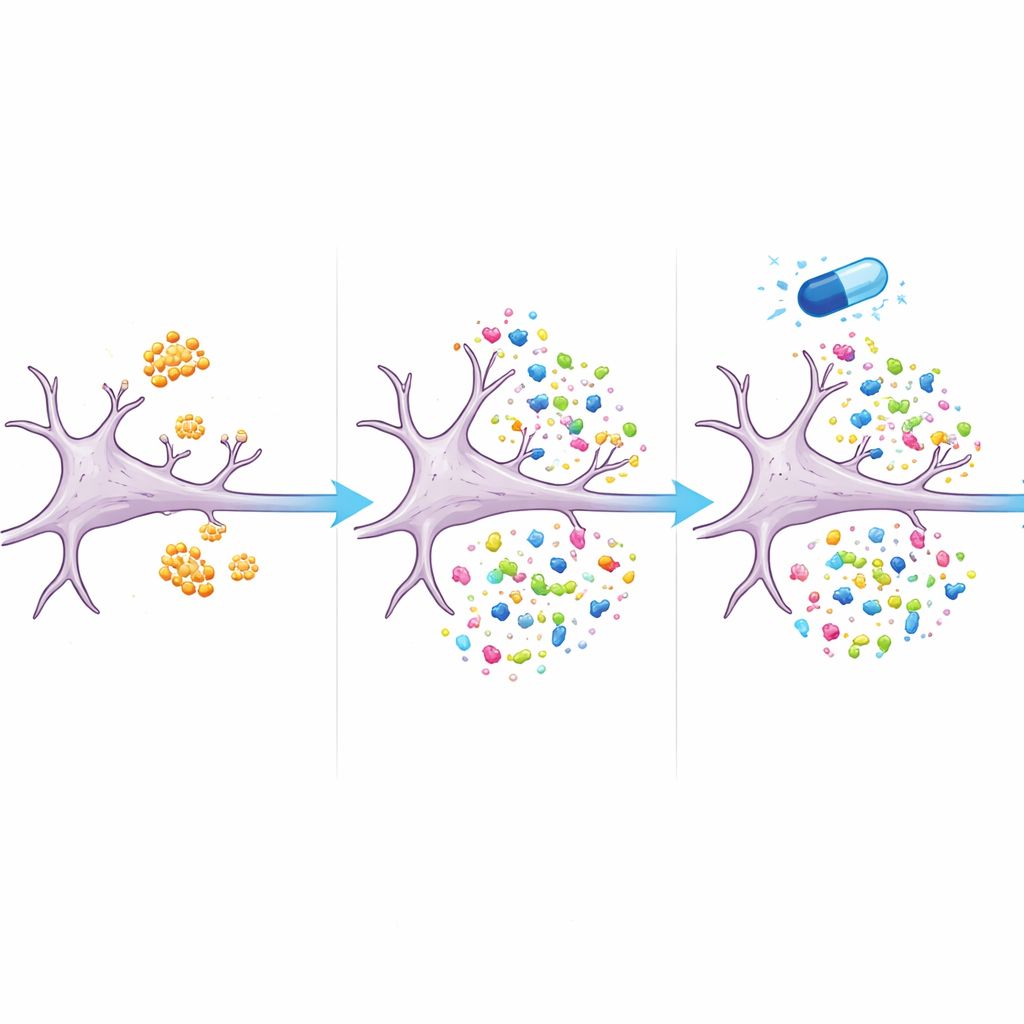
Un farmaco che rimodula l’equilibrio proteico
Elemento cruciale: molte delle proteine disturbate sono tornate verso livelli normali quando le cellule sono state trattate con eFT508 insieme all’amiloide‑beta. Più di due terzi delle proteine alterate dall’amiloide‑beta da sola non risultavano più significativamente diverse dalle cellule non trattate in presenza del farmaco. Tra queste c’erano proteine legate alla struttura e alla funzione sinaptica, così come componenti dei sistemi cellulari di riciclo ed energetici. I risultati suggeriscono che eFT508 non si limita a spegnere la sintesi proteica; appare piuttosto in grado di rimodellare quali proteine vengono prodotte, spostando il sistema lontano da un profilo simile all’Alzheimer verso un equilibrio più sano.
Che cosa potrebbe significare per i trattamenti futuri
Questo lavoro delinea i danni legati all’Alzheimer nelle fasi iniziali come una fase di iper‑connessione e sottile disgestione proteica piuttosto che una perdita netta. Basse concentrazioni di amiloide‑beta promuovono la formazione di sinapsi extra, talvolta insolite, e alterano selettivamente il repertorio di proteine che i neuroni producono. In questo modello in coltura, eFT508 può sia normalizzare il numero di sinapsi sia correggere molte delle alterazioni proteiche, suggerendo che un’aggiustata regolazione della sintesi proteica potrebbe rallentare o prevenire la progressione dal lieve deterioramento cognitivo alla demenza conclamata. Sebbene resti molto da verificare in animali vivi e negli esseri umani, lo studio mette in luce un nuovo modo di pensare — e forse di intervenire — nelle fasi più precoci della malattia di Alzheimer.
Citazione: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
Parole chiave: Malattia di Alzheimer, cambiamenti sinaptici, oligomeri di amiloide beta, sintesi proteica, neurodegenerazione precoce