Clear Sky Science · it
Mappare sottotipi strutturali eterogenei del cervello nella malattia di Alzheimer e nel deterioramento cognitivo lieve usando modelli normativi
Perché questa ricerca è importante per la salute del cervello
La malattia di Alzheimer e la sua fase di avvertimento precoce, il deterioramento cognitivo lieve, non si manifestano allo stesso modo in tutti i pazienti. Alcune persone peggiorano rapidamente, altre più lentamente; alcune mostrano una notevole atrofia cerebrale, altre molto meno. Questo studio pone una domanda pratica con grandi implicazioni per famiglie e medici: è possibile usare le immagini cerebrali per mappare in modo sistematico queste differenze individuali, così da identificare chi è su un percorso più aggressivo e adattare di conseguenza le cure?
Confrontare ogni cervello con una “tabella di crescita”
Invece di confrontare semplicemente i pazienti con Alzheimer con un gruppo di controllo, i ricercatori hanno costruito qualcosa di simile alle tabelle di crescita pediatriche, ma per il cervello. Utilizzando scansioni MRI di oltre mille adulti sani di età compresa tra 18 e 92 anni, hanno modellato come il volume della materia grigia in 90 regioni cerebrali cambia normalmente con l’età in uomini e donne. Questo “modello normativo” definisce l’intervallo atteso per ciascuna regione a una data età e sesso. Poi, per ogni persona inclusa nei grandi dataset sulla malattia di Alzheimer, hanno calcolato quanto i volumi cerebrali individuali si discostassero da quanto sarebbe tipico, regione per regione. Il risultato è una mappa personalizzata che mostra dove il cervello è insolitamente ridotto o preservato per quella fase della vita.
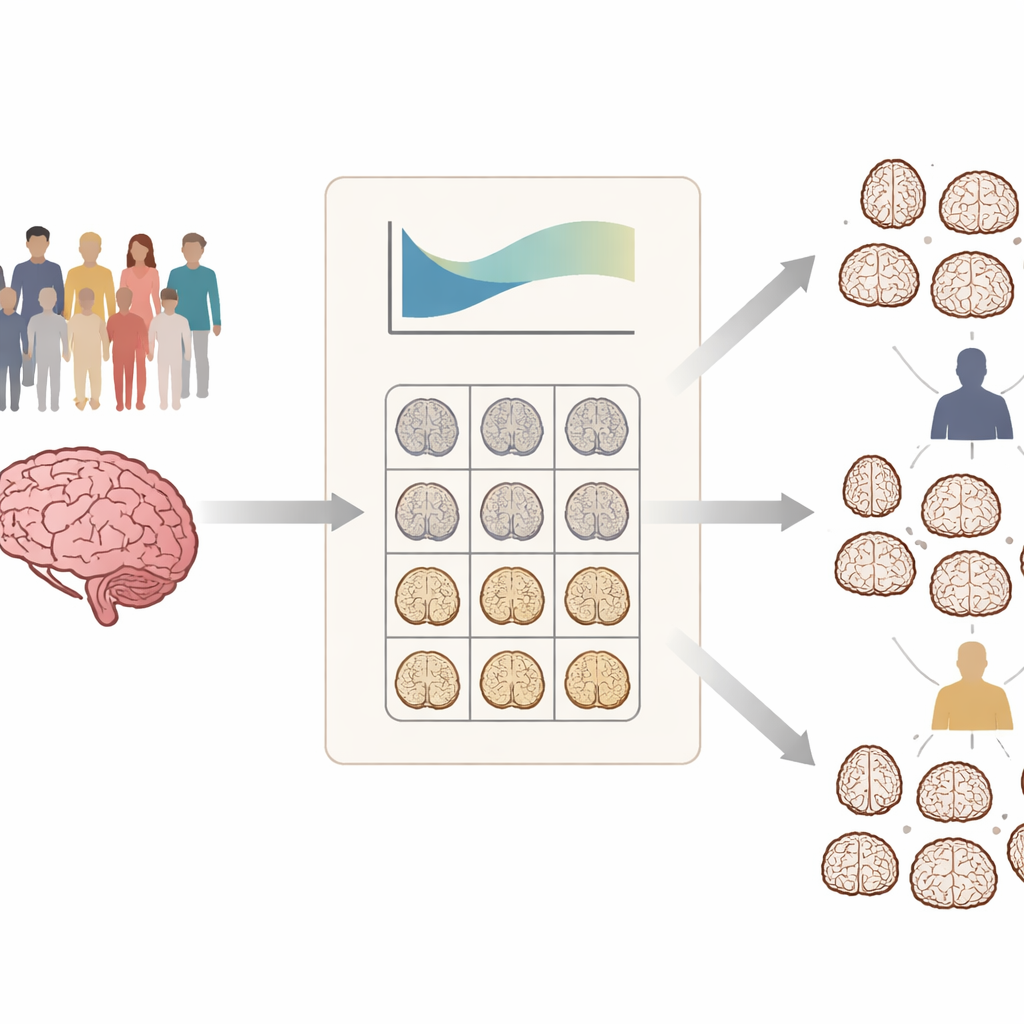
Due principali modelli di cambiamento cerebrale nei pazienti
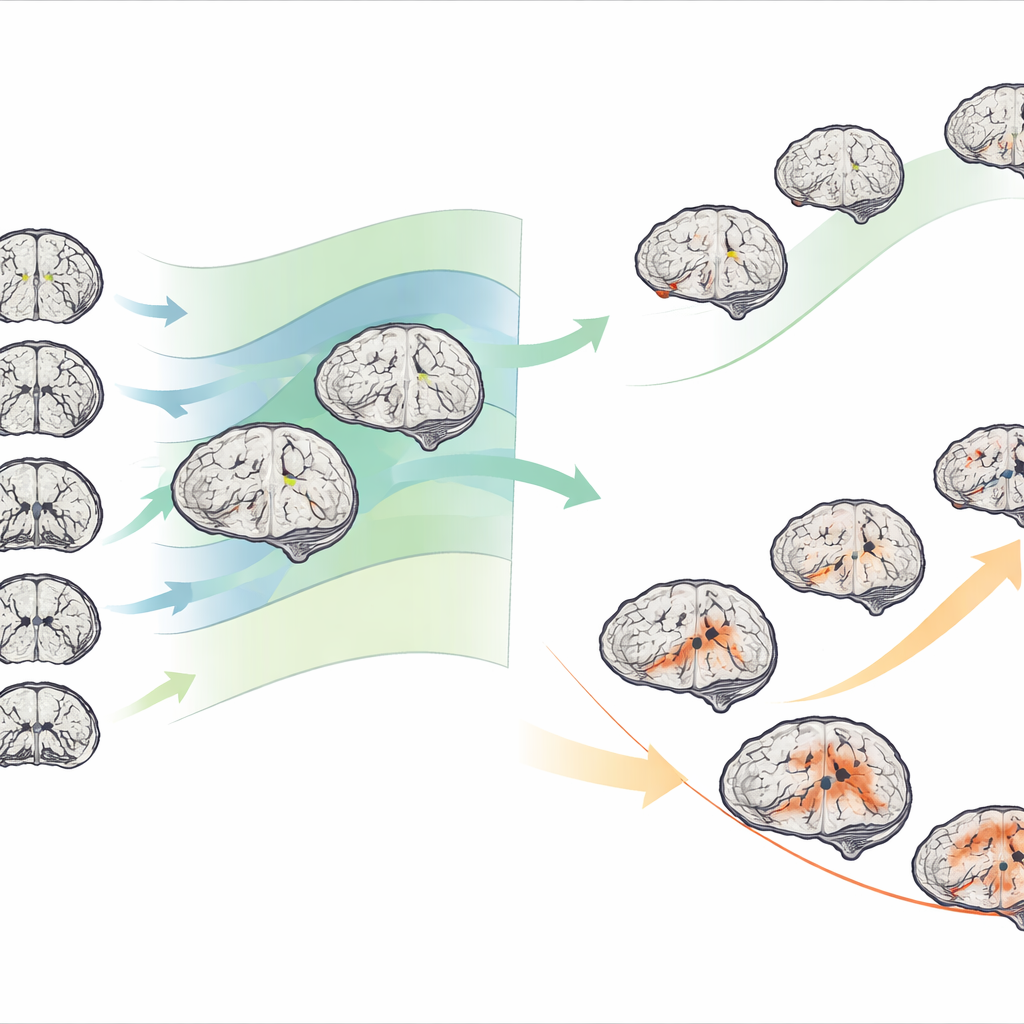
Quando il team ha applicato questo approccio a centinaia di persone con deterioramento cognitivo lieve e malattia di Alzheimer, ha rilevato un’ampia variabilità: non tutti i pazienti mostravano le stesse aree di atrofia e la gravità variava notevolmente. Raggruppando le persone in base alle loro mappe di deviazione, hanno identificato in modo consistente due sottotipi strutturali in entrambe le condizioni. Un sottotipo mostrava scostamenti relativamente lievi dalla norma, mentre l’altro mostrava deviazioni negative molto più marcate, specialmente in strutture profonde legate alla memoria come l’ippocampo, la regione parahippocampale e l’amigdala. Questi cervelli con “deviazioni severe” risultavano chiaramente più atrofici del previsto per età e sesso in molte regioni.
Collegare i modelli cerebrali al pensiero, ai marker e alla progressione
I sottotipi strutturali non erano solo pattern astratti su una scansione; rispecchiavano strettamente differenze cliniche nel mondo reale. Le persone nel sottotipo severo ottenevano punteggi peggiori nei test di memoria e funzione cognitiva, mostravano un metabolismo cerebrale più basso nelle immagini PET e avevano maggior probabilità di presentare livelli anomali di proteine correlate all’Alzheimer nel liquido cerebrospinale. Nel corso di anni di follow-up, declinavano anche più rapidamente nelle scale cognitive standard. Tra coloro con deterioramento cognitivo lieve, il sottotipo severo aveva un rischio più alto di conversione alla malattia di Alzheimer conclamata e avveniva più rapidamente. È importante che gli individui tendevano a mantenere il loro sottotipo durante la progressione: i pazienti che iniziavano nel gruppo strutturalmente più lieve solitamente evolvevano verso un pattern di Alzheimer più lieve, mentre quelli nel gruppo più danneggiato tendevano per lo più a spostarsi nel sottotipo di Alzheimer più aggressivo.
Dalle mappe cerebrali alla biologia sottostante
Per indagare perché questi pattern differissero, gli autori hanno confrontato le mappe regionali di atrofia con dettagliate mappe di attività genica provenienti da cervelli umani donati. Hanno riscontrato che le aree più colpite in ciascun sottotipo tendevano a esprimere particolari insiemi di geni coinvolti nelle connessioni e nella comunicazione dei neuroni, e in tipi cellulari associati ai vasi sanguigni e alla mielina. Il sottotipo severo mostrava legami particolarmente forti con geni relativi alle proiezioni neuronali e alle sinapsi, suggerendo che il deterioramento di questi sistemi potrebbe guidare il suo decorso più aggressivo. Hanno anche confermato che le persone portatrici della variante genetica di rischio APOE ε4 tendevano ad avere deviazioni negative più marcate e un declino strutturale più rapido, in particolare nella fase di deterioramento cognitivo lieve.
Verso cure più personalizzate per l’Alzheimer
Nel complesso, lo studio mostra che un confronto accurato del cervello di ciascuna persona con un intervallo “normale” ben caratterizzato può rivelare sottotipi significativi della malattia di Alzheimer e del deterioramento cognitivo lieve. Questi sottotipi differiscono nella struttura cerebrale, nelle capacità cognitive, nei marker della malattia e nella velocità di progressione, e sembrano essere radicati in firme molecolari distinte. Per pazienti e clinici, ciò suggerisce che strumenti diagnostici futuri potrebbero usare tali mappe cerebrali individualizzate per individuare precocemente gli individui ad alto rischio, scegliere programmi di monitoraggio o trattamenti sperimentali più appropriati e progettare studi che raggruppino i partecipanti per sottotipo biologico anziché per ampia diagnosi.
Citazione: Wei, X., Zhang, T., Xiong, R. et al. Mapping heterogeneous brain structural subtypes in alzheimer’s disease and mild cognitive impairment using normative models. Transl Psychiatry 16, 168 (2026). https://doi.org/10.1038/s41398-026-03902-0
Parole chiave: Malattia di Alzheimer, deterioramento cognitivo lieve, risonanza magnetica cerebrale, modellizzazione normativa, neurologia personalizzata