Clear Sky Science · it
Effetti prenatali e postnatali dell’attivazione immunitaria gestazionale su vie sinaptiche e neuroevolutive tramite meccanismi epigenetici
Come il sistema immunitario materno modella il cervello del bambino
Le infezioni durante la gravidanza sono da tempo associate a un rischio aumentato di condizioni come la schizofrenia, l’autismo e l’ADHD nei figli, ma il “ponte” biologico tra una madre malata e un cervello suscettibile in età adulta è rimasto poco chiaro. Questo studio utilizza topi per mostrare come la risposta immunitaria materna all’influenza in gravidanza possa lasciare segni chimici duraturi sul cervello in sviluppo, modificando il modo in cui le cellule cerebrali comunicano e potenzialmente aumentando il rischio di problemi neurologici e di salute mentale in seguito.
Malattia in gravidanza e rischio cerebrale per tutta la vita
Studi epidemiologici sull’uomo hanno mostrato che quando le donne in gravidanza subiscono infezioni, i loro figli hanno maggior probabilità di sviluppare una serie di disturbi psichiatrici e neuroevolutivi in età adulta. Gli autori si concentrano sull’attivazione immunitaria materna, la cascata di segnali immunitari rilasciati quando l’organismo combatte un’infezione. Questi segnali possono attraversare o influenzare la placenta e interagire con il cervello in sviluppo in un momento in cui si stanno formando i circuiti. La corteccia frontale — fondamentale per la pianificazione, la presa di decisioni e il controllo emotivo — si sviluppa per un lungo periodo ed è particolarmente sensibile alle alterazioni precoci.
Dissezionare gli effetti prenatali e postnatali
Per separare ciò che avviene nell’utero da ciò che avviene dopo la nascita, i ricercatori hanno infettato topi gravidi con un virus influenzale lieve e non letale durante una fase precoce della gestazione equivalente alla fine del primo trimestre umano. Alcuni cuccioli sono rimasti con le madri biologiche, mentre altri sono stati allattati da madri surrogate entro 24 ore dalla nascita. Questo ha creato quattro gruppi: prole senza esposizione prima o dopo la nascita, esposta solo prima della nascita, solo dopo la nascita, o in entrambi i periodi. Quando la prole ha raggiunto l’età adulta, il team ha esaminato neuroni della corteccia frontale, valutando sia l’attività genica sia i “segni epigenetici” — tag chimici sulle proteine che impacchettano il DNA che aiutano a controllare quali geni sono attivi o inattivi. 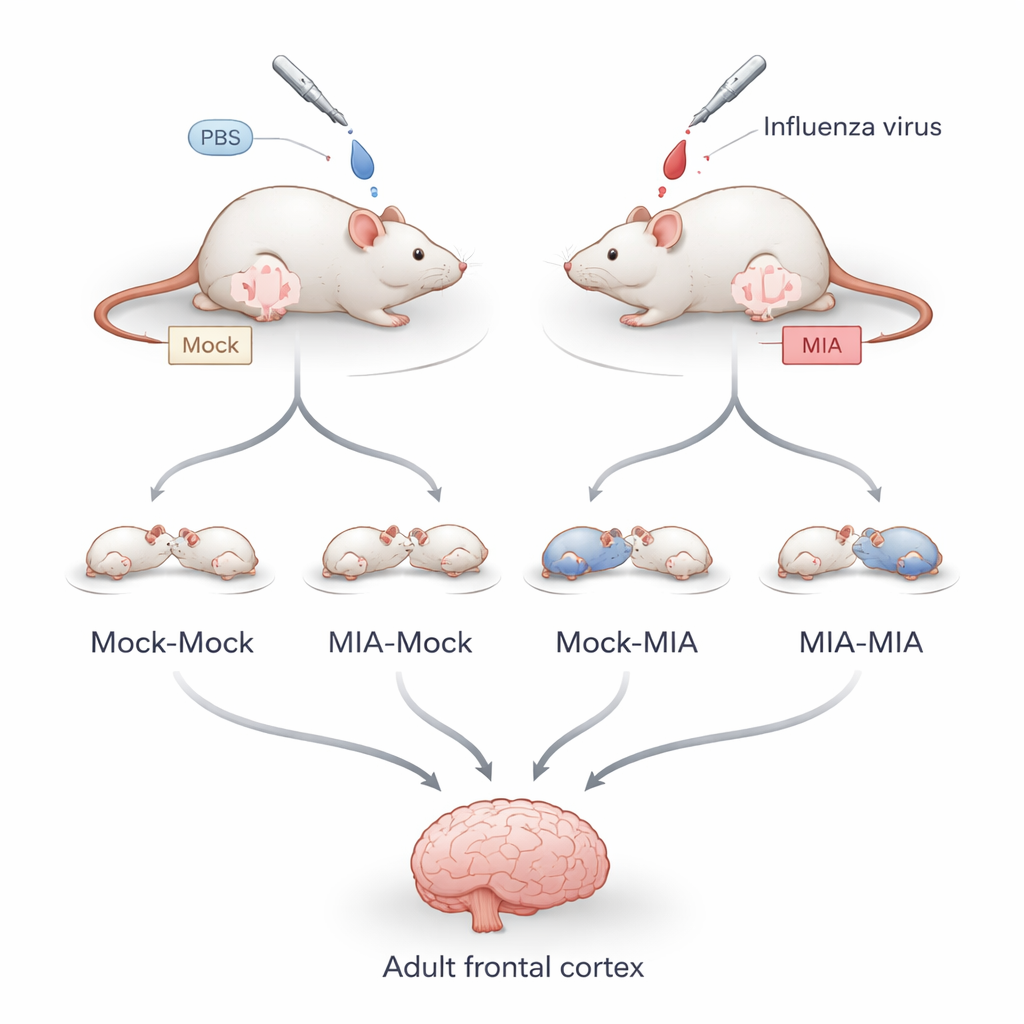
Segni chimici duraturi sul DNA cerebrale
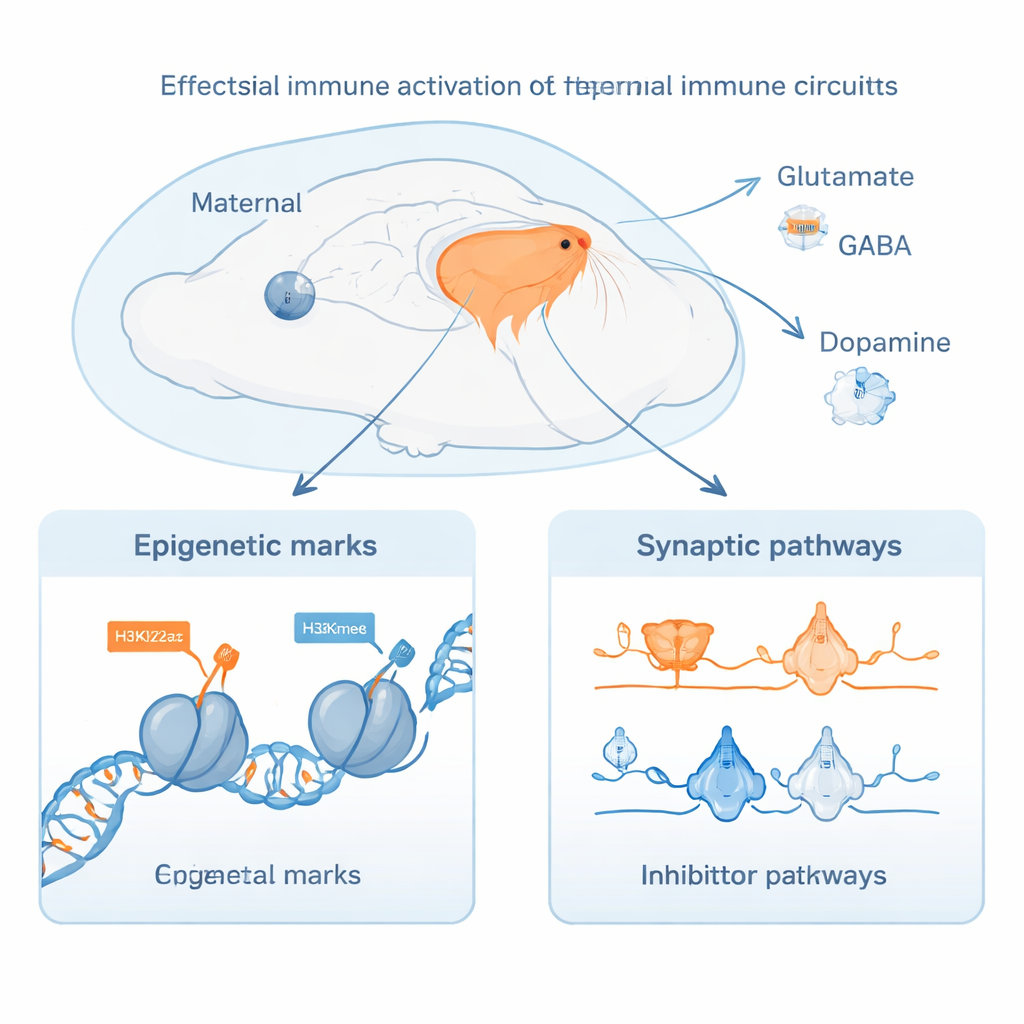
Lo studio si è concentrato su due marche istoniche, H3K27ac e H3K4me3, che segnalano interruttori attivi e punti di avvio per i geni. Utilizzando metodi di sequenziamento sensibili, gli autori hanno mappato decine di migliaia di queste regioni regolatorie e misurato quali geni erano più o meno attivi in ciascun gruppo. Hanno scoperto che l’attivazione immunitaria materna prima della nascita produceva cambiamenti diffusi e persistenti nelle regioni enhancer — tratti di DNA che funzionano come manopole di controllo per l’attività genica. Queste modificazioni erano particolarmente arricchite nei geni coinvolti nella costruzione del prosencefalo, nell’orientamento delle fibre nervose in crescita e nell’istituzione dei primi punti di comunicazione tra neuroni. Molti degli stessi geni mostravano anche attività alterata dopo la nascita quando i cuccioli erano allevati da madri con attivazione immunitaria, indicando una traiettoria regolatoria sostenuta attraverso lo sviluppo piuttosto che uno shock di breve durata.
Dai cambiamenti epigenetici alle alterazioni di sinapsi e circuiti
Sia l’esposizione prenatale sia quella postnatale hanno influenzato vie molecolari che governano come i neuroni si segnalano tra loro. I geni legati al glutammato (il principale neurotrasmettitore eccitatorio), al GABA (il principale neurotrasmettitore inibitorio) e alla dopamina (importante per motivazione e ricompensa) hanno mostrato cambiamenti coordinati nei loro elementi regolatori e nei livelli di espressione. Questi sistemi sono ripetutamente implicati in schizofrenia, depressione, autismo e dipendenza. Gli autori hanno inoltre riscontrato che geni coinvolti nell’organizzazione delle sinapsi, nella crescita dell’assone e nel raffinamento dei circuiti cerebrali erano alterati, in particolare dall’esposizione postnatale, suggerendo che il comportamento materno e i cambiamenti immunitari in corso dopo la nascita contribuiscono a modellare come le reti neurali vengono cablate e regolate. Le analisi di rete hanno evidenziato un nucleo di fattori di trascrizione — regolatori principali dell’attività genica — che risultavano perturbati in entrambe le finestre temporali.
Collegamenti con il rischio psichiatrico umano
Per verificare quanto questi cambiamenti nei topi siano rilevanti per la malattia umana, il team ha convertito le posizioni enhancer e promotrici dei topi nei loro più prossimi corrispettivi umani e le ha confrontate con grandi studi genetici sui disturbi psichiatrici. Le regioni alterate dall’attivazione immunitaria materna risultavano fortemente arricchite in loci di rischio umano per schizofrenia, disturbo bipolare, depressione, nevroticismo e ADHD, ma non nella maggior parte delle condizioni non psichiatriche. Questo schema suggerisce che gli stessi tipi di regioni regolatorie del DNA che portano rischio genetico ereditario per le malattie mentali sono anche sensibili alle sfide immunitarie durante la gravidanza e la prima infanzia, costituendo un punto di convergenza tra geni e ambiente.
Cosa significa per la salute umana
Per un lettore non specialista, il messaggio chiave è che la risposta immunitaria della madre — non solo l’infezione in sé — può lasciare “note ai margini” durature nel manuale di istruzioni del cervello in sviluppo. Queste note epigenetiche, scritte prima e subito dopo la nascita, possono alterare sottilmente come le cellule cerebrali crescono e comunicano tra loro nei circuiti che regolano pensiero, umore e comportamento. Sebbene la maggior parte dei bambini di madri malate non svilupperà disturbi psichiatrici, questo lavoro aiuta a spiegare perché alcuni possono essere più vulnerabili e sottolinea l’importanza di prevenire e gestire infezioni e infiammazione durante la gravidanza e la prima infanzia come parte della salute cerebrale a lungo termine.
Citazione: Zhu, B., Li, G., Saunders, J.M. et al. Prenatal and postnatal effects of gestational immune activation on synaptic and neurodevelopmental pathways via epigenetic mechanisms. Transl Psychiatry 16, 82 (2026). https://doi.org/10.1038/s41398-026-03884-z
Parole chiave: attivazione immunitaria materna, epigenetica, neuroevoluzione, segnalazione sinaptica, rischio psichiatrico