Clear Sky Science · it
La modifica m6A mediata da METTL3 regola CDKN1A per attenuare il deficit cognitivo e l’apoptosi neuronale indotti dalla privazione cronica del sonno nei ratti
Perché le notti insonni possono danneggiare la memoria
Molti minimizzano la perdita cronica di sonno come parte normale della vita moderna, ma la ricerca sta rivelando che la mancanza di riposo può danneggiare in modo silenzioso le aree cerebrali che supportano l’apprendimento e la memoria. Questo studio sui ratti scava fino al livello delle singole molecole nei neuroni dell’ippocampo e identifica un interruttore chimico specifico — chiamato METTL3 — che sembra proteggere le cellule cerebrali dagli effetti nocivi della privazione cronica del sonno. Comprendere questo interruttore potrebbe eventualmente indicare nuove strategie per proteggere la memoria in persone che non possono facilmente evitare la perdita di sonno, come lavoratori a turni, persone che assistono altri e pazienti con disturbi del sonno.
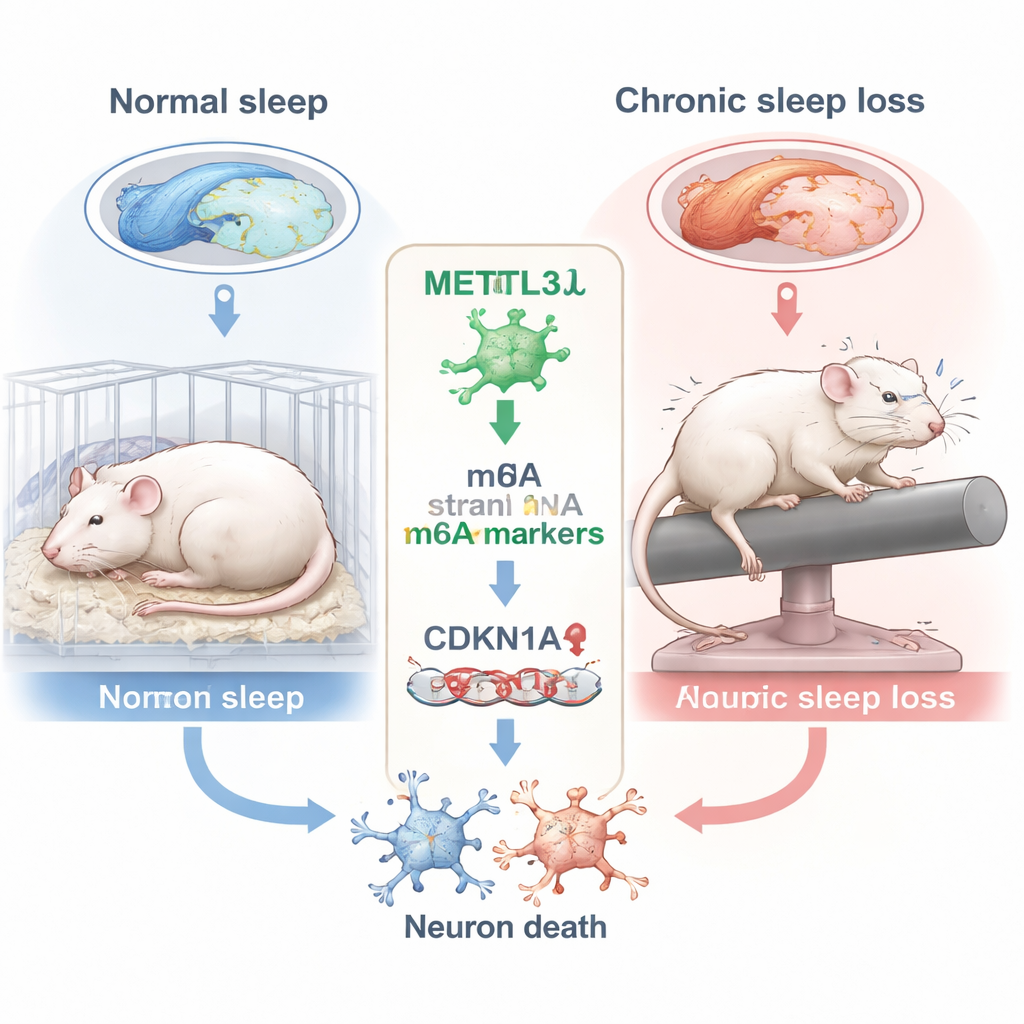
Come la perdita di sonno a lungo termine danneggia il centro della memoria
I ricercatori si sono concentrati sull’ippocampo, una regione cerebrale a forma di cavalluccio marino essenziale per la formazione di nuovi ricordi. All’interno dell’ippocampo hanno esaminato una sottoregione chiamata CA3, che aiuta a codificare e recuperare informazioni spaziali — abilità testate con compiti come trovare una piattaforma nascosta nell’acqua. I ratti sono stati tenuti svegli per 10 ore al giorno per sei settimane mediante un’asta rotante delicata che li svegliava ripetutamente. Quando la memoria è stata valutata nel noto Morris Water Maze, i ratti privati di sonno hanno percorso rotte meno dirette, hanno attraversato meno volte la posizione della piattaforma precedente e hanno trascorso meno tempo nel quadrante target: tutti segnali di deficit della memoria spaziale rispetto agli animali ben riposati.
Un segno chimico sull’RNA che viene meno
Per capire cosa stava succedendo nei neuroni CA3, il gruppo ha analizzato un marcatore chimico sull’RNA chiamato m6A, uno dei marchi interni più comuni sull’RNA messaggero. Questi marker aiutano a regolare la durata degli RNA e l’efficienza con cui vengono usati per produrre proteine. Un enzima chiave che aggiunge i marchi m6A è METTL3. Utilizzando il sequenziamento m6A ad alto rendimento e analisi dell’espressione genica, gli scienziati hanno scoperto che la privazione cronica del sonno riduceva in modo significativo METTL3 nella regione CA3. Questo calo è stato confermato sia a livello di RNA sia a livello proteico. Il profilo dei geni interessati suggeriva alterazioni nel controllo del ciclo cellulare e nelle risposte allo stress, facendo supporre che la perdita di sonno potesse spingere i neuroni verso stati non salutari.
Dalla variazione molecolare alla morte neuronale
Per valutare come la diminuzione di METTL3 potesse influenzare direttamente i neuroni, i ricercatori si sono rivolti a cellule ippocampali murine coltivate in piastre. Quando hanno usato piccoli RNA interferenti per silenziare METTL3, le cellule sono diventate molto più vulnerabili a un trattamento dannoso con rapamicina, un farmaco che stressa i neuroni. Queste cellule deplete di METTL3 hanno mostrato livelli più elevati di proteine classiche della “suicidio cellulare” come Bax e caspasi-3 clivata, e un maggior numero di cellule è stato identificato come apoptotico tramite citometria a flusso. Analisi più approfondite degli RNA hanno indicato un singolo gene, CDKN1A (che codifica la proteina p21), come attore chiave: quando METTL3 veniva ridotto, i livelli di CDKN1A aumentavano marcamente.
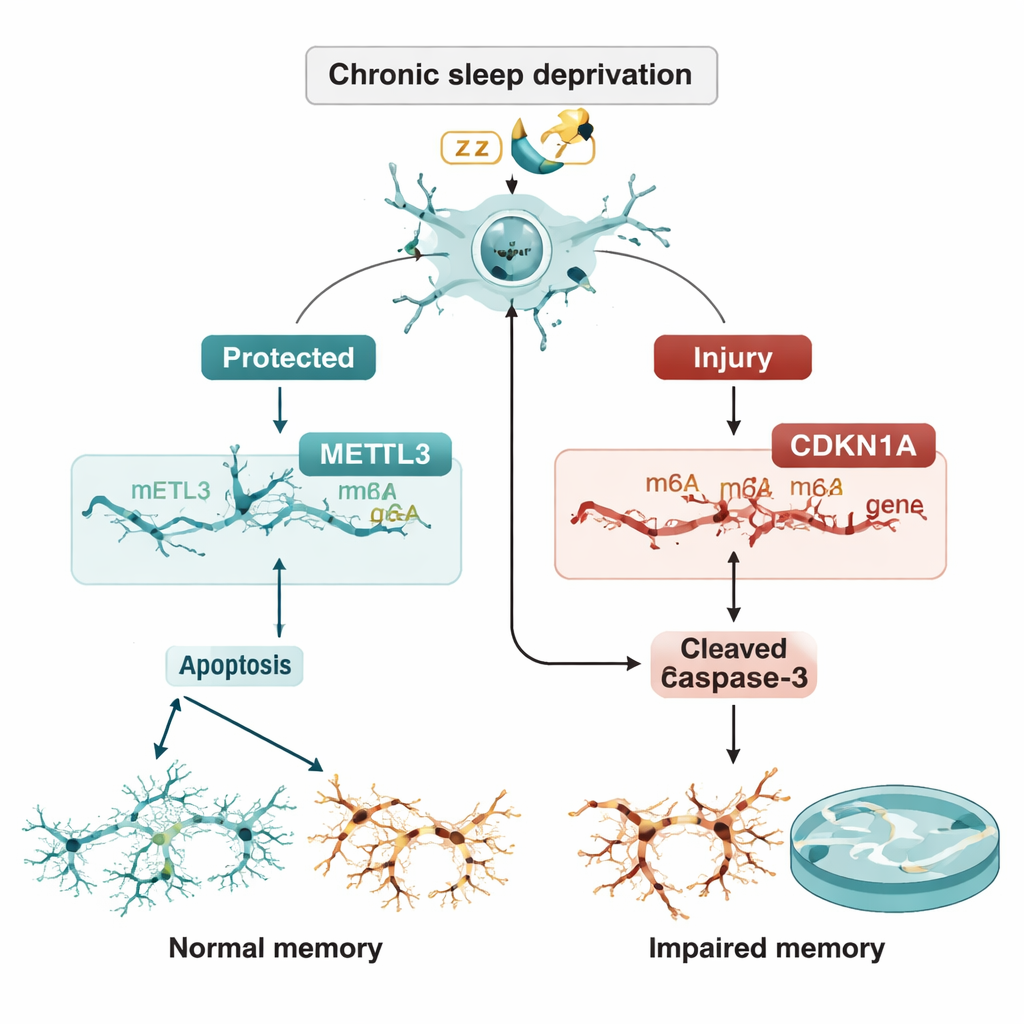
Un equilibrio fragile tra protezione e autodistruzione
Il team ha quindi verificato se METTL3 controllasse CDKN1A tramite l’etichettatura m6A. Hanno dimostrato che la riduzione di METTL3 abbassava i marchi m6A sull’RNA di CDKN1A e rendeva quell’RNA più stabile, così i suoi livelli aumentavano invece di venire degradati. L’aumento di CDKN1A, a sua volta, spingeva i neuroni verso l’apoptosi. Crucialmente, quando CDKN1A veniva silenziato, la morte cellulare addizionale causata dalla perdita di METTL3 veniva in gran parte invertita. Nei ratti vivi, la somministrazione di METTL3 in eccesso direttamente nella regione CA3 mediante un vettore virale riduceva i livelli di CDKN1A, abbassava l’abbondanza di proteine apoptotiche, preservava la struttura neuronale nelle colorazioni tissutali e migliorava le prestazioni nel water maze nonostante la continua perdita di sonno.
Cosa significa per le persone che non dormono abbastanza
In parole semplici, la privazione cronica del sonno sembra abbassare un enzima protettivo, METTL3, in un circuito cerebrale critico per la memoria. Quando METTL3 diminuisce, non può più etichettare correttamente alcuni RNA, in particolare quello che codifica CDKN1A. Quell’RNA allora si accumula, spingendo i neuroni verso la morte programmata e contribuendo ai problemi di memoria. Ripristinando METTL3, i ricercatori sono stati in grado di riportare CDKN1A a livelli più bassi, ridurre la perdita neuronale e recuperare la memoria nei ratti privati di sonno. Sebbene questo lavoro sia ancora a livello animale, identifica la via METTL3–CDKN1A come un promettente obiettivo per futuri farmaci volti a proteggere il cervello dalle conseguenze cognitive della perdita cronica di sonno.
Citazione: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Parole chiave: privazione cronica del sonno, ippocampo, metilazione dell'RNA, apoptosi neuronale, deficit della memoria