Clear Sky Science · it
Primi cambiamenti funzionali e GFAP plasmatico in famiglie svedesi con mutazioni dell’Alzheimer a trasmissione autosomica dominante
Perché questo studio è importante per le famiglie
La malattia di Alzheimer spesso sembra comparire all’improvviso, ma in realtà cambiamenti dannosi nel cervello si accumulano silenziosamente per molti anni. In famiglie rare portatrici di mutazioni ereditarie («autosomiche dominanti») dell’Alzheimer, gli scienziati possono stimare quando è probabile che compaiano i sintomi e osservare l’evoluzione di questi cambiamenti precoci. Questo studio ha seguito famiglie svedesi con tali mutazioni per capire come l’uso di energia del cervello, le capacità cognitive e un marcatore ematico delle cellule di supporto cerebrale (GFAP) cambino molto prima della comparsa dei problemi di memoria — e come questi cambiamenti differiscano a seconda del gene coinvolto.
Seguire l’orologio della malattia nelle famiglie ad alto rischio
Poiché le persone con Alzheimer autosomico dominante (ADAD) sviluppano i sintomi solitamente a un’età abbastanza prevedibile, i ricercatori possono calcolare gli «anni stimati all’esordio» (EYO) — quanti anni una persona è prima o dopo l’epoca prevista per i primi segnali della malattia. Il gruppo ha studiato 45 adulti appartenenti a famiglie svedesi con mutazioni nei geni APP o PSEN1, oltre a parenti non portatori. Per una media di oltre sette anni, i partecipanti si sono sottoposti a esami cerebrali che misurano quanto glucosio usa il cervello (FDG PET), a test cognitivi dettagliati e, per un sottoinsieme, a esami del sangue per il GFAP, una proteina rilasciata quando le cellule di supporto cerebrale chiamate astrociti diventano reattive. Questo disegno ha permesso agli scienziati di allineare i diversi cambiamenti biologici lungo una linea temporale condivisa della malattia, invece di limitarsi a confrontare le persone in un singolo momento temporale.
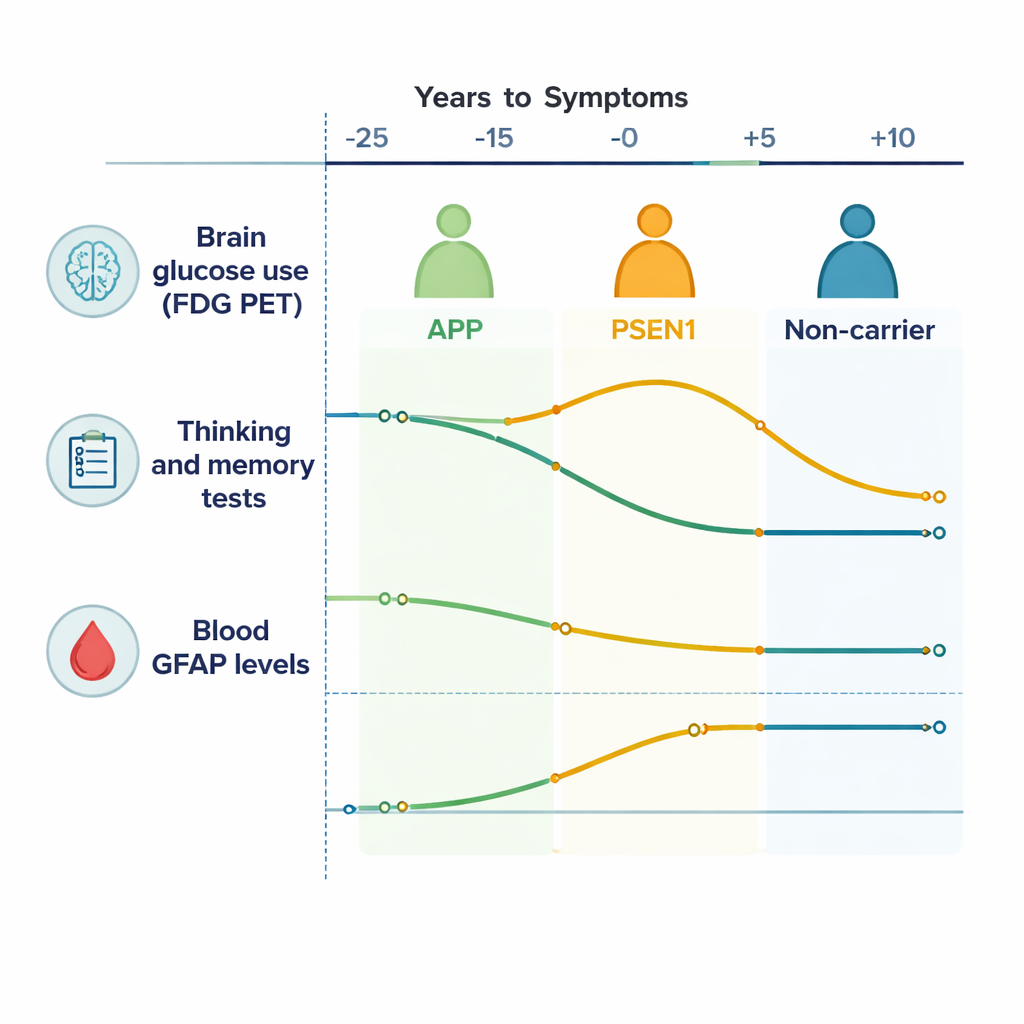
Monitorare nel tempo l’energia cerebrale e le funzioni cognitive
Alla corteccia cerebrale, le persone con mutazioni associate all’Alzheimer hanno mostrato una graduale riduzione del segnale FDG PET rispetto ai familiari non portatori, il che indica che i loro cervelli consumavano meno glucosio nel tempo — un segno di cellule cerebrali in difficoltà. Anche le regioni sottocorticali in profondità nel cervello, in particolare il caudato e il talamo, hanno mostrato un’attività in calo, guidata soprattutto dai portatori di mutazioni APP. I test di memoria e di altre funzioni cognitive sono peggiorati in vari domini, inclusa la memoria episodica e la flessibilità mentale, a partire da circa 10–15 anni prima dell’esordio previsto dei sintomi. In altre parole, mentre le persone si sentivano e funzionavano normalmente nella vita quotidiana, test sensibili e immagini rivelavano già che i loro cervelli stavano lavorando meno efficacemente.
Pattern diversi a seconda del gene dell’Alzheimer
Un’osservazione chiave è che i due principali gruppi di mutazione — APP e PSEN1 — non seguivano percorsi identici. Nei portatori di PSEN1, i ricercatori hanno osservato un periodo precoce, circa 20–10 anni prima dell’esordio previsto, in cui alcune aree cerebrali mostravano un uso di glucosio insolitamente elevato («ipermetabolismo»), insieme a prestazioni cognitive migliori, prima di un successivo declino. Questo probabilmente riflette una fase compensatoria temporanea, in cui il cervello e le sue cellule di supporto aumentano l’attività per far fronte al danno crescente. I portatori di APP, invece, hanno mostrato un calo più lineare e graduale del metabolismo cerebrale senza questo picco iniziale. Questi schemi specifici per gene suggeriscono che la «malattia di Alzheimer» non è una singola storia biologica, anche nelle forme ereditarie, ma una famiglia di processi correlati che si sviluppano in modo diverso a seconda della mutazione sottostante.
Cosa rivela un esame del sangue sullo stress cerebrale precoce
Il GFAP, misurato da un semplice prelievo di sangue, ha fornito uno sguardo su come gli astrociti rispondono ai cambiamenti precoci dell’Alzheimer. I livelli di GFAP tendevano ad aumentare in modo costante man mano che le persone si avvicinavano all’età prevista per l’esordio dei sintomi sia nei portatori di mutazione sia nei non portatori, ma le relazioni tra GFAP, metabolismo cerebrale e funzioni cognitive erano specifiche per gene. Nei portatori di APP, livelli più elevati di GFAP erano associati a un calo del consumo di glucosio nelle regioni profonde del cervello e a un peggioramento delle prestazioni nella maggior parte dei test cognitivi, suggerendo che l’attivazione degli astrociti è strettamente collegata ai danni precoci e alla perdita di funzione. Nei portatori di PSEN1, questi legami erano più deboli o assenti, indicando ancora una volta rotte biologiche differenti che conducono allo stesso esito clinico della demenza.
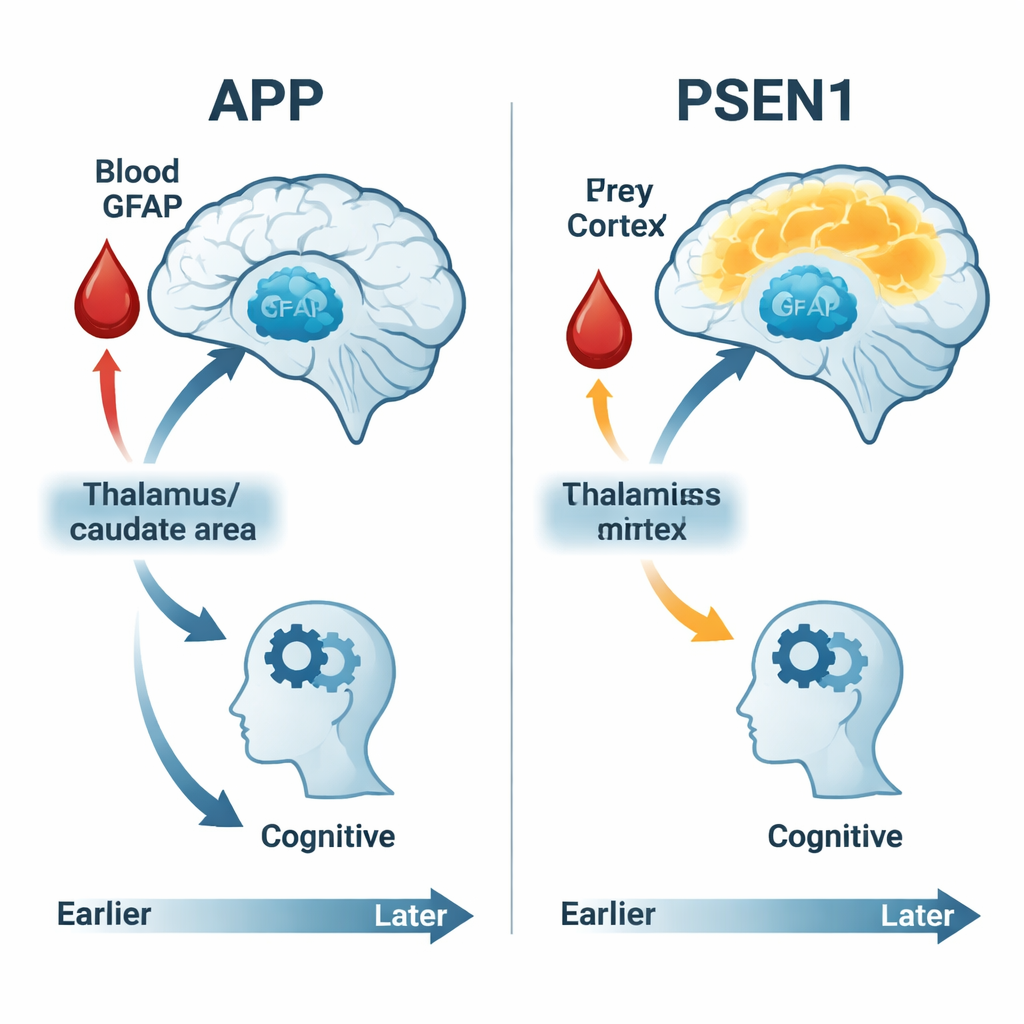
Cosa significa per la rilevazione precoce e il trattamento
Per un lettore non specialistico, il messaggio principale è che in queste famiglie ad alto rischio i cambiamenti legati all’Alzheimer iniziano decenni prima della perdita di memoria evidente — e non sono uguali per tutti. Le immagini che misurano l’uso del glucosio, i test cognitivi dettagliati e un singolo marcatore ematico come il GFAP possono insieme rivelare quando il cervello comincia a faticare e con quale rapidità procede questo declino. È importante che persone con diverse forme genetiche di Alzheimer mostrino sequenze di cambiamento differenti: alcuni hanno una fase iniziale di iperattività, altri evidenziano un declino costante, e il marcatore ematico dello stress degli astrociti si lega più fortemente al danno in alcuni gruppi rispetto ad altri. Riconoscere queste traiettorie distinte può aiutare a indirizzare meglio farmaci e studi clinici alle persone giuste nel momento giusto, e sostiene la promessa di test del sangue come il GFAP per intercettare l’Alzheimer più precocemente — prima che i sintomi privino le persone della loro indipendenza.
Citazione: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Parole chiave: malattia di Alzheimer autosomica dominante, biomarker plasmatico GFAP, metabolismo glucidico cerebrale, astrociti e neurodegenerazione, rilevazione precoce dell’Alzheimer