Clear Sky Science · it
Convergenza e divergenza dei geni informati da varianti comuni e rare dei disturbi dello spettro autistico in vie tissutali specifiche e reti geniche
Perché il puzzle genetico dell’autismo è importante
Famiglie e clinici sanno da tempo che il disturbo dello spettro autistico (ASD) è altamente variabile: alcune persone necessitano di supporto per tutta la vita, mentre altre vivono in modo indipendente ma incontrano difficoltà sociali. Gran parte di questa diversità è ritenuta di origine genetica, tuttavia il rischio è distribuito su migliaia di variazioni del DNA, ciascuna delle quali influisce sul cervello e sul corpo in modi sottili. Questo studio pone una domanda semplice ma rilevante: come interagiscono varianti rare e potenti e le molte varianti comuni e deboli nei diversi tessuti per modellare l’autismo — e cosa implica ciò per la comprensione e il trattamento della condizione?
Due tipi di indizi genetici
I ricercatori distinguono tra varianti rare, che possono alterare fortemente un gene ma si riscontrano in poche persone, e varianti comuni, frequenti nella popolazione ma di solito a piccolo effetto. Le varianti rare sono state più facili da collegare all’autismo in famiglie specifiche, ma spiegano solo una piccola frazione del rischio genetico complessivo. Le varianti comuni, prese nel loro insieme, rendono conto di gran parte della componente ereditaria dell’autismo, ma l’effetto di ognuna è minimo e facile da trascurare. Gli autori di questo lavoro hanno cercato di integrare segnali sia rari sia comuni, chiedendosi se convergano sugli stessi sistemi biologici o indichino parti diverse del corpo e meccanismi patologici differenti.
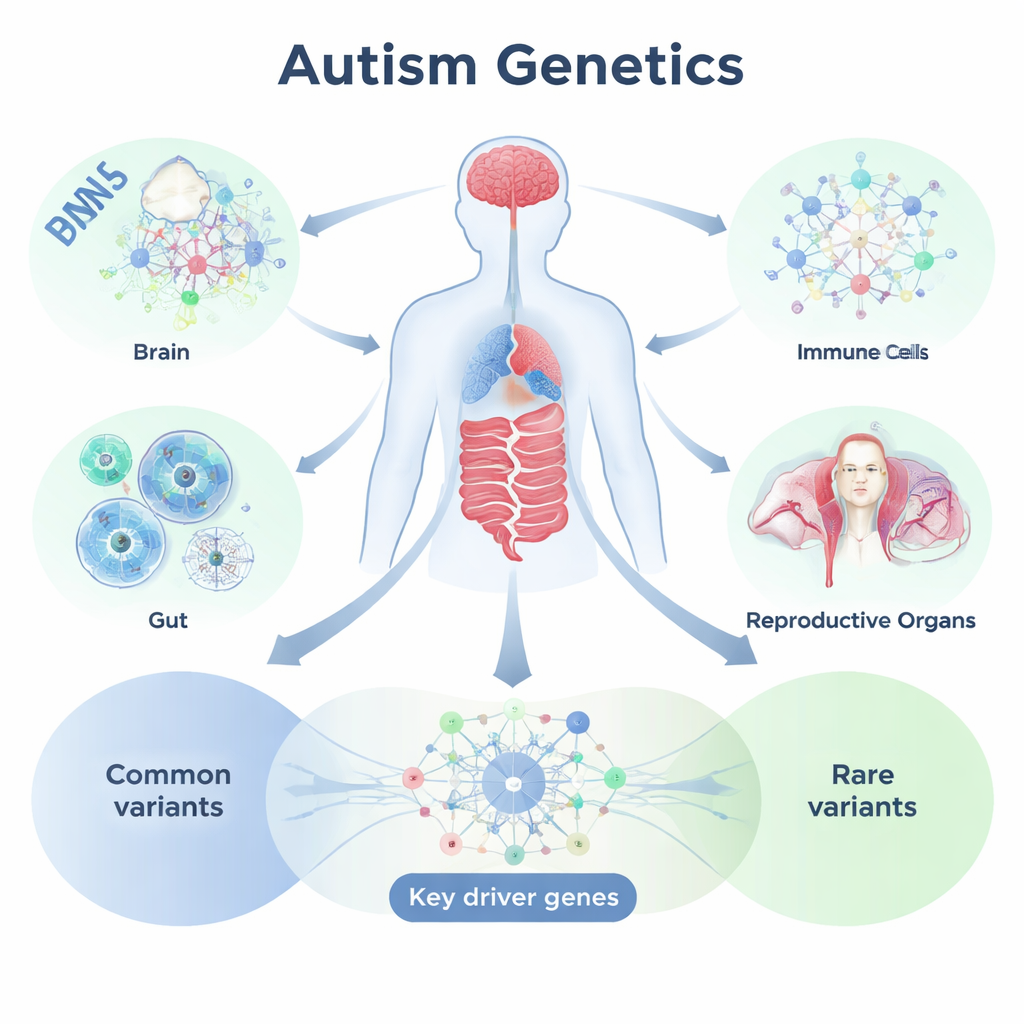
Mappare i segnali del DNA sui tessuti e sulle reti
Per affrontare la questione, il gruppo ha utilizzato un framework analitico chiamato Mergeomics, che combina studi genetici su larga scala con informazioni su come i geni vengono attivati e disattivati in tessuti specifici. Hanno iniziato da dati di associazione genome‑wide su oltre nove milioni di varianti comuni del DNA provenienti da più di 18.000 individui con autismo e circa 28.000 controlli non autistici. Hanno poi mappato queste varianti sui geni impiegando dati di riferimento dettagliati sull’attività genica in quasi 50 tessuti, incluse numerose regioni cerebrali oltre a organi periferici come quelli digestivi, immunitari, riproduttivi e altri. Raggruppando geni che sono attivati insieme nello stesso tessuto ed esaminando quanto fortemente quei gruppi si allineano con le varianti associate all’autismo, i ricercatori hanno identificato “moduli” specifici per tessuto e reti regolatorie che sembrano importanti per l’ASD.
Sia il cervello sia il corpo contribuiscono
L’analisi ha confermato un ruolo centrale del cervello — in particolare regioni come la corteccia cingolata anteriore, l’amigdala, la corteccia frontale, il cervelletto e aree corticali più ampie, note per essere coinvolte in emozione, comportamento sociale, funzioni cognitive e coordinazione. Le reti geniche in queste aree cerebrali erano ricche sia di varianti comuni sia di varianti rare correlate all’autismo e risultavano collegate a segnali sinaptici, neuro‑sviluppo e controllo immunitario nel cervello. Tuttavia il quadro non si è fermato al cranio. Con sorpresa, molti tessuti periferici, in particolare quelli digestivi, immunitari, endocrini e riproduttivi, contenevano moduli genici fortemente informati da varianti comuni associate all’autismo. Questi moduli erano associati a processi come risposte immunitarie, crescita e divisione cellulare, produzione di energia, splicing dell’mRNA e a una via di controllo principale nota come mTOR, tutte implicate nello sviluppo cerebrale e nel comportamento.
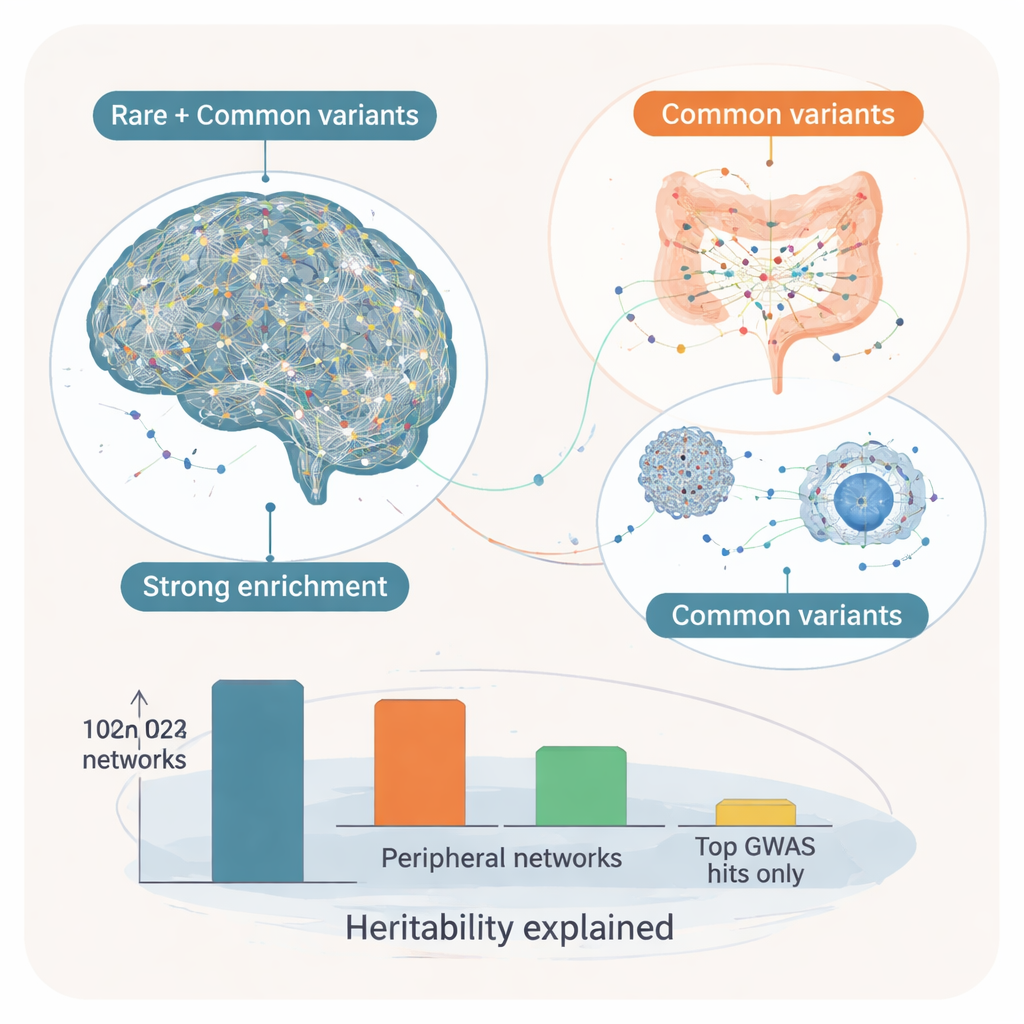
Geni chiave di controllo e l’idea core–modifier
Inserendo questi moduli in reti regolatorie geniche direzionali, i ricercatori hanno quindi identificato quali geni occupano i nodi centrali — i cosiddetti “key drivers” che influenzano molti altri geni. Nelle reti cerebrali, questi driver mostrano un forte arricchimento sia per varianti rare ad alto impatto associate all’autismo sia per varianti comuni, suggerendo che costituiscono un insieme “core” di geni dove entrambi i tipi di rischio convergono. Esempi includono SYT1, che regola il rilascio di neurotrasmettitori alle sinapsi, e ADD2, coinvolto nella forma e connettività neuronale. Le loro reti circostanti contenevano un miscuglio di geni autistici rari noti e bersagli di varianti comuni implicati nella comunicazione sinaptica e nell’eccitabilità neuronale. Al contrario, i driver chiave nei tessuti periferici, specialmente quelli digestivi ed endocrini, risultavano più fortemente influenzati solo dalle varianti comuni. Questi sembrano agire come “modificatori”, modulando vie immunitarie, metaboliche e di segnalazione che possono determinare come le vulnerabilità cerebrali core si manifestano nei sintomi.
Cosa significa per le persone e per i trattamenti futuri
Quando gli autori hanno stimato quanto del rischio ereditabile dell’autismo potesse essere ricondotto a queste reti, i moduli cerebrali spiegavano circa il 7% della componente ereditaria e i moduli periferici un ulteriore 3%, catturando insieme quasi tutta l’ereditarietà da varianti comuni osservata nello studio originale — e molto più di quanto spiegato dalle singole varianti più forti. Per i non specialisti, il messaggio è che la genetica dell’autismo segue uno schema a strati: varianti rare e comuni convergono su un insieme core di reti focalizzate sul cervello, cruciali per il neuro‑sviluppo, mentre diffuse varianti comuni in tessuti intestinali, immunitari e ormonali probabilmente modificano il decorso e le caratteristiche della condizione. Questo quadro core–modifier aiuta a spiegare perché l’autismo appare così diverso da una persona all’altra e suggerisce che terapie future potrebbero dover intervenire non solo sul cervello, ma anche sui sistemi corporei più ampi che interagiscono con esso.
Citazione: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
Parole chiave: genetica dell'autismo, varianti rare, varianti comuni, reti cerebrali, asse intestino‑cervello