Clear Sky Science · it
Recettore dell’istamina H3 come bersaglio per il disturbo da uso di alcol: mettere in discussione la prevedibilità dei modelli animali per la traduzione clinica nello sviluppo di farmaci
Perché questa ricerca conta nella vita di tutti i giorni
Il disturbo da uso di alcol colpisce milioni di persone in tutto il mondo, eppure i farmaci attualmente disponibili aiutano solo una frazione di chi ne ha bisogno. Questo articolo segue l’intero percorso di un promettente candidato farmaco, BP1.3656B, dal banco di laboratorio alle sperimentazioni umane. Mostra come un’idea che funziona bene negli animali possa comunque fallire negli esseri umani — e perché questo divario è importante per chiunque speri in trattamenti migliori per i problemi legati all’alcol.
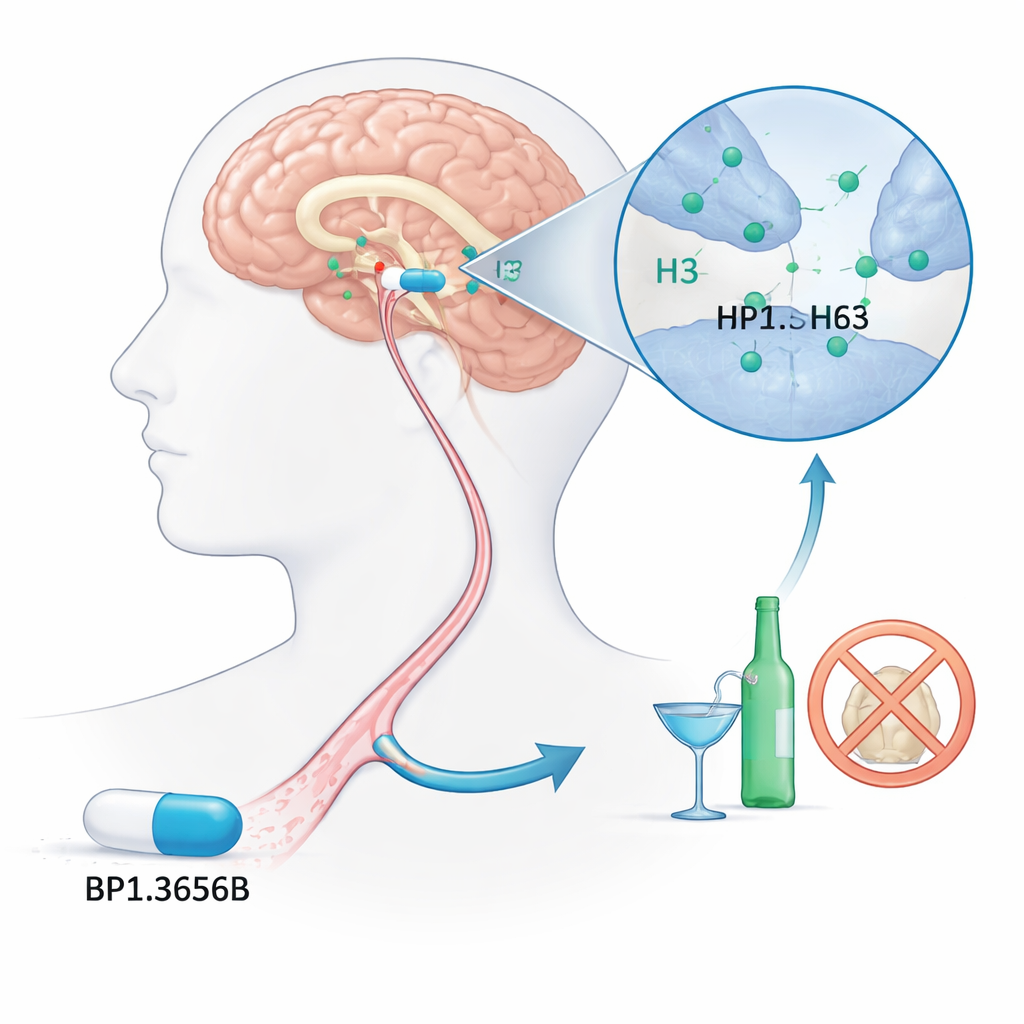
Un nuovo bersaglio cerebrale per il consumo problematico di alcol
I ricercatori si sono concentrati su un interruttore cerebrale meno conosciuto chiamato recettore dell’istamina H3. L’istamina è nota soprattutto per il suo ruolo nelle allergie, ma nel cervello contribuisce a regolare la vigilanza e la comunicazione tra i neuroni. Il recettore H3 agisce come un dimmer, riducendo il rilascio di istamina e di altri messaggeri chimici coinvolti nella ricompensa e nella motivazione. Poiché l’alcol interagisce in modo marcato con questi sistemi cerebrali, gli scienziati sospettano da tempo che bloccare i recettori H3 possa ridurre l’impulso a bere. BP1.3656B è stato progettato come un potente antagonista di H3, con la speranza di attenuare l’attrazione esercitata dall’alcol sui circuiti di ricompensa del cervello.
Dalla chimica alle storie di successo negli animali
Nei primi test, BP1.3656B ha mostrato il profilo che gli sviluppatori di farmaci sognano. Si legava con grande affinità e selettività al recettore H3, penetrava bene nel cervello e si è dimostrato sicuro negli screening di laboratorio standard. Nei topi, il farmaco riduceva l’esplosione di attività che di solito segue una somministrazione di alcol e diminuiva modestamente il consumo simile a binge nel test del “bere al buio”. Nei ratti addestrati a premere una leva per ottenere alcol, BP1.3656B riduceva nettamente la quantità consumata e quanto si impegnavano per ottenere alcol, sia negli animali che erano semplicemente forti bevitori sia in quelli resi dipendenti fisicamente. Inoltre attenuava il bere ricadente e alleviava l’ansia associata all’astinenza da alcol. Nel complesso, questi risultati suggerivano che il farmaco potesse ridurre la motivazione a bere e aiutare a prevenire la ricaduta nel consumo intenso.
Prime sperimentazioni umane: il farmaco raggiunge il bersaglio?
Sono seguiti studi di Fase I su volontari sani. Singole somministrazioni e dosi ripetute fino a 90 microgrammi sono state generalmente ben tollerate, con effetti collaterali principalmente lievi legati al sonno, coerenti con la natura di stimolo della veglia degli antagonisti H3. Le misurazioni del sangue hanno mostrato uno schema chiaro e prevedibile di assorbimento ed eliminazione del farmaco. Per accertare che raggiungesse il bersaglio previsto nel cervello umano vivo, il team ha utilizzato la tomografia a emissione di positroni, una scansione cerebrale in grado di mostrare quanti recettori sono occupati da un farmaco. Anche dosi relativamente basse di BP1.3656B hanno bloccato la maggior parte dei recettori H3 in diverse aree cerebrali importanti per motivazione e ricompensa, confermando che, almeno dal punto di vista biologico, il farmaco faceva ciò per cui era stato progettato.
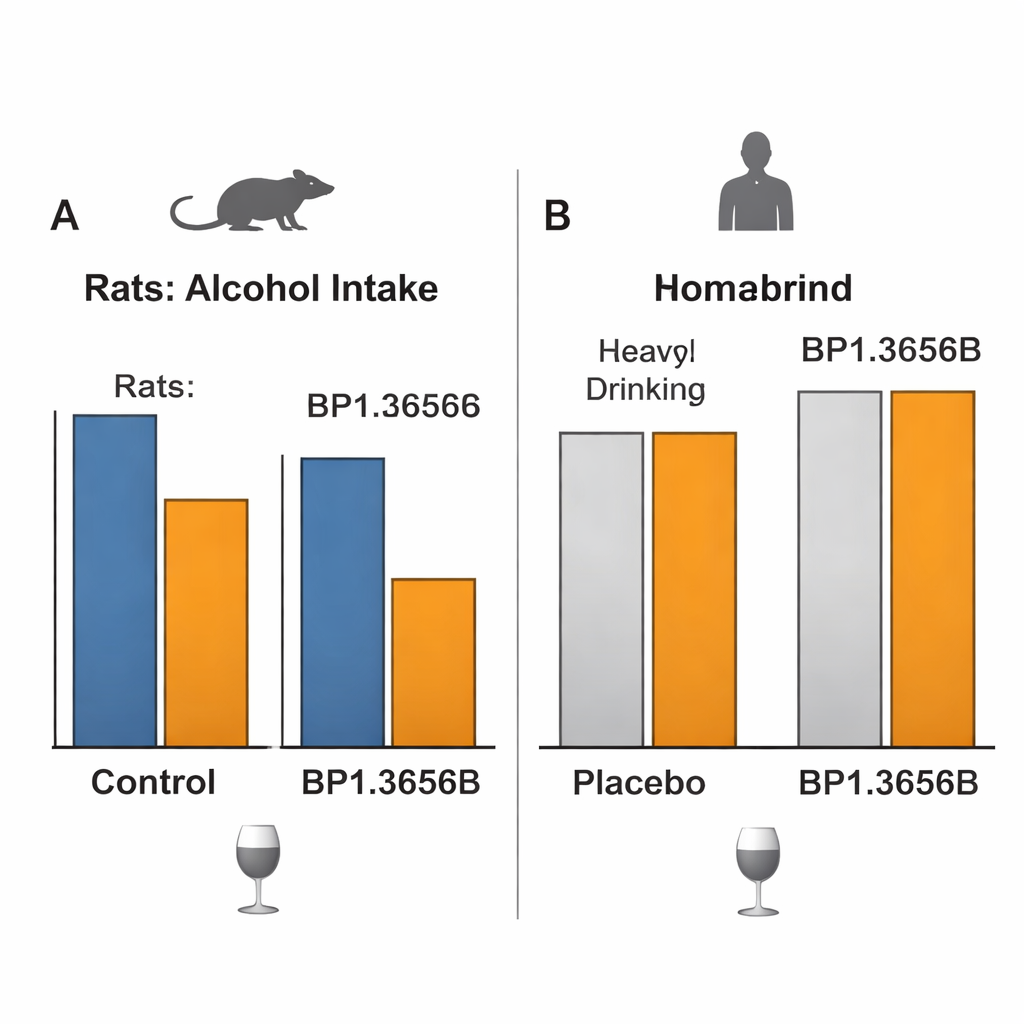
Quando risultati promettenti negli animali non si traducono nelle persone
La domanda cruciale era se tutto ciò si traducesse in cambiamenti significativi nel consumo di alcol nelle persone con disturbo da uso di alcol. In uno studio di laboratorio controllato, adulti con problemi di alcol che non cercavano trattamento hanno ricevuto BP1.3656B o placebo e poi hanno partecipato a sessioni in cui potevano auto-somministrarsi alcol per via endovenosa premendo un pulsante, in condizioni progettate per misurare sia il piacere sia la motivazione. Il farmaco non ha mostrato alcun effetto rilevabile sulla quantità di alcol che sceglievano di ricevere. Un più ampio trial clinico di 12 settimane, multicentrico e condotto in più paesi, ha poi testato tre dosi giornaliere di BP1.3656B rispetto a placebo in pazienti che cercavano trattamento. Tutti i gruppi, compreso il placebo, hanno ridotto in modo sostanziale i giorni di consumo intenso e l’apporto complessivo di alcol nel tempo, ma il farmaco non ha superato il placebo su nessuna misura importante di consumo o di craving, nonostante una buona sicurezza e un chiaro impegno sul bersaglio.
Che cosa significa per i trattamenti futuri
Per un lettore non esperto, la conclusione è sobria ma importante: un farmaco che sembrava eccellente in cellule, topi e ratti — e che chiaramente raggiungeva il suo bersaglio nel cervello umano — ha comunque fallito nel far bere meno le persone. Questo non significa che la scienza fosse sbagliata, ma sottolinea quanto sia incerta la previsione degli esiti umani basandosi solo sui modelli animali. Gli autori sostengono che studi umani di laboratorio più piccoli e in fase precoce, che testino direttamente l’impatto di un farmaco sull’uso di alcol, dovrebbero essere usati più routinariamente per «de-rischiare» lo sviluppo prima di lanciare trial grandi e costosi. In altre parole, questo lavoro mostra che non servono solo nuove idee farmacologiche, ma anche modi migliori per decidere quali di queste idee abbiano davvero una possibilità di aiutare le persone che lottano con il disturbo da uso di alcol.
Citazione: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
Parole chiave: disturbo da uso di alcol, recettore dell’istamina H3, BP1.3656B, trattamento della dipendenza, ricerca traslazionale