Clear Sky Science · it
Predittori computazionali delle varianti per la farmacogenomica: dalla valutazione di singoli alleli alla stima delle reazioni avverse ai farmaci antidepressivi
Perché i tuoi geni contano per la sicurezza degli antidepressivi
Quando due persone assumono lo stesso antidepressivo, una può migliorare con pochi effetti collaterali mentre l’altra può avere problemi seri, compresa la tossicità da farmaco. Questo studio esplora se programmi informatici possono interpretare piccole differenze nel nostro DNA per prevedere chi è probabile che metabolizzi gli antidepressivi in modo sicuro e chi potrebbe essere a maggior rischio di reazioni dannose, rendendo la prescrizione quotidiana più sicura e precisa.

Da etichette rigide a punteggi genetici flessibili
Oggi molte cliniche si affidano a un sistema chiamato “star alleles”, che raggruppa varianti del DNA note nei geni che processano i farmaci in poche categorie funzionali ampie, come attività normale o ridotta. Questo approccio ha aiutato a guidare i trattamenti, ma fallisce quando una persona porta varianti rare o mai viste prima, o combinazioni complesse di cambiamenti non presenti nelle liste ufficiali. Gli autori sostengono che questo sia un punto cieco rilevante: la maggior parte delle varianti farmacogenetiche è rara e una quota considerevole della variabilità nella risposta ai farmaci rimane inspiegata dalle etichette attuali.
Testare strumenti più intelligenti su varianti note e nuove
Il gruppo ha valutato dieci strumenti computazionali che assegnano un punteggio al potenziale danno di una modifica del DNA, inclusi due nuovi framework sviluppati dagli autori (PharmGScore e PharmMLScore). Innanzitutto hanno verificato se questi strumenti riuscivano a riprodurre le categorie funzionali già assegnate a 541 star alleles curate in otto geni chiave per il metabolismo dei farmaci. Sommando i punteggi di tutte le varianti all’interno di ciascun aplotipo, diversi strumenti eguagliarono o addirittura superarono le prestazioni del sistema a stelle, con PharmGScore in testa. Successivamente hanno sfidato gli strumenti con dati provenienti da esperimenti di laboratorio ad alta produttività su due enzimi importanti, CYP2C9 e CYP2C19, che metabolizzano molti farmaci. Questi esperimenti hanno misurato come migliaia di singole varianti influenzavano l’attività enzimatica e i livelli di proteina, la maggior parte delle quali non era mai stata osservata nei pazienti. Anche qui, gli strumenti migliori, in particolare gli ensemble focalizzati sui farmacogeni e CADD, individuarono con precisione le varianti che compromettevano gravemente la funzione enzimatica.
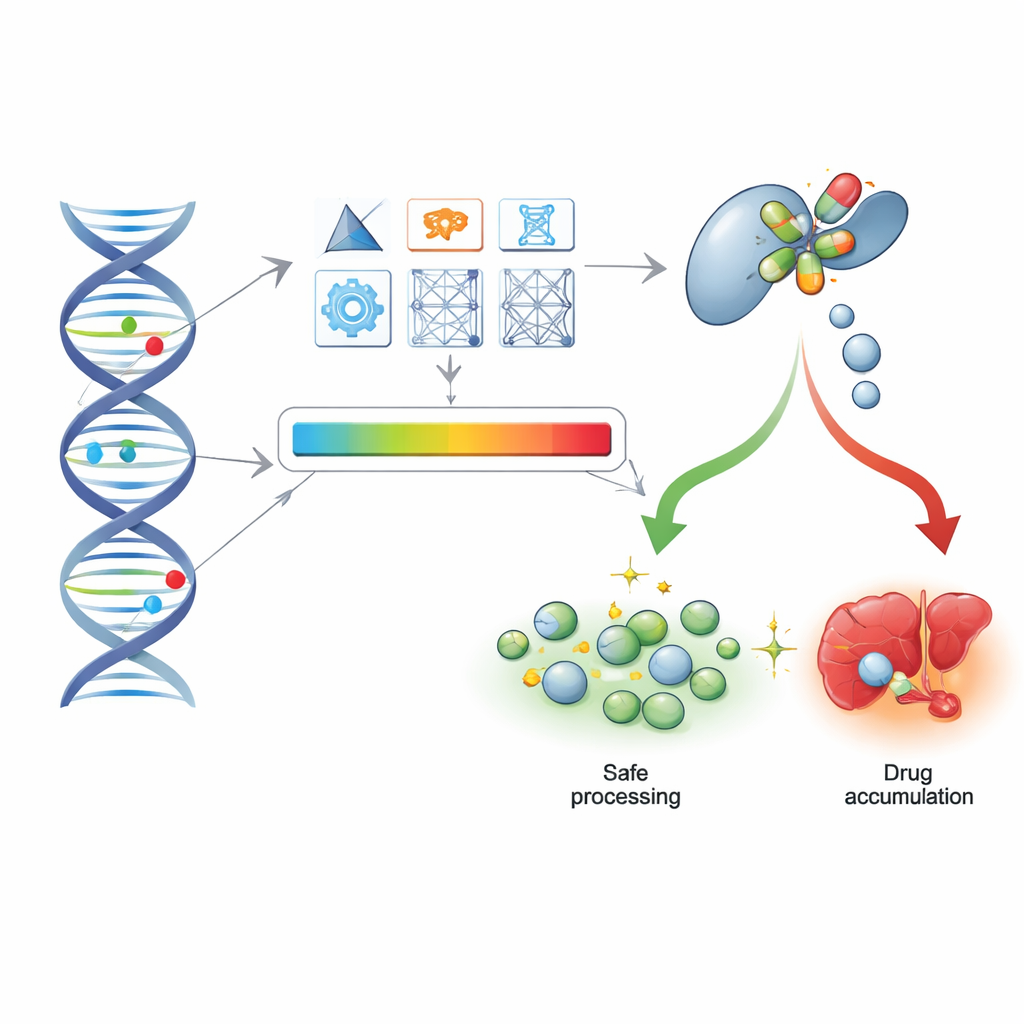
Dalle sequenze di DNA ai documenti clinici reali
Per verificare se questi punteggi computazionali resistono nella pratica medica quotidiana, i ricercatori si sono rivolti ai dati di sequenziamento dell’esoma di oltre 200.000 partecipanti della UK Biobank, insieme alle loro storie di prescrizioni e cartelle ospedaliere. Hanno confrontato le predizioni degli strumenti con le chiamate di star allele per cinque geni principali coinvolti nell’elaborazione dei farmaci e hanno scoperto che i metodi con i punteggi migliori riuscivano in larga misura a ricostruire gli stessi raggruppamenti funzionali, nonostante il fatto che i dati di esoma non catturino alcuni cambiamenti non codificanti e strutturali. È importante sottolineare che l’approccio additivo — sommare l’impatto di tutte le varianti in un gene — funzionò sufficientemente bene da separare le persone con genotipi non-funzionali da quelle con attività normale.
Individuare le persone a rischio di gravi reazioni agli antidepressivi
Gli autori si sono poi concentrati sull’uso e sulla sicurezza degli antidepressivi, mettendo a fuoco l’enzima CYP2C19, che contribuisce alla degradazione di diversi farmaci comuni per la depressione. Tra più di 75.000 utilizzatori di antidepressivi, hanno esaminato due esiti: il cambio frequente di farmaci, come indicatore approssimativo di risposta inadeguata, e record ospedalieri o di decesso che indicassero avvelenamento da antidepressivi. Sebbene né gli star alleles né la maggior parte dei punteggi mostrassero un segnale forte o chiaro per i cambi di trattamento, emerse un pattern significativo per le reazioni avverse gravi. I portatori di varianti dannose di CYP2C19 avevano circa il 20–35% in più di probabilità di presentare codici di avvelenamento grave da antidepressivi nei loro record, sia classificati mediante star alleles sia tramite strumenti computazionali con prestazioni elevate come PharmGScore, PharmMLScore e CADD. Questa relazione rimase simile anche quando le analisi furono ristrette ai casi senza documentazione di autolesionismo.
Cosa potrebbe significare per le prescrizioni future
Nel complesso, lo studio dimostra che predittori computazionali progettati con cura possono raggiungere lo stesso livello di accuratezza del tradizionale sistema a star alleles, superandone però la debolezza principale: l’incapacità di gestire varianti genetiche nuove, rare o complesse. Traducendo le sequenze di DNA grezze in punteggi di rischio continui che operano su tutto il genoma, questi strumenti potrebbero alla fine consentire ai clinici di andare oltre una breve lista di genotipi noti e anticipare meglio chi è a maggior rischio di gravi effetti collaterali da antidepressivi. Prima dell’uso nella pratica di routine saranno necessarie ulteriori validazioni e l’integrazione con altri fattori clinici, ma questo lavoro pone una solida base per prescrizioni più sicure e personalizzate basate su informazioni genetiche complete.
Citazione: Hajto, J., Piechota, M., Krätschmer, I. et al. Computational variant predictors for pharmacogenomics: from evaluation of single alleles to assessment of adverse drug reactions to antidepressants. Pharmacogenomics J 26, 8 (2026). https://doi.org/10.1038/s41397-026-00399-0
Parole chiave: farmacogenomica, antidepressivi, varianti genetiche, reazioni avverse ai farmaci, predizione computazionale