Clear Sky Science · it
Soppressione della produzione energetica mitocondriale da parte di un peptide cupredossina batterico fotosintetico inibisce la crescita tumorale
Trasformare i batteri in combattenti del cancro
Le cellule tumorali sono assetate di energia. Si affidano a minuscole “centrali elettriche” interne, i mitocondri, per generare l’energia necessaria a crescere, diffondersi e resistere alle terapie. Questo studio esplora un alleato inaspettato nella lotta contro il cancro: un breve frammento di una proteina originariamente trovata in batteri fotosintetici. I ricercatori dimostrano che questo peptide progettato può penetrare nelle cellule tumorali, arrestare la loro fornitura energetica alla fonte e rendere la radioterapia molto più efficace, risparmiando in larga misura le cellule normali.
Un piccolo peptide con un grande compito
Il gruppo è partito da una scoperta precedente secondo cui una proteina batterica chiamata azurina può rallentare la crescita tumorale agendo sul famoso soppressore tumorale p53. Hanno quindi cercato batteri presenti dentro e intorno ai tumori umani, concentrandosi su microrganismi fotosintetici che usano la luce per generare energia. Questi batteri possiedono una famiglia correlata di proteine chiamate cupredossine. Confrontando le loro strutture e la storia evolutiva, i ricercatori si sono focalizzati su una cupredossina, auracianina B, e hanno ricavato una breve regione di 28 amminoacidi che hanno chiamato aurB. Questo frammento è solubile in acqua, può attraversare le membrane cellulari e ha una conformazione che suggeriva la possibilità di interagire con macchinari chiave per la produzione di energia all’interno delle cellule.
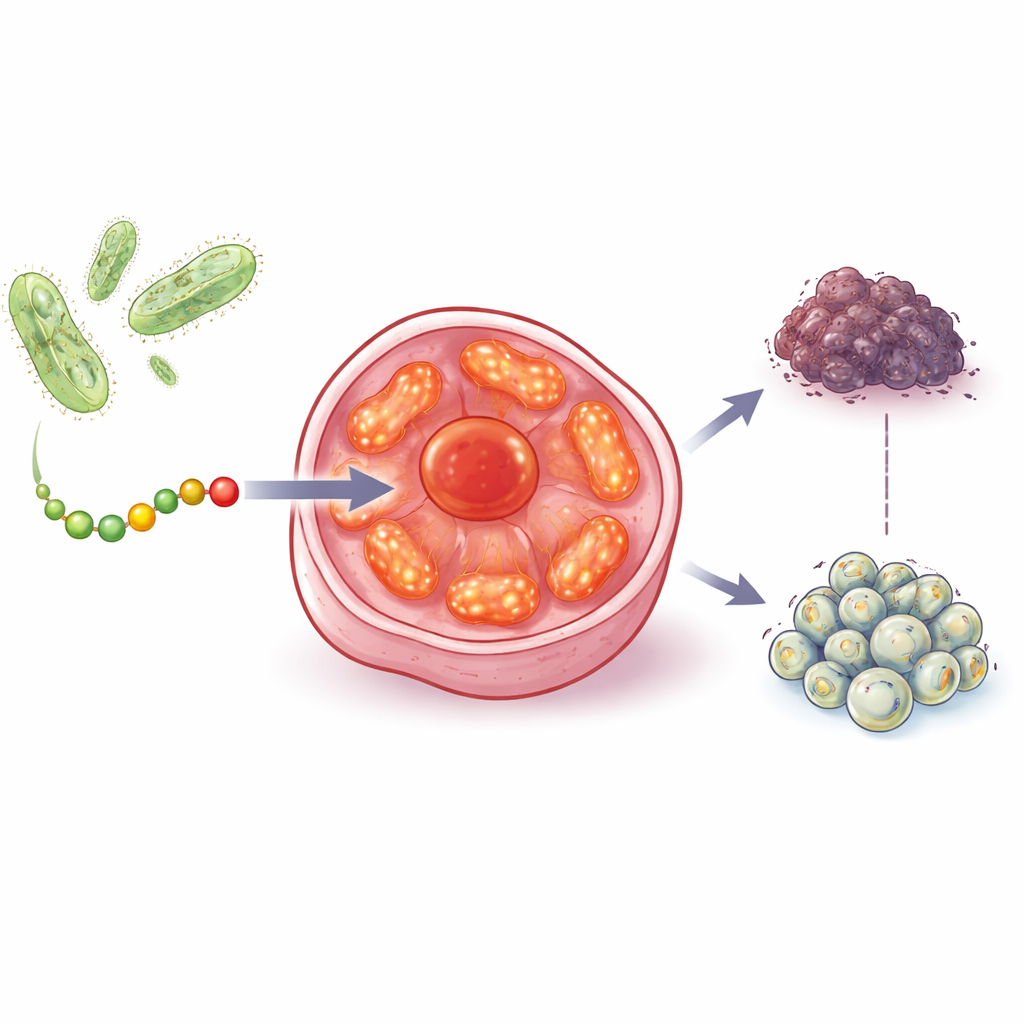
Trovare e colpire le centrali energetiche del cancro
Nei test di laboratorio, aurB ha ridotto la sopravvivenza di linee cellulari di tumore al seno, alla prostata, al colon e all’ovaio, anche quando quelle cellule erano prive di p53 funzionante o di recettori ormonali di cui molti farmaci attuali dipendono. È importante notare che aurB aveva effetti molto più deboli su cellule normali della prostata, del cuore e del muscolo, nonostante queste cellule sane siano ricche di mitocondri. Esperimenti di imaging hanno mostrato che aurB entra preferenzialmente nelle cellule cancerose e poi si concentra all’interno dei loro mitocondri. La microscopia elettronica, utilizzando aurB legato a piccolissimi bastoncini d’oro come marcatore visivo, ha confermato che il peptide si accumula effettivamente in questi organelli.
Tagliare la fornitura di energia
Una volta all’interno dei mitocondri, aurB si è legato a un componente specifico dell’ATP sintasi — la turbina molecolare che produce ATP, la principale valuta energetica della cellula. Esperimenti biochimici di pull-down e spettrometria di massa hanno identificato questo partner come ATP5C, parte del nucleo centrale dell’enzima. Misure con risonanza plasmonica di superficie hanno mostrato che aurB si attacca ad ATP5C con forza moderata e rilascio lento, coerente con un’interazione stabile. Saggi funzionali hanno quindi rivelato cosa provoca questo legame: aurB ha ridotto drasticamente i livelli mitocondriali di ATP nelle cellule di cancro alla prostata, ha rallentato il tasso di consumo di ossigeno e ha bloccato sia la respirazione sia la via metabolica di riserva della glicolisi. Con il collasso della produzione energetica, le cellule tumorali hanno mostrato segni di morte cellulare programmata guidata dalla caspasi-3, un enzima esecutore chiave.
Bloccare i tumori e potenziare la radioterapia
I ricercatori hanno poi testato aurB in modelli murini di cancro prostatico aggressivo. In animali portatori di tumori prostatici umani sottocutanei, iniezioni regolari di aurB hanno ridotto la crescita tumorale di circa due terzi, in modo comparabile o superiore al farmaco chemioterapico paclitaxel, ma senza perdita di peso o segni evidenti di malessere. I campioni tumorali dei topi trattati contenevano meno cellule in divisione e molte più cellule in necrosi o apoptosi. In un secondo modello che imita la metastasi ossea — una sede comune e letale della diffusione del cancro prostatico — aurB da solo ha rallentato l’espansione tumorale nel femore e ridotto il numero di metastasi polmonari. Quando combinato con una dose modesta di radiazioni, però, l’effetto è stato drammatico: i tumori nella zampa trattata sono stati quasi eliminati e le metastasi polmonari sono diminuite di oltre il 90 percento rispetto ai controlli.
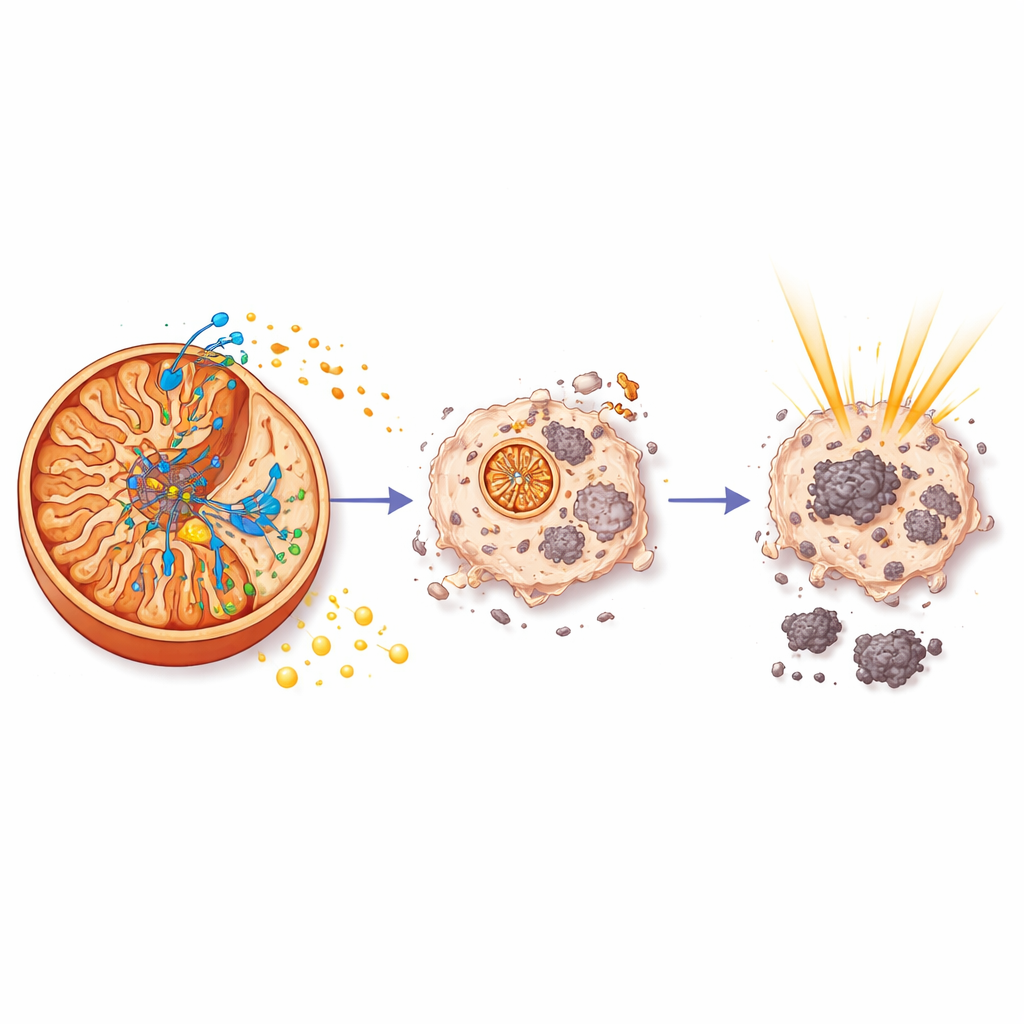
Perché l’energia è importante per la radioterapia
Per capire perché aurB rende la radioterapia più efficace, il team ha esaminato l’attività genica nei tumori dei topi trattati. Hanno scoperto che aurB, ma non la sola radioterapia, ha attenuato una rete di geni controllata da HIF-1, un regolatore maestro che aiuta le cellule tumorali ad adattarsi alla bassa disponibilità di ossigeno e alimenta la resistenza alle terapie. Nelle condizioni di carenza energetica create da aurB, le principali vie di crescita e sopravvivenza guidate da PI3K e c-Myc sono state spente, e anche il circuito glicolitico che permette ai tumori di prosperare in ambienti ostili è stato soppresso. In sostanza, sabotando la produzione di ATP direttamente alla turbina mitocondriale, aurB ha spinto le cellule tumorali in una crisi energetica che le ha rese molto più vulnerabili al danno indotto dalle radiazioni.
Una nuova classe di bloccanti energetici di precisione
Questo lavoro introduce una nuova strategia per la terapia del cancro: progettare piccoli peptidi ispirati ai batteri che si dirigono verso i sistemi energetici mitocondriali alterati nei tumori. AurB, derivato da una proteina batterica fotosintetica, prende di mira in modo selettivo un componente dell’ATP sintasi spesso iperattivo in tumori come quelli della prostata, del seno, dell’ovaio e del cervello. Privando direttamente le cellule tumorali dell’energia e indebolendo le loro difese, specialmente contro la radioterapia, tali peptidi potrebbero integrare i trattamenti esistenti e offrire opzioni dove gli approcci immunitari risultano insufficienti. Pur restando molto lavoro da fare prima che questo concetto arrivi in clinica, lo studio dimostra che antiche proteine energetiche batteriche possono essere riprogettate in strumenti antitumorali moderni e altamente mirati.
Citazione: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
Parole chiave: ATP sintasi mitocondriale, metabolismo del cancro, peptidi terapeutici, cancro alla prostata, sensibilizzazione alla radioterapia