Clear Sky Science · it
La segnalazione cGMP-protein chinasi G attenua la calcificazione della valvola aortica tramite autofagia mediata da ULK1
Perché la “ruggine” delle valvole cardiache conta
Con l’avanzare dell’età, la valvola aortica — la principale porta di uscita del cuore — può progressivamente irrigidirsi e ricoprirsi di depositi calcarei, una condizione nota come malattia calcifica della valvola aortica. Questo “indurimento” costringe il cuore a pompare con più forza e può provocare dolore toracico, svenimenti, insufficienza cardiaca o la necessità di sostituire la valvola chirurgicamente. Al momento non esiste una terapia medica che rallenti in modo affidabile questo processo: i medici possono solo attendere che la valvola sia gravemente compromessa e intervenire. Questo studio esplora una via cellulare intrinseca che sembra proteggere la valvola dalla calcificazione e testa un farmaco moderno per l’insufficienza cardiaca come possibile modo per riattivare quella protezione.
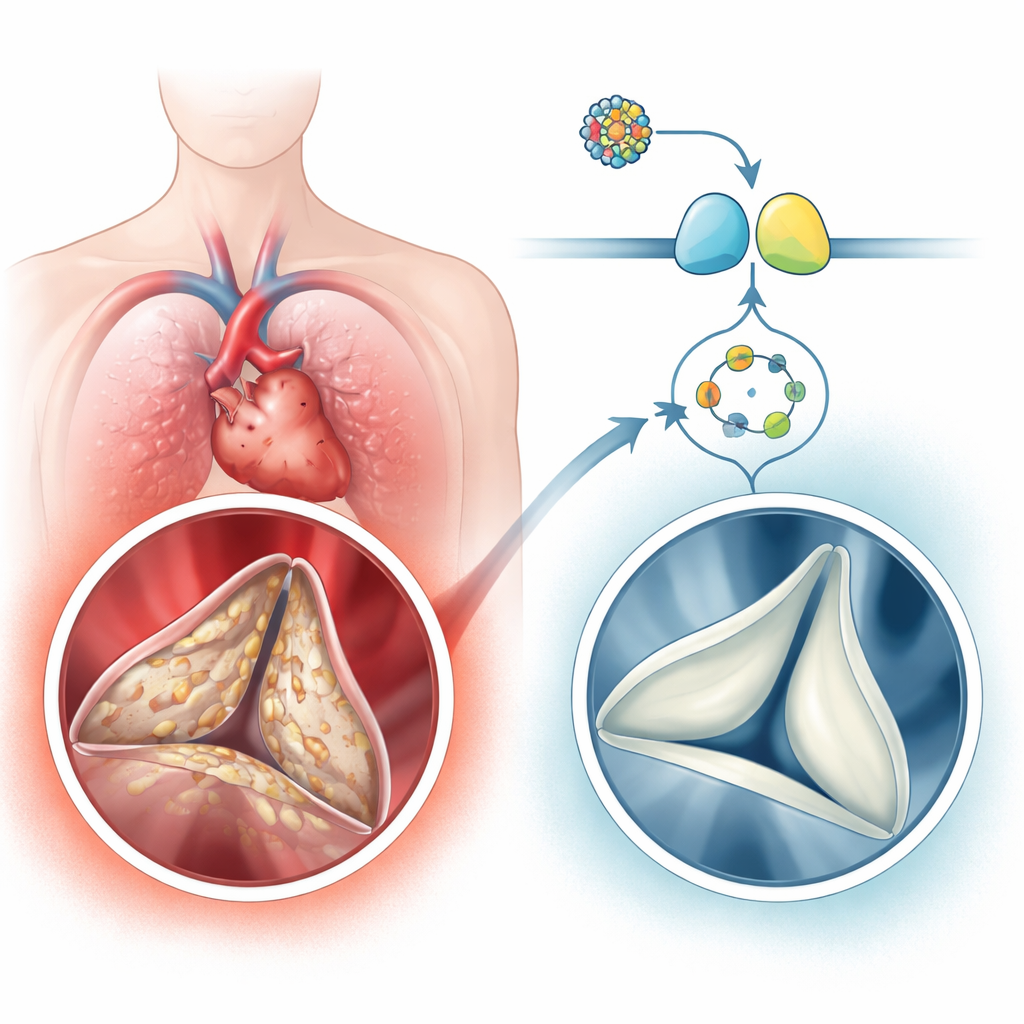
Un problema cardiaco comune ma trascurato
La malattia calcifica della valvola aortica è sorprendentemente comune negli anziani, colpendo diverse percentuali di persone oltre i 65 anni e fino a uno su dieci oltre i 75. La malattia non è semplicemente un “logoramento” passivo. Le cellule del tessuto connettivo della valvola, note come cellule interstiziali valvolari, si trasformano in stati simili alla riparazione di ferite e al tessuto osseo. Depositano collagene in eccesso e poi calcio, trasformando le cuspidi un tempo flessibili in lembi rigidi come la pietra. Gli autori hanno analizzato tessuto valvolare umano e ampi dataset di espressione genica e hanno riscontrato che una via di segnalazione centrata su una piccola molecola chiamata cGMP e sulla sua enzima partner, la protein chinasi G (PKG), risultava costantemente ridotta nelle valvole calcificate, mentre geni e proteine associati alla formazione ossea risultavano aumentati. Le persone con grave calcificazione valvolare presentavano anche livelli più bassi di cGMP nel sangue, in correlazione con il grado di restringimento e ostruzione valvolare.
Un segnale protettivo che scompare
Per sondare causa ed effetto, il team ha utilizzato topi e cellule valvolari umane coltivate. Topi ingegnerizzati per produrre meno PKG svilupparono cuspidi valvolari più spesse e maggiormente calcificate dopo un danno controllato alla valvola aortica, e le loro valvole mostrarono livelli più alti di una proteina maestro della formazione ossea. In cellule valvolari umane coltivate in condizioni che favorivano l’accumulo di calcio, la riduzione di PKG con strumenti genetici accelerò questa trasformazione di tipo osseo. Questi risultati suggeriscono che la segnalazione cGMP–PKG agisce normalmente come un freno alla riprogrammazione cellulare dannosa nella valvola — e quando questo freno si indebolisce, la calcificazione accelera.
Riadattare un farmaco per l’insufficienza cardiaca
I ricercatori si sono poi chiesti se potenziare questa via potesse rallentare o invertire la calcificazione. Hanno testato tre farmaci che aumentano il cGMP in modi differenti, incluso il vericiguat, un medicinale approvato per alcuni pazienti con insufficienza cardiaca. In cellule valvolari umane, tutti e tre i farmaci ridussero i depositi di calcio e i marcatori della trasformazione verso il tipo osseo, con il vericiguat che mostrò l’effetto più marcato. Il vericiguat ridusse anche la calcificazione in piccoli frammenti di tessuto valvolare umano mantenuti vitali al di fuori del corpo. In due modelli murini — uno indotto da dieta ad alto contenuto di colesterolo e l’altro da un danno meccanico alla valvola — il trattamento quotidiano con vericiguat portò a cuspidi più sottili, meno calcificate e a un migliore flusso ematico attraverso la valvola, senza indebolire la capacità di pompaggio del cuore. Quando il PKG venne ridotto geneticamente, tuttavia, il vericiguat perse in gran parte i suoi benefici, indicando che il PKG è il principale mediatore a valle.
Pulizia cellulare, valvole più sane
Approfondendo, il team scoprì che il vericiguat e il PKG proteggevano le piccole centrali energetiche delle cellule valvolari, i mitocondri. In condizioni calcificanti, le cellule accumulavano specie reattive dell’ossigeno dannose, perdevano il potenziale di membrana mitocondriale e producevano meno energia. Il vericiguat ripristinò le prestazioni mitocondriali e ridusse lo stress ossidativo. Mappe su larga scala delle proteine e dei siti fosforilati indirizzarono verso l’autofagia — il sistema cellulare di pulizia e riciclo. In valvole umane calcificate, l’imaging microscopico e i marcatori proteici mostrarono una ridotta formazione e attività degli autofagosomi, i “sacchi della spazzatura” dell’autofagia. Nell’analisi a singola cellula, diversi sottotipi di cellule valvolari provenienti da valvole malate mostrarono una soppressione generalizzata dei programmi legati all’autofagia. In colture cellulari, il blocco dell’autofagia annullò l’effetto protettivo dell’attivazione di PKG, suggerendo che il PKG agisce in gran parte risvegliando questo sistema di pulizia.
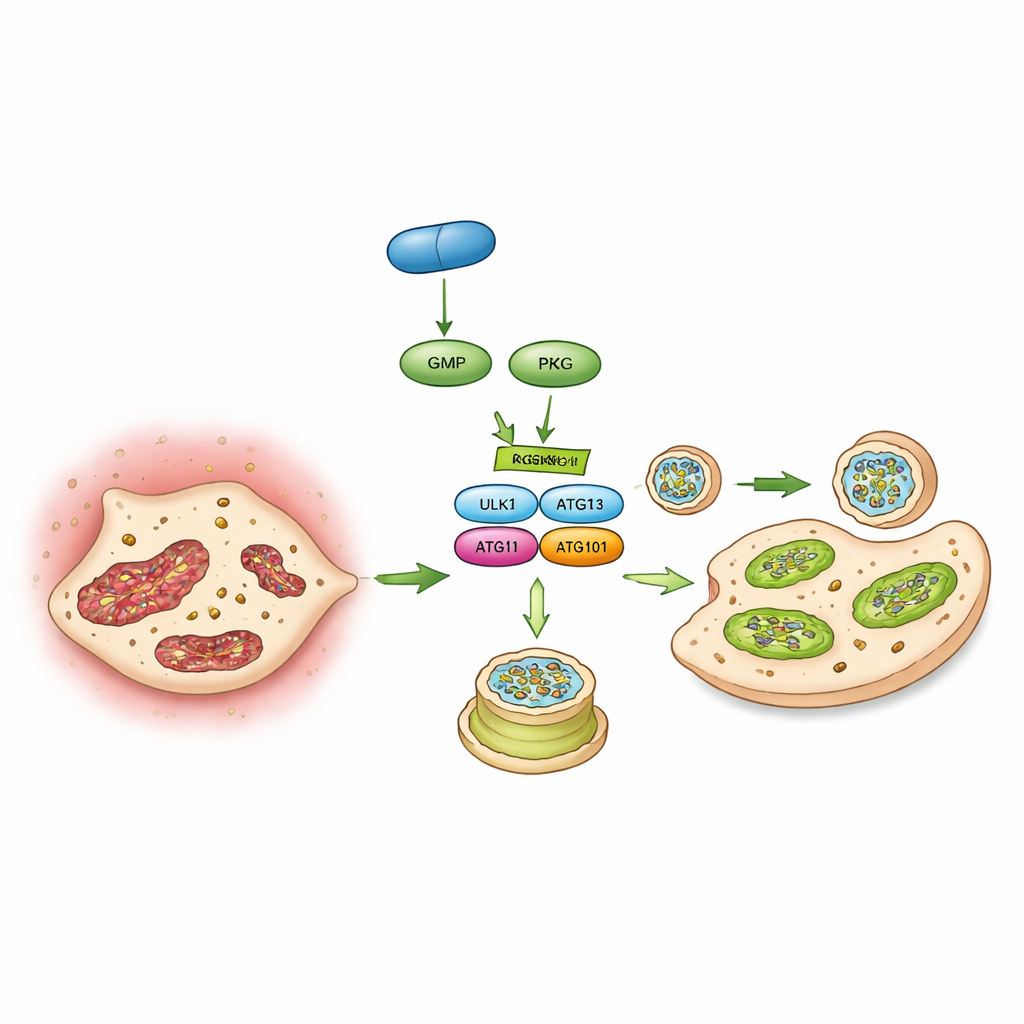
Invertire un interruttore molecolare
Infine, gli autori hanno identificato uno specifico interruttore molecolare che collega il PKG all’autofagia: una proteina chiamata ULK1 che avvia la formazione degli autofagosomi. Usando la fosfoproteomica, studi di interazione e saggi di chinasi in vitro, dimostrarono che il PKG aggiunge direttamente un gruppo fosfato a ULK1 in un sito particolare (un amminoacido chiamato serina 556). Quando questo sito venne mutato in modo da non poter più essere modificato, il PKG non poteva più potenziare l’autofagia né bloccare la calcificazione nelle cellule valvolari. Nei topi, l’espressione forzata di questo mutante ULK1 non reattivo nelle cellule valvolari eliminò anch’essa la capacità del vericiguat di proteggere la valvola. Nel loro insieme, questi risultati delineano una catena di eventi: il vericiguat stimola il cGMP, che attiva il PKG, che aziona l’interruttore ULK1, che risveglia l’autofagia, che preserva i mitocondri e impedisce alle cellule valvolari di trasformarsi in cellule produttrici di tessuto osseo.
Cosa potrebbe significare per i pazienti
Questo lavoro colloca l’asse cGMP–PKG–ULK1–autofagia come un sistema di difesa intrinseco contro la “ruggine” della valvola aortica. Nella malattia calcifica valvolare, quella difesa è attenuata, permettendo alle cellule di accumulare danno e di evolvere verso un’identità simile all’osso. Ripristinando farmacologicamente il segnale con un farmaco già impiegato nelle cliniche per l’insufficienza cardiaca, i ricercatori rallentarono la calcificazione in diversi modelli sperimentali. Sebbene saranno necessari studi clinici nell’uomo nella malattia valvolare, lo studio propone un’idea chiara e verificabile: potenziare con attenzione questa via di pulizia cellulare potrebbe un giorno ritardare o ridurre la necessità di sostituzione valvolare negli anziani a rischio di stenosi aortica.
Citazione: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Parole chiave: malattia calcifica della valvola aortica, segnalazione cGMP PKG, vericiguat, autofagia, calcificazione delle valvole cardiache