Clear Sky Science · it
La proteina simile a visinin 1 interrompe l’omeostasi del calcio e favorisce la fibrillazione atriale in modelli umani e di roditore
Perché questa storia sul ritmo cardiaco è importante
La fibrillazione atriale è un disturbo del ritmo cardiaco comune che aumenta il rischio di ictus e insufficienza cardiaca. Molte persone convivono con questa condizione, eppure i medici faticano ancora a prevenirla o a impedire che si ripresenti dopo il trattamento. Questo studio mette in luce una proteina precedentemente trascurata nelle cellule cardiache, chiamata VILIP-1, che funziona come un interruttore del calcio difettoso e contribuisce a promuovere la fibrillazione atriale sia nell’uomo sia negli animali. Identificando questo interruttore e dimostrando che farmaci già disponibili possono attenuarne l’attività, il lavoro apre una nuova strada verso terapie più sicure e mirate.
Uno sguardo più ravvicinato a un battito caotico
In un cuore sano, onde elettriche si propagano in modo ordinato attraverso le camere superiori, gli atri, guidando ogni battito. Quest’ordine dipende in gran parte dal calcio, un minerale carico che entra e esce dalle cellule cardiache per coordinare contrazione e rilassamento. Nella fibrillazione atriale, questo traffico di calcio diventa disordinato: perdite aggiuntive e oscillazioni dei livelli di calcio innescano segnali elettrici anomali che possono degenerare in ritmi rapidi e irregolari. I medici sanno da anni che la gestione alterata del calcio è centrale in questo disturbo, ma i fattori a monte che scatenano il caos sono rimasti poco chiari.
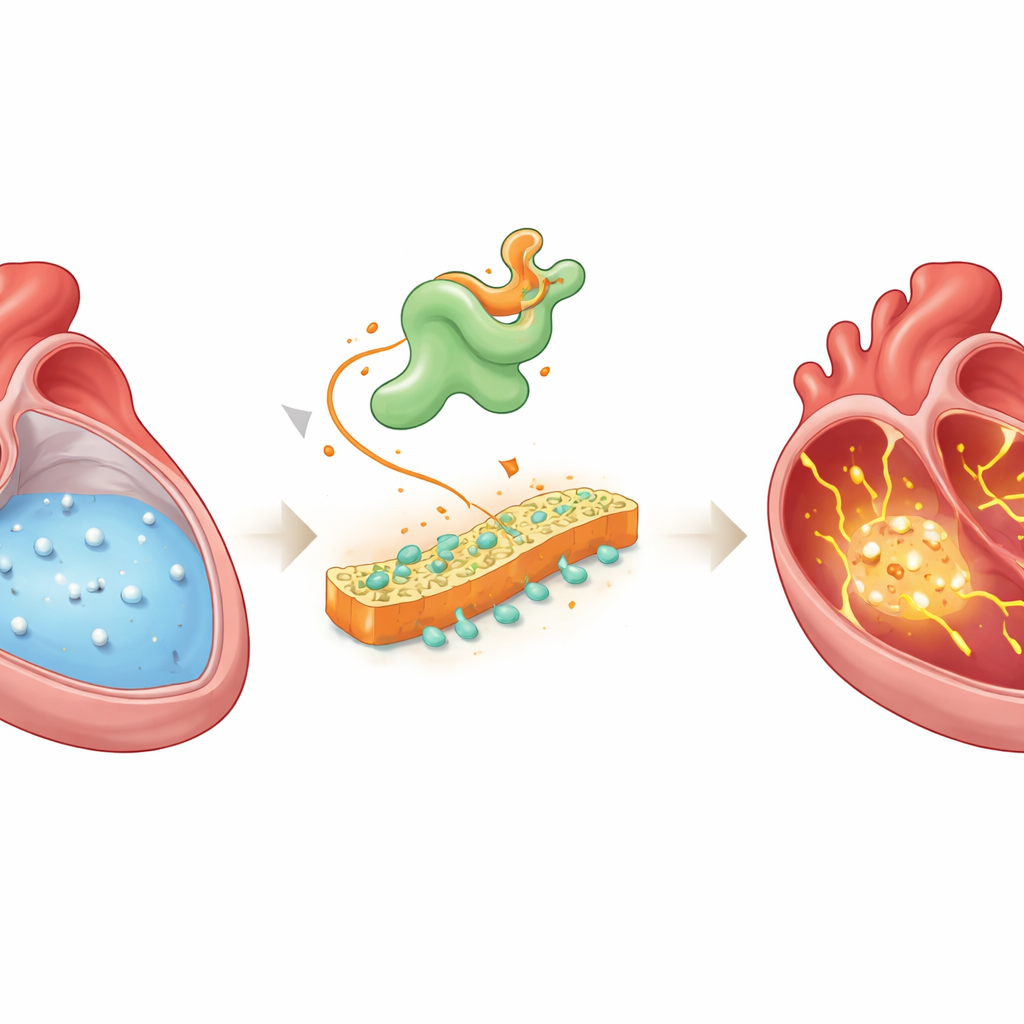
Scoprire un colpevole nascosto
I ricercatori hanno combinato diverse tecniche avanzate per cercare molecole che colleghino il malfunzionamento del calcio alla fibrillazione atriale. Hanno registrato segnali di calcio da centinaia di singole cellule atriali in ratti con fibrillazione atriale indotta da pacing, quindi hanno sequenziato l’insieme dei geni attivi in quelle stesse cellule. Hanno inoltre confrontato l’attività genica nel tessuto atriale di pazienti con fibrillazione atriale rispetto a pazienti con ritmo normale. Sovrapponendo questi set di dati e tracciando come le cellule evolvono dallo stato sano a quello malato, un gene è emerso ripetutamente: Vsnl1, che codifica la proteina VILIP-1, una molecola sensibile al calcio studiata in precedenza soprattutto nel cervello e nel pancreas, non nel cuore.
Come VILIP-1 altera l’equilibrio del calcio
Nel tessuto atriale sia dei pazienti sia dei modelli animali, i livelli di VILIP-1 risultavano significativamente più elevati e la proteina era concentrata sulla superficie cellulare. Per verificare se questa alterazione fosse solo un effetto secondario o un fattore causale, il team ha indotto cellule atriali murine a produrre quantità extra di VILIP-1. Questi topi non presentavano evidenti danni strutturali al cuore, ma i loro atri divenivano molto più suscettibili a entrare in fibrillazione atriale durante il pacing elettrico. Registrazioni elettriche dettagliate hanno mostrato un aumento delle afterdepolarizzazioni ritardate — anomalie dopo ogni battito — e alternanze da battito a battito nella forma del potenziale d’azione, segni classici di comportamento elettrico instabile legato a sovraccarico di calcio. L’imaging ad alta risoluzione del calcio ha confermato frequenti onde di calcio spontanee e svuotamento delle riserve interne di calcio, indicando perdite interne alle cellule di entità severa.
Il partner critico sulla superficie cellulare
Per capire come VILIP-1 provochi questa disfunzione, gli scienziati hanno mappato le proteine che interagiscono con essa nelle cellule cardiache. Utilizzando due metodi complementari — l’isolamento di partner di legame dal tessuto atriale e la marcatura delle proteine vicine con un “alone di biotina” in cellule vive — hanno individuato NCX-1, il principale scambiatore sodio–calcio nella membrana di superficie cardiaca. Questo scambiatore normalmente aiuta a espellere il calcio in cambio di sodio, ma in certe condizioni può funzionare in senso inverso e spingere calcio nella cellula. Lo studio ha mostrato che VILIP-1 si lega fisicamente a NCX-1 e aumenta il numero di molecole di NCX-1 presenti nella membrana senza aumentare la produzione totale di NCX-1. Di conseguenza, le correnti dello scambiatore diventavano maggiori, e bloccare NCX-1 con un inibitore selettivo riduceva le onde di calcio e rendeva più difficile provocare la fibrillazione atriale nei topi con eccesso di VILIP-1.
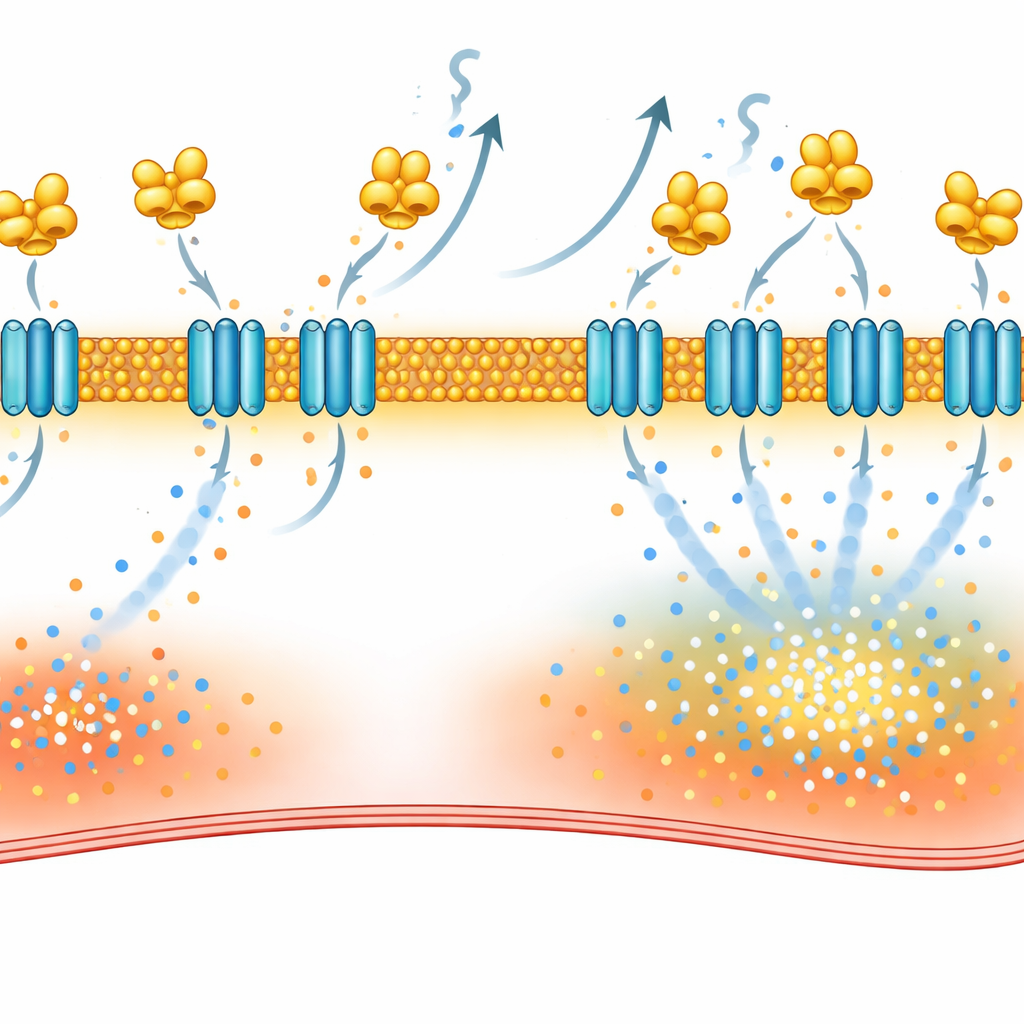
Spegnere l’interruttore difettoso con farmaci esistenti
VILIP-1 si ancora alle membrane tramite un tag grasso chiamato miristato, che viene esposto quando il calcio si lega alla proteina. Il gruppo ha usato desloratadina, precedentemente dimostrata interferire con questo passaggio di ancoraggio, e ha osservato una riduzione di NCX-1 sulla superficie cellulare, la normalizzazione delle correnti dello scambiatore, la diminuzione delle onde di calcio e una riduzione degli episodi di fibrillazione atriale nei modelli di ratto. Hanno anche testato repaglinide, un farmaco per il diabete noto per legare sensori del calcio correlati. Saggi biofisici hanno confermato che repaglinide si lega direttamente a VILIP-1. In ratti sottoposti a pacing e in tessuto atriale di pazienti con fibrillazione atriale, il trattamento con repaglinide ha ridotto NCX-1 nella membrana, attenuato le perdite di calcio nelle singole cellule e diminuito sostanzialmente la facilità con cui si poteva indurre la fibrillazione atriale.
Cosa significa per le persone con battito irregolare
Nel complesso, lo studio delinea un circuito autoreinforzante: l’aumento dei livelli di calcio recluta VILIP-1 alla superficie cellulare, dove essa potenzia NCX-1, che a sua volta alimenta ulteriore sovraccarico di calcio e crea le condizioni per la fibrillazione atriale. Interrompendo questo circuito a livello di VILIP-1 — sia bloccando il suo ancoraggio grasso sia legando il suo dominio sensibile al calcio — farmaci esistenti possono ristabilire un equilibrio del calcio più stabile e ridurre la vulnerabilità all’aritmia nel tessuto cardiaco umano e di roditore. Sebbene siano necessari ulteriori studi per raffinare la specificità dei farmaci e testare queste strategie in modelli animali più grandi e in trial clinici, VILIP-1 emerge ora come una promettente nuova leva per prevenire e trattare questo diffuso e spesso ostinato disturbo del ritmo cardiaco.
Citazione: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
Parole chiave: fibrillazione atriale, segnalazione del calcio, aritmia cardiaca, scambiatore sodio-calcio, bersagli terapeutici