Clear Sky Science · it
Segnalazione Fibrinogeno–Bmal1 come bersaglio terapeutico per limitare la dissezione aortica preservando la contrattilità delle VSMC
Perché il guardiano nascosto dell’aorta è importante
La dissezione aortica è una delle emergenze più temute in medicina: l’arteria principale che esce dal cuore può lacerarsi all’improvviso, spesso senza preavviso, e molti pazienti muoiono nel giro di poche ore. L’intervento chirurgico può salvare vite, ma è rischioso e non sempre fattibile immediatamente. Questo studio esplora un alleato inaspettato già presente nel nostro sangue—il fibrinogeno, una proteina della coagulazione—e mostra che, oltre a contribuire a fermare le emorragie, potrebbe effettivamente aiutare a mantenere coesa l’aorta e rallentare la progressione della malattia, guadagnando così tempo prezioso per i medici.
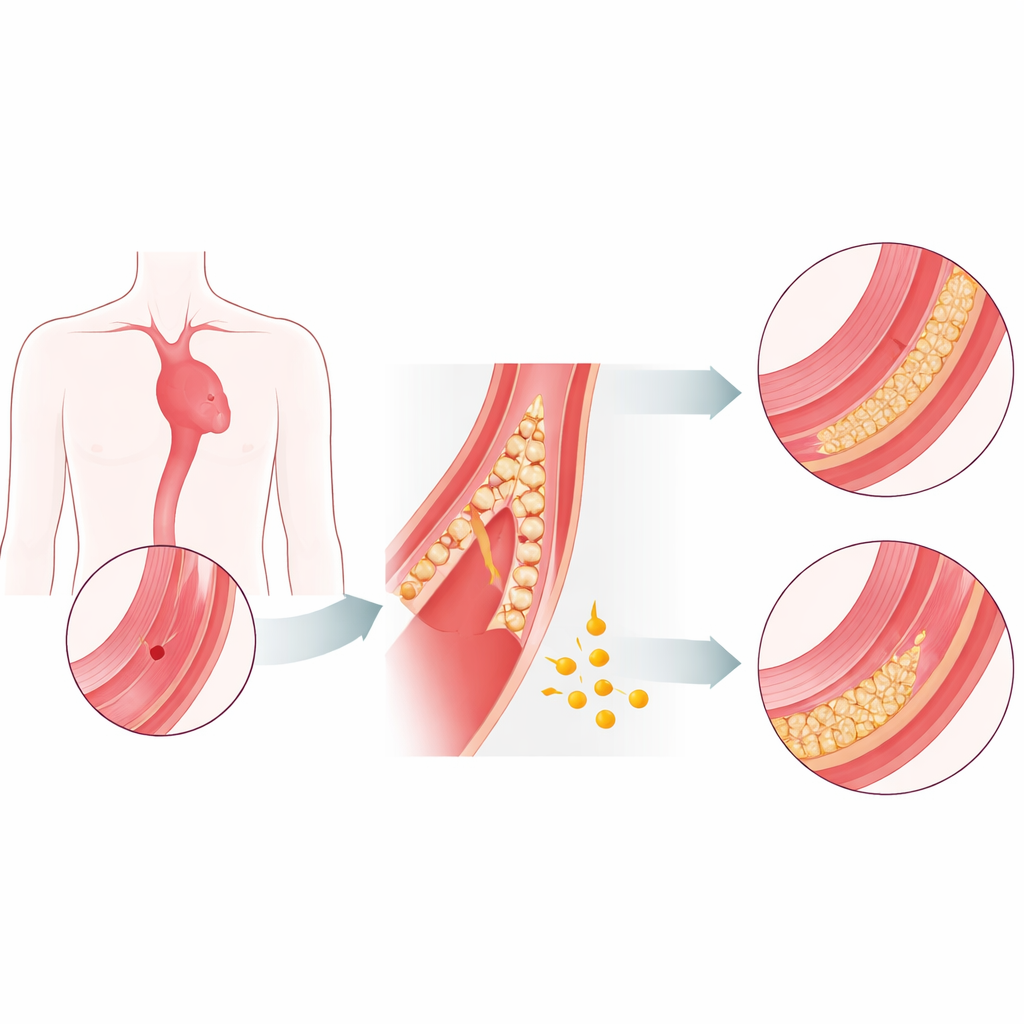
Un killer silenzioso che necessita di nuove opzioni
L’aorta è costruita come un robusto tubo multistrato. Quando gli strati interni si indeboliscono e si separano, il sangue può insinuarsi nella parete e spalmarla—questa è la dissezione aortica. Nella fase iniziale, pericolosa, il rischio di morte aumenta ora dopo ora, e l’intervento d’urgenza è spesso l’unica opzione. I pazienti che sopravvivono a sufficienza per raggiungere una fase più stabile e cronica tendono ad avere esiti molto migliori. Oggi non esistono farmaci dimostrati in grado di rallentare in modo affidabile il processo di lacerazione o di rinforzare la parete aortica. Gli autori hanno voluto verificare se il fibrinogeno, una proteina sanguigna comune nota soprattutto per il suo ruolo nella coagulazione, potesse agire anche come stabilizzatore naturale dell’aorta.
Indizi dai pazienti: più fibrinogeno, migliore sopravvivenza
Il gruppo ha esaminato inizialmente 310 pazienti con dissezione aortica acuta che non potevano sottoporsi a chirurgia e sono stati trattati solo con farmaci. Hanno confrontato chi è sopravvissuto al ricovero con chi è deceduto. I pazienti deceduti avevano in genere livelli di fibrinogeno molto più bassi nel sangue. Raggruppando i pazienti in base ai livelli di fibrinogeno, è emerso che livelli molto bassi (al di sotto di 2 grammi per litro) erano associati a tassi di mortalità molto più elevati, mentre livelli alti (sopra i 4 grammi per litro) erano correlati a una migliore sopravvivenza. Questo schema suggeriva che il fibrinogeno non fosse solo un osservatore passivo ma potesse effettivamente contribuire a far resistere l’aorta a ulteriori lacerazioni.
Osservare la rottura e la guarigione dell’aorta nei topi
Per andare oltre l’associazione e testare la causalità, gli scienziati hanno utilizzato modelli murini in cui l’aorta può essere indotta a indebolirsi e a disseccarsi. In questi animali il fibrinogeno era normalmente assente dalla parete aortica sana, ma con lo sviluppo della malattia iniziava a infiltrarsi nello strato mediale dove risiedono le cellule muscolari lisce. Colpisce che l’accumulo maggiore di fibrinogeno comparisse nei segmenti gravemente danneggiati ma ancora non rotti, suggerendo che la sua presenza potesse contribuire a impedire la rottura finale della parete. Quando i ricercatori hanno ridotto la produzione epatica di fibrinogeno tramite terapia genica, le dissezioni sono peggiorate: le aorte si sono dilatate di più, il danno strutturale è aumentato e più topi sono morti. La somministrazione di fibrinogeno purificato ha invertito questi effetti. Esperimenti indipendenti con un diverso modello di aneurisma aortico hanno mostrato una tendenza protettiva simile, rafforzando l’ipotesi che il fibrinogeno difenda attivamente la parete vascolare.
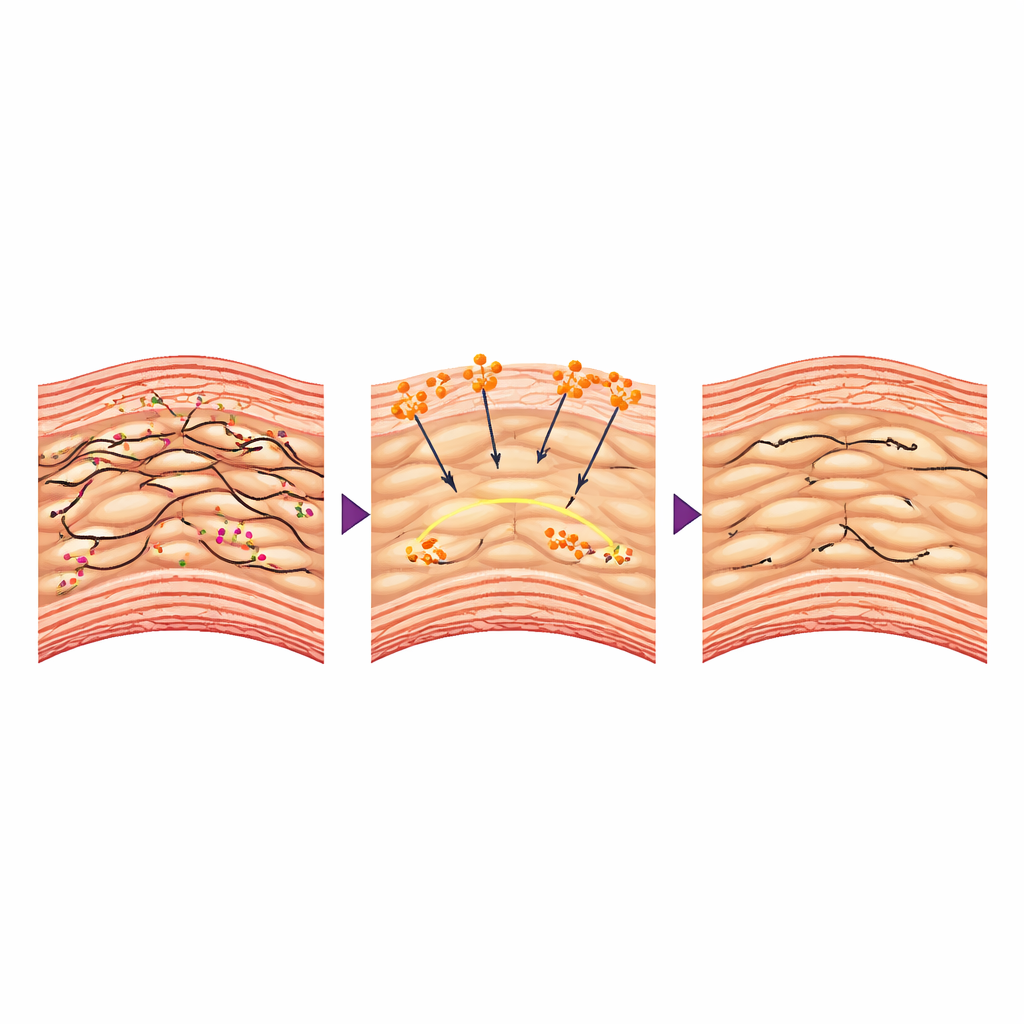
Il dialogo nascosto tra proteina del sangue e cellule muscolari
Come potrebbe una proteina della coagulazione proteggere dall’interno l’aorta? Gli autori si sono concentrati sulle cellule muscolari lisce vascolari, le cellule contrattili che formano lo strato mediale dell’aorta e fungono da “anelli di rinforzo” viventi. Nella malattia queste cellule spesso perdono il loro stato contrattile stretto e si trasformano in una forma più sintetica e lassa che degrada il tessuto circostante. Lo studio ha rilevato che quando il fibrinogeno penetrava nella parete aortica interagiva con recettori specifici su queste cellule e contribuiva a preservare il loro impalcato interno di filamenti di actina. Le cellule muscolari lisce provenienti da animali trattati erano più rigide, si contraevano più fortemente nei test ed esprimevano più marcatori “contrattili” e meno proteine che degradano la matrice di supporto. A livello genico, il fibrinogeno attenuava l’attività di Bmal1, un regolatore master legato all’orologio biologico che in questo contesto promuoveva cambiamenti nocivi nel comportamento delle cellule muscolari. Forzare l’aumento di Bmal1 annullava i benefici del fibrinogeno, dimostrando che questo percorso di segnalazione è centrale per l’effetto protettivo.
Dal meccanismo al potenziale trattamento
Poiché il fibrinogeno promuove anche la coagulazione, il gruppo si è chiesto se il suo beneficio fosse semplicemente dovuto alla formazione di coaguli più robusti. Utilizzando un potente anticoagulante per bloccare la trombina—l’enzima che trasforma il fibrinogeno in un coagulo solido—hanno mostrato che il fibrinogeno proteggeva comunque l’aorta anche quando la formazione del coagulo era in gran parte disabilitata. Infine, hanno testato dosi differenti e hanno scoperto che solo quantità sufficientemente alte di fibrinogeno somministrato rallentavano la malattia, riducevano le rotture e preservavano la struttura tissutale. Nel complesso, questi risultati dipingono il fibrinogeno come una molecola a doppio scopo: a livelli più elevati, il fibrinogeno intatto può penetrare in una parete aortica indebolita, calmare un percorso di segnalazione dannoso nelle cellule muscolari lisce e aiutarle a rimanere forti e contrattili. Per i pazienti, ciò apre la possibilità che infusioni di fibrinogeno, dosate con cura, possano un giorno diventare un trattamento farmacologico per rallentare la dissezione aortica e allungare in sicurezza la finestra per un intervento chirurgico programmato salvavita.
Citazione: Zhong, X., Li, D., Zhao, Y. et al. Fibrinogen–Bmal1 signaling as a therapeutic target to limit aortic dissection by preserving VSMC contractility. Sig Transduct Target Ther 11, 103 (2026). https://doi.org/10.1038/s41392-026-02610-x
Parole chiave: dissezione aortica, fibrinogeno, cellule muscolari lisce vascolari, segnalazione Bmal1, aneurisma aortico