Clear Sky Science · it
M6A-modificato circArhgap26 attenua il danno da ischemia‒ripervenimento cardiaco sopprimendo la palmitoilazione di plakophilin-1
Perché è importante proteggere il cuore dopo un infarto
Quando una persona subisce un infarto, i medici si affrettano a ricanalizzare l’arteria ostruita per ripristinare il flusso sanguigno. Questo intervento salva vite, ma ha anche un lato negativo: il ritorno improvviso del sangue può danneggiare ulteriormente il cuore, un problema noto come lesione da ischemia–ripervenimento. Lo studio qui riassunto esplora un inatteso difensore naturale all’interno delle cellule cardiache — un frammento circolare di RNA chiamato circArhgap26 — che aiuta a proteggere il muscolo cardiaco da questa seconda ondata di danno. Capire come funziona questa piccola molecola potrebbe indicare nuove terapie e test ematici per i pazienti con malattie cardiache.
Un cerchio nascosto nello script genetico del cuore
La maggior parte di noi pensa ai geni come a filamenti lineari di DNA e RNA, ma le cellule producono anche molecole di RNA a forma di anello, dette RNA circolari, che sono particolarmente stabili e possono modulare molti processi cellulari. I ricercatori hanno cercato nei cuori di topo gli RNA circolari che cambiano durante il danno cardiaco e si sono concentrati su uno, circArhgap26, i cui livelli calavano drasticamente quando il flusso sanguigno veniva interrotto e poi ripristinato. Hanno confermato che questo RNA circolare forma un loop chiuso, si trova principalmente nel compartimento citosolico della cellula e non funge da stampo per la sintesi proteica. Sembra invece agire come regolatore, interagendo con altre molecole per influenzare se una cellula cardiaca sopravvive o muore dopo uno stress. 
Prove che l’RNA circolare protegge il cuore
Per capire cosa fa realmente circArhgap26, il gruppo ha aumentato o ridotto i suoi livelli nei cuori di topo. Quando hanno usato un virus per aumentare circArhgap26 specificamente nei cardiomiociti, gli animali sottoposti a un’occlusione temporanea di un’arteria coronaria seguita da ripristino del flusso mostravano una funzione di pompa cardiaca migliore, aree danneggiate più piccole e un numero inferiore di cellule in morte. Anche i marcatori classici di danno nel sangue e nel tessuto cardiaco risultavano più bassi. L’opposto accadeva quando l’RNA circolare veniva silenziato: anche senza un infarto indotto, la funzione cardiaca peggiorava e la morte cellulare aumentava, e questi problemi si aggravavano ulteriormente con l’aggiunta dell’ischemia–ripervenimento. Effetti protettivi simili comparivano in cellule cardiache umane simulate in laboratorio, suggerendo che il meccanismo sia conservato tra topi e uomini.
Un partner proteico dannoso tenuto sotto controllo
Approfondendo, i ricercatori hanno indagato come circArhgap26 eserciti questa protezione. Usando tecniche biochimiche di “pesca”, hanno scoperto che si lega direttamente a una proteina strutturale chiamata plakophilin‑1 (PKP1), che può influenzare quanto saldamente le cellule si attaccano tra loro e quanto facilmente entrano in morte programmata. Nei cuori lesionati e nelle cellule cardiache sotto stress, i livelli di PKP1 aumentavano ed erano associati a danni maggiori. Il silenziamento di PKP1 attenuava il danno cardiaco e la morte cellulare, mentre la sua sovraespressione peggiorava gli esiti. Quando circArhgap26 veniva aumentato, la quantità di proteina PKP1 diminuiva pur senza cambiamenti nell’attività del gene, suggerendo un controllo a valle della sintesi dell’RNA. Esperimenti hanno mostrato che circArhgap26 accelera la degradazione della proteina PKP1 interferendo con un processo di modificazione lipidica chiamato palmitoilazione che normalmente stabilizza PKP1.
Una contesa molecolare sui segnali di morte cellulare
La palmitoilazione è catalizzata da una famiglia di enzimi; uno in particolare, ZDHHC1, è stato identificato come responsabile dell’aggiunta di gruppi grassi a PKP1 rendendola più stabile. CircArhgap26 si lega a PKP1 nella stessa regione utilizzata da ZDHHC1, creando una contesa molecolare. Quando l’RNA circolare prevale, PKP1 riceve meno tag lipidici, diventa meno stabile e viene eliminata più rapidamente. Ciò ha un effetto a catena: PKP1 normalmente potenzia la produzione di un’altra proteina, APAF1, interagendo con una regione di controllo del suo RNA. APAF1 è una componente chiave del macchinario che attiva le caspasi‑9 e caspasi‑3, gli esecutori principali della morte cellulare. Con PKP1 meno stabile, la sintesi di proteina APAF1 diminuisce, la cascata di segnalazione della morte è attenuata e le cellule cardiache hanno maggiori probabilità di sopravvivere allo stress del ripristino del flusso sanguigno. 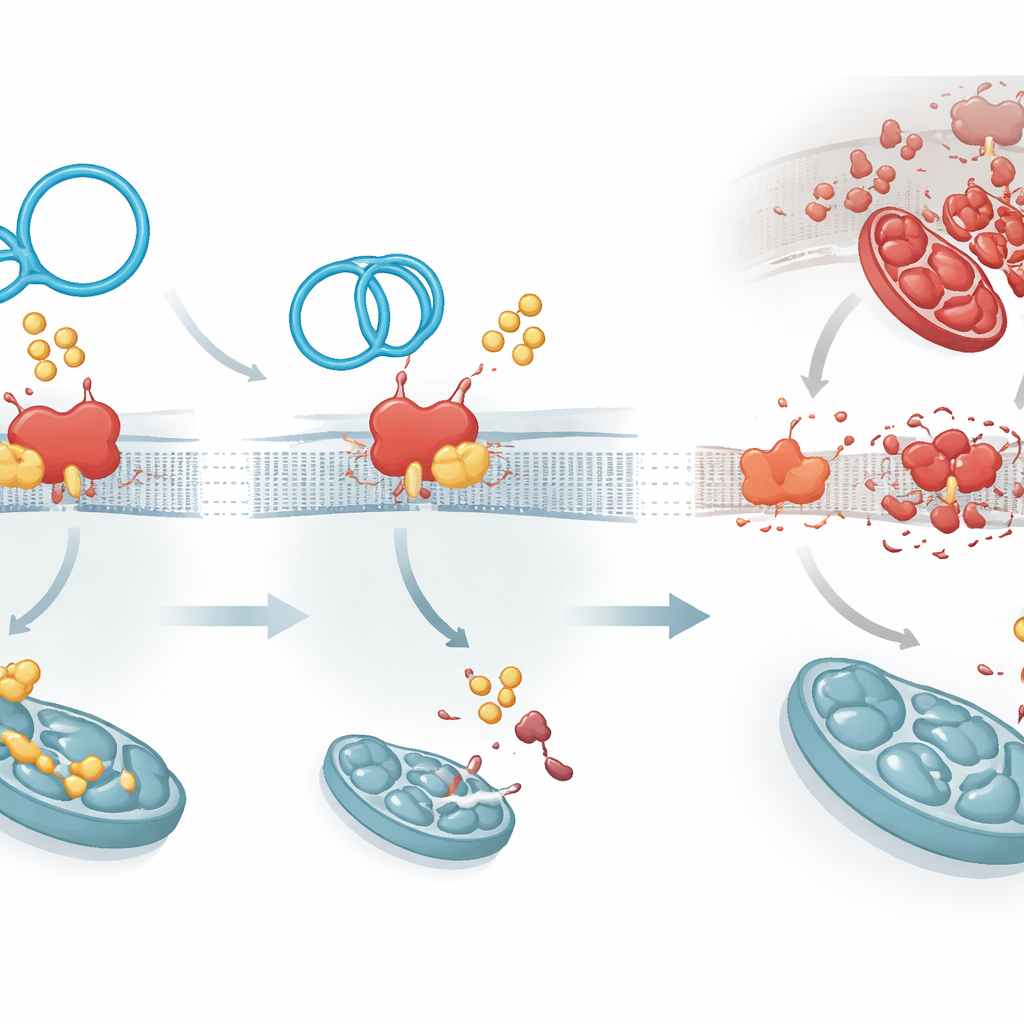
Regolazione del cerchio e prospettive per i pazienti
Lo studio rivela anche come circArhgap26 venga ridotto durante il danno. Un comune segnale chimico sull’RNA, chiamato m6A, si accumula su questo RNA circolare nei cuori sotto stress. Una proteina “lettore” chiamata YTHDF2 riconosce questa modifica e promuove la degradazione di circArhgap26, indebolendo la difesa naturale del cuore proprio quando è più necessaria. È importante che la versione umana di questo RNA circolare sia molto simile a quella murina ed è significativamente più bassa nel sangue dei pazienti sottoposti a procedure di ricanalizzazione rispetto a volontari sani. Complessivamente, questi risultati suggeriscono che ripristinare o imitare circArhgap26 potrebbe sia servire come biomarcatore ematico di rischio sia costituire una nuova terapia. In termini chiari, il lavoro scopre una piccola molecola circolare che funge da guardiano contro il danno da ripervenimento disinnescando una catena di reazioni letali all’interno delle cellule cardiache.
Citazione: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Parole chiave: lesione da ischemia-ripervenimento, RNA circolare, infarto, apoptosi dei cardiomiociti, terapia a base di RNA