Clear Sky Science · it
La sinergia chemo‑fototermica accende l’immunità antitumorale tramite ferroptosi
Trasformare il calore e la luce del corpo in un’arma contro il cancro
I farmaci chemioterapici possono ridurre i tumori, ma spesso comportano effetti collaterali intensi e non sempre impediscono la recidiva. Questo studio esplora un nuovo modo per rendere un farmaco esistente, il docetaxel, più efficace e intelligente, incapsulandolo in piccole particelle sensibili al calore e attivandole con luce nel vicino infrarosso. L’obiettivo non è solo uccidere le cellule tumorali in modo più preciso, ma anche risvegliare il sistema immunitario così che possa riconoscere e eliminare il cancro in tutto il corpo e prevenire future ricadute. 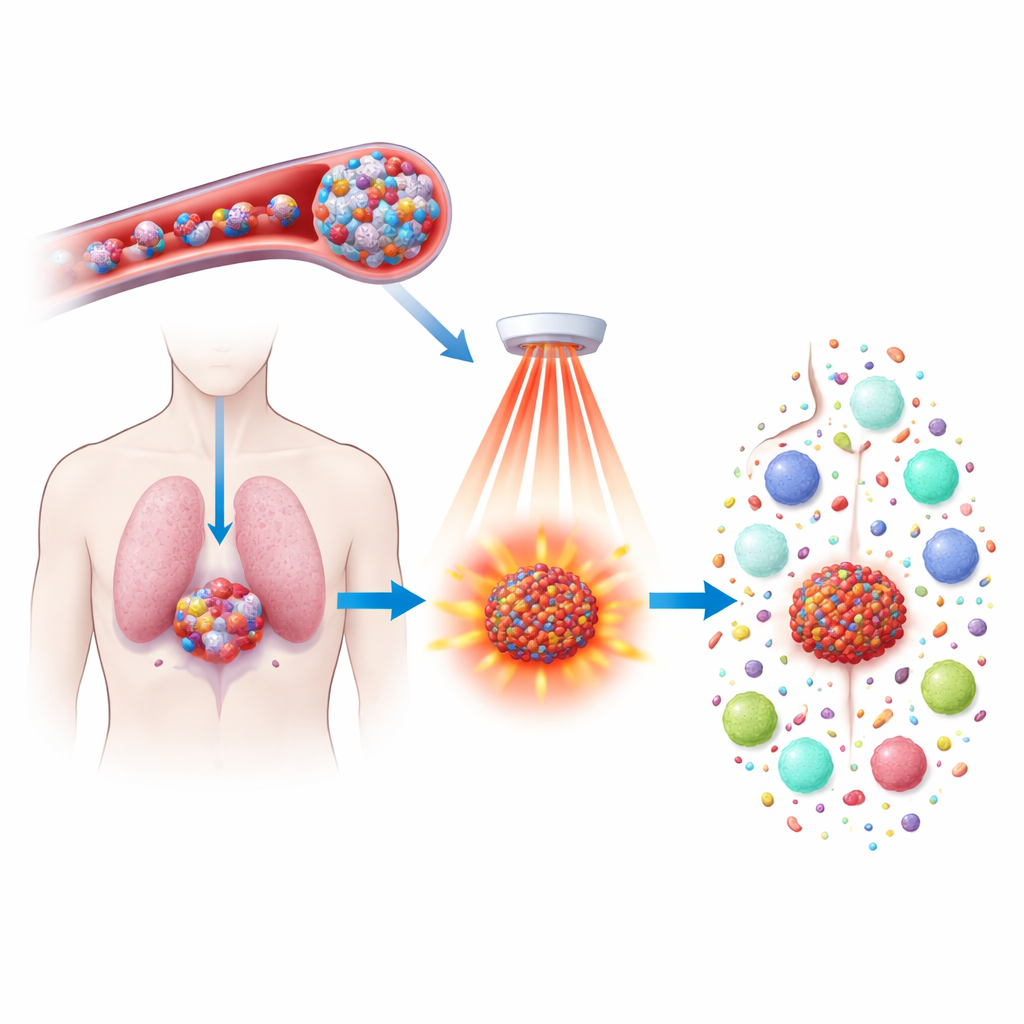
Piccoli corrieri che sanno dove andare
I ricercatori hanno realizzato un nuovo tipo di nanoparticella a partire da un polimero contenente ferrocene, una molecola contenente ferro che reagisce intensamente con il perossido di idrogeno—un ossidante presente in quantità maggiori nei tumori rispetto ai tessuti normali. Questi polimeri si autoassemblano in sfere idrofile capaci di trasportare sia docetaxel sia un colorante assorbente della luce chiamato IR808. Una volta iniettate nel flusso sanguigno, le particelle sono sufficientemente piccole e stabili da circolare e infiltrarsi nei tumori, dove i vasi sanguigni permeabili e gli alti livelli di perossido di idrogeno cominciano a degradarle e a rilasciare lentamente il loro carico. Questo design concentra il trattamento nel tumore limitando al contempo i danni agli organi sani.
Usare la luce per potenziare il danno locale
La luce nel vicino infrarosso, che può penetrare i tessuti in sicurezza, viene quindi indirizzata verso l’area tumorale. L’IR808 all’interno delle nanoparticelle assorbe questa luce e la converte in calore generando allo stesso tempo specie reattive dell’ossigeno. La combinazione tra il perossido di idrogeno prodotto dal tumore e gli ossidanti indotti dalla luce fa sì che le particelle si disfino più rapidamente e rilascino il farmaco proprio dove serve. Contemporaneamente, il ferro nel segmento di ferrocene aiuta a trasformare questi ossidanti in forme particolarmente aggressive che attaccano i componenti lipidici delle membrane cellulari. Questo assalto chimico e termico mirato aumenta nettamente il potere letale rispetto al solo docetaxel o al solo trattamento con luce. 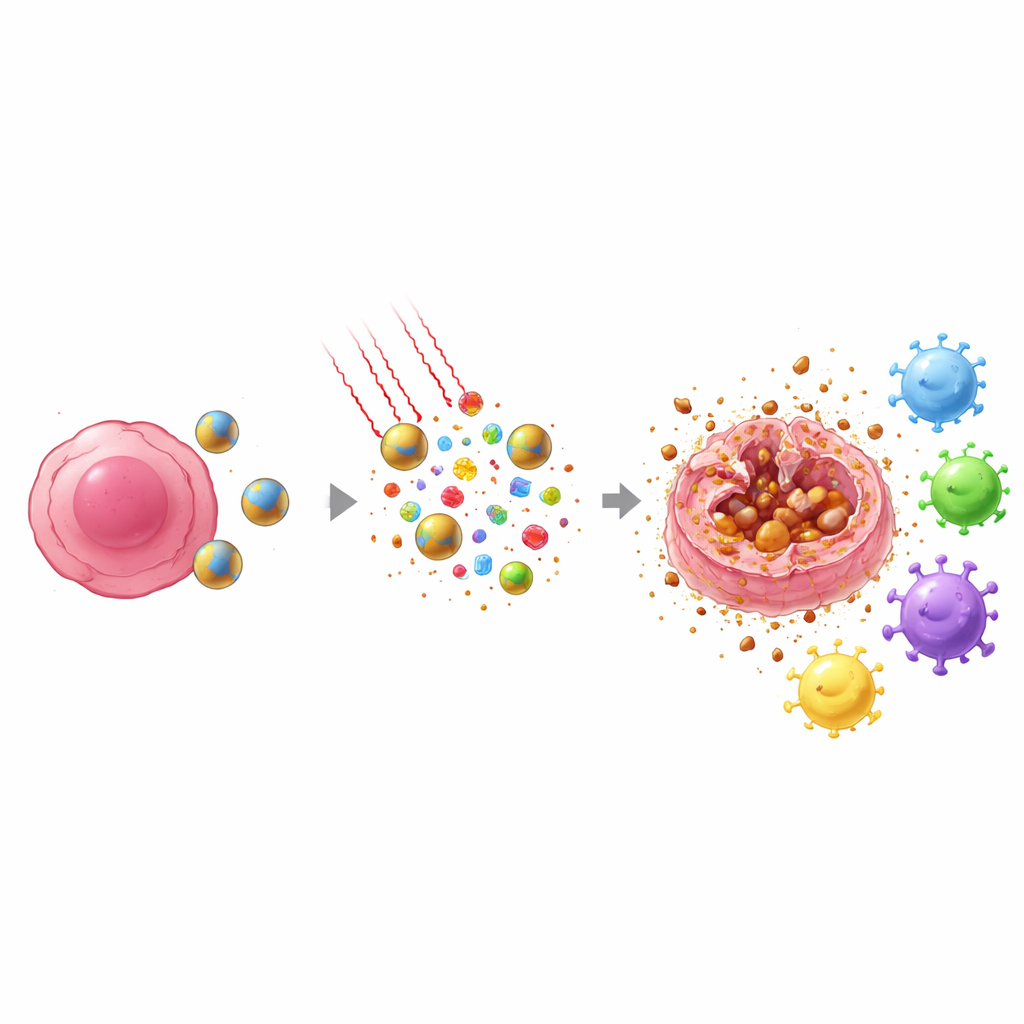
Un “bruciamento” controllato che segnala il sistema immunitario
È importante notare che il modo in cui le cellule tumorali muoiono con questo trattamento è diverso dalla chemioterapia ordinaria. Anziché degradarsi silenziosamente in frammenti ordinati, molte cellule vanno incontro a un processo chiamato ferroptosi, una forma di morte guidata dal ferro che danneggia i lipidi e in cui la membrana esterna si rompe. Quando ciò avviene, le cellule riversano segnali di allarme interni e frammenti tumorali nell’ambiente circostante. Allo stesso tempo, il docetaxel spinge una proteina nucleare chiave, HMGB1, verso il bordo cellulare, predisponendola al rilascio. Insieme, calore, ossidanti e azione farmacologica creano un’esplosione di segnali di pericolo e antigeni che le sentinelle immunitarie vicine—le cellule dendritiche—possono rilevare e trasportare ai linfonodi.
Dall’attacco locale alla difesa sistemica
Nei modelli tumorali murini, questo trattamento chemo‑fototermico combinato non solo ha ridotto i tumori direttamente riscaldati in modo più efficace di ciascun singolo componente, ma ha anche modificato il paesaggio immunitario. I tumori hanno mostrato un numero maggiore di cellule dendritiche mature e un incremento dei linfociti T citotossici, sia nel tumore stesso sia nei linfonodi drenanti. In alcuni topi immunocompetenti, i tumori primari sono scomparsi dopo sole due cicli di trattamento. Quando gli scienziati hanno poi impiantato nuovi tumori in siti distanti o nella zampa opposta, queste crescite secondarie sono state rallentate o soppresse, indicando che gli animali avevano sviluppato una forma di memoria immunitaria specifica per il cancro. L’aggiunta di un anticorpo che blocca i checkpoint e previene l’esaurimento dei linfociti T ha ulteriormente ridotto le metastasi polmonari e prolungato la sopravvivenza, suggerendo che questo trattamento locale può essere combinato con le moderne immunoterapie.
Perché questo è importante per la cura del cancro in futuro
Per un non specialista, il punto chiave è che questo approccio trasforma il docetaxel da veleno sistemico grezzo a parte di una strategia anti‑tumorale intelligente e multistep. Incapsulando il farmaco in nanoparticelle attivabili dalla luce e contenenti ferro che rispondono alla chimica stessa del tumore, la terapia provoca più danno all’interno dei tumori risparmiando i tessuti sani. Il particolare schema di morte cellulare che induce funziona come un vaccino dall’interno del tumore, insegnando al sistema immunitario a riconoscere e ricordare il cancro. Se questi risultati si traducessero nell’uomo, tali sistemi chemo‑fototermici potrebbero contribuire a convertire tumori “freddi” resistenti in tumori “caldi” più reattivi ai trattamenti basati sul sistema immunitario, riducendo potenzialmente le recidive e migliorando il controllo a lungo termine.
Citazione: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Parole chiave: nanomedicina oncologica, terapia fototermica, ferroptosi, immunoterapia oncologica, consegna di docetaxel