Clear Sky Science · it
Prodrug nanozymico a coordinazione conduttiva innesca con precisione piroptosi, cuprotosi e ferroptosi per una vaccinazione antitumorale in situ
Trasformare i tumori nei propri vaccini
Il trattamento del cancro di solito mira a uccidere direttamente le cellule tumorali, ma cosa succederebbe se un tumore potesse essere trasformato in un vaccino contro se stesso? Questo studio descrive un «prodrug» nanoparticellare intelligente che viaggia in sicurezza nell’organismo, si attiva solo all’interno dei tumori e induce le cellule cancerose a morire in modo da allertare potentemente il sistema immunitario. Il risultato non è solo la riduzione del tumore primario, ma anche l’addestramento dell’organismo a cercare e distruggere tumori e metastasi distanti.
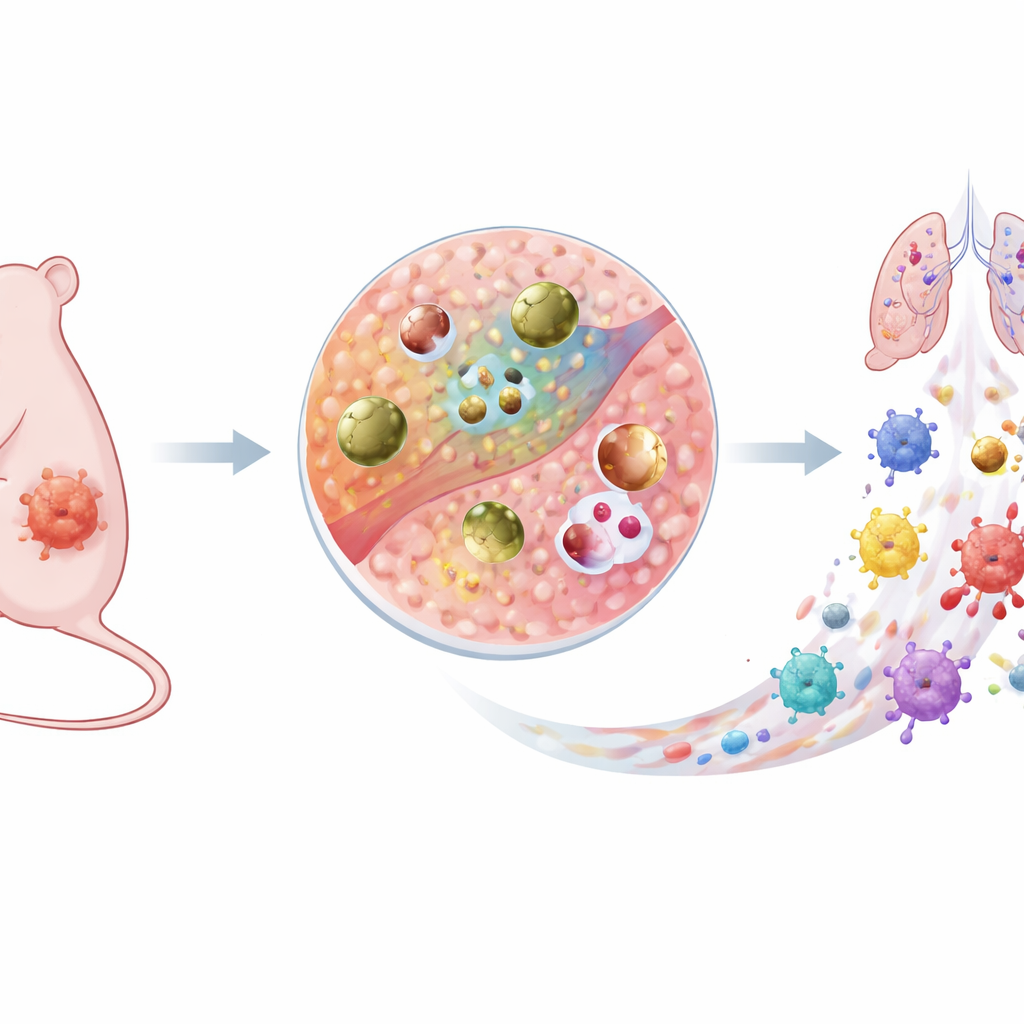
Una nuova arma intelligente contro il cancro
I ricercatori hanno costruito una minuscola particella a base di rame chiamata Cu–DHN che si comporta come un farmaco dormiente durante la circolazione e come un aggressivo agente antitumorale una volta raggiunto il tumore. È assemblata da ioni rame, un precursore innocuo (1,5-diidrossinaftalene, o DHN) e l’amminoacido cisteina. Insieme formano una rete di coordinazione conduttiva, per cui gli elettroni possono muoversi facilmente attraverso la particella. Questa «autostrada elettronica» interna permette all’intero nanoparticolo, non solo alla sua superficie, di partecipare a reazioni chimiche. Elemento cruciale: Cu–DHN è progettato per rispondere solo alla chimica anomala del microambiente tumorale, dove glutatione e perossido di idrogeno sono entrambi anormalmente elevati.
Come la chimica tumorale aziona l’interruttore
All’interno dei tumori, Cu–DHN agisce come un enzima artificiale. In presenza contemporanea di glutatione e perossido di idrogeno, prima utilizza il glutatione per riportare gli ioni rame in uno stato altamente reattivo e poi sfrutta il perossido di idrogeno per generare un flusso continuo di ossidanti estremamente aggressivi (radicali ossidrilici). Questi ossidanti svolgono una doppia azione: danneggiano componenti cellulari e trasformano il DHN innocuo intrappolato nella particella in juglone, un potente composto antitumorale. Il juglone, a sua volta, sopprime le difese antiossidanti del tumore e aumenta ulteriormente i livelli di perossido di idrogeno, creando un circuito autoamplificato di stress ossidativo che rimane confinato al tumore, perché solo il microambiente tumorale fornisce gli input chimici necessari per avviare il ciclo.
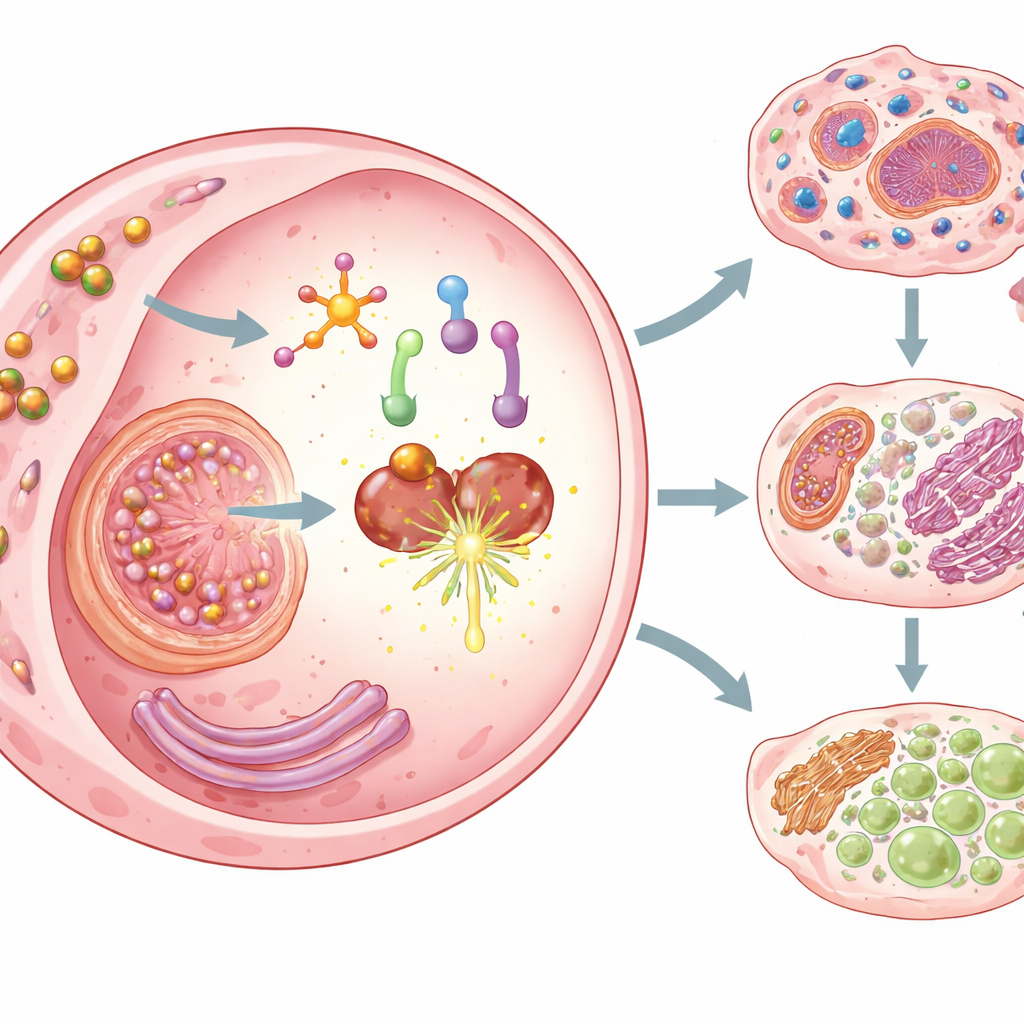
Innescare tre forme di morte delle cellule tumorali
Una volta attivato, Cu–DHN non si limita a tossicizzare le cellule cancerose. Innesca tre forme regolate di morte cellulare particolarmente visibili al sistema immunitario. Innanzitutto, il juglone inverte la silenziamento epigenetico di una proteina poretica chiamata gasdermina D e attiva un complesso sensore infiammatorio, portando le cellule alla piroptosi—una forma di morte drammatica che fa esplodere la membrana e riversare il contenuto interno. In secondo luogo, il rame trasportato dalle nanoparticelle, assorbito efficientemente dalle cellule tumorali, induce la cuprotosi, una forma di morte legata all’accumulo tossico di rame nelle macchine metaboliche chiave. Terzo, deplezionando il glutatione e disattivando un enzima protettivo (GPX4), Cu–DHN favorisce la ferroptosi, una morte guidata dalla perossidazione lipidica. Insieme, questi meccanismi garantiscono che le cellule tumorali non vengano solo eliminate in modo efficiente ma muoiano in una maniera particolarmente immunogenica.
Dall’attacco locale alla difesa sistemica
La piroptosi e il danno ossidativo associato inducono le cellule tumorali a rilasciare un’ondata di segnali d’allarme: antigeni associati al tumore, molecole di pericolo come ATP e HMGB1 e marcatori di stress sulla loro superficie. In modelli murini di carcinoma mammario aggressivo, una singola iniezione di Cu–DHN nel tumore primario ha portato a una forte attivazione delle cellule dendritiche nei linfonodi vicini e a un’impennata di linfociti CD8 cacciatori di tumori. Queste cellule immunitarie si sono poi spostate verso tumori non trattati sul lato opposto del corpo e verso i polmoni, dove hanno rallentato o quasi prevenuto la crescita di nuovi tumori e noduli metastatici. Il blocco dei linfociti CD8 ha sostanzialmente eliminato questa protezione, confermando che Cu–DHN trasforma il tumore primario in un vaccino in situ che insegna al sistema immunitario a riconoscere e distruggere il cancro altrove.
Effetti potenti con un profilo di sicurezza migliore
Una preoccupazione importante delle terapie basate sulla piroptosi è il rischio di danneggiare i tessuti normali, che esprimono anch’essi le stesse proteine poretiche. Quando il juglone viene somministrato direttamente nella sua forma attiva, i topi manifestano tossicità significativa per fegato, reni e sangue. Al contrario, Cu–DHN rimane inattivo nei tessuti sani, poiché questi ultimi non possiedono la combinazione di inneschi chimici necessari per attivare la particella. Nei topi, Cu–DHN ha eguagliato il potere citotossico e anti-metastatico del juglone attivo evitando danni agli organi, anomalie ematiche e perdita di peso. In termini semplici, questo lavoro mostra come una nanoparticella conduttiva e intelligente possa restare silente nell’organismo, risvegliarsi solo all’interno dei tumori, costringere le cellule cancerose a morire in modo immunostimolante e fungere così da piattaforma vaccinale antitumorale precisa e autosufficiente.
Citazione: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
Parole chiave: immunoterapia del cancro, nanomedicina, piroptosi, vaccini antitumorali, microambiente tumorale