Clear Sky Science · it
Il profilo spazio-temporale rivela dinamiche e regolazioni di checkpoint distinte di cellule CAR-T e CAR-NKT contro tumori solidi
Perché questa ricerca è importante per la cura del cancro futura
Molti hanno sentito parlare delle cellule CAR-T, una terapia d’avanguardia in cui le cellule immunitarie del paziente vengono ingegnerizzate per ricercare e distruggere il cancro. Queste terapie funzionano in modo straordinario nei tumori ematologici, ma hanno incontrato difficoltà contro i tumori solidi come quelli ovarici, polmonari o pancreatici. Lo studio pone una domanda semplice ma cruciale: esiste un tipo di cellula immunitaria migliore per questo compito? Confrontando le tradizionali cellule CAR-T con un diverso tipo ingegnerizzato chiamato CAR-NKT, i ricercatori tracciano come ciascuna si comporta nell’organismo nel tempo e suggeriscono come rendere le prossime generazioni di terapie cellulari “off-the-shelf” più sicure ed efficaci per i tumori solidi.
Due tipi di cellule anti-cancro costruite su misura
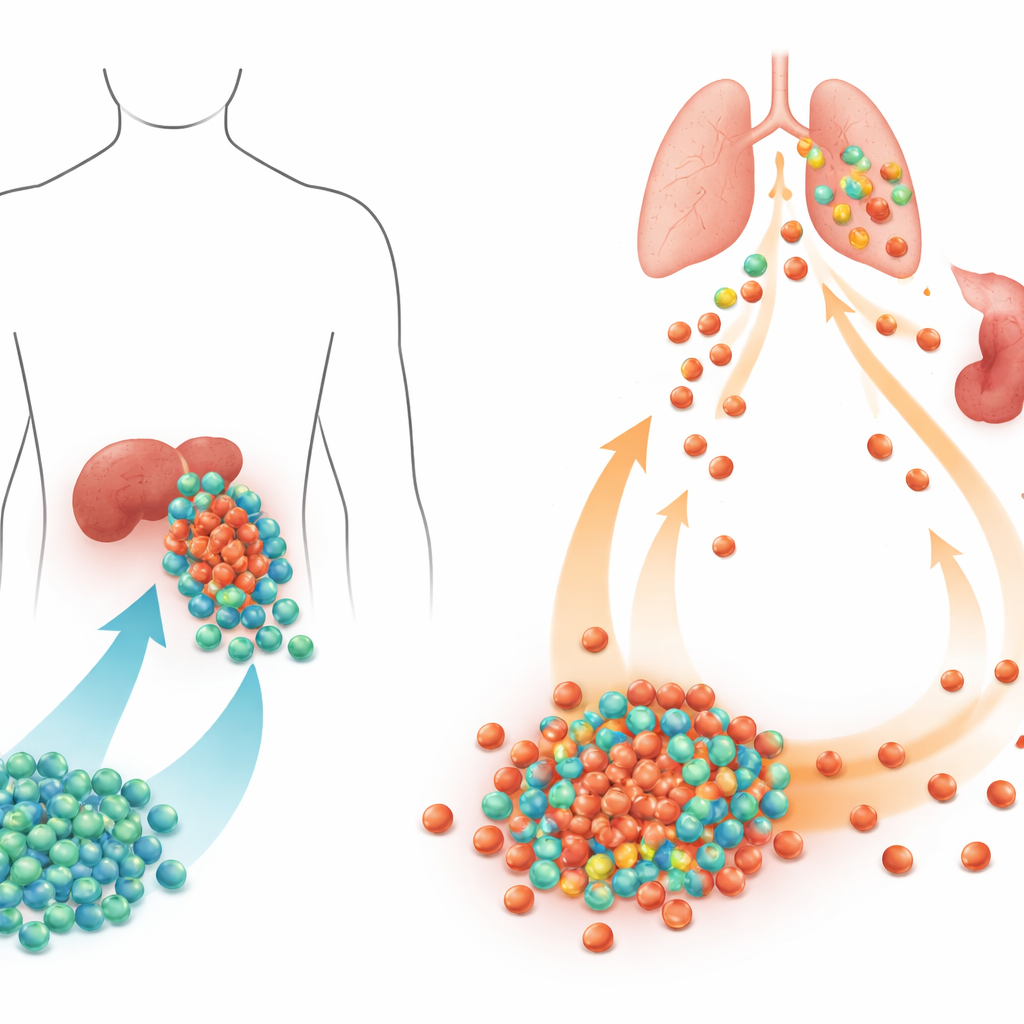
Il team ha creato due terapie che riconoscono lo stesso marcatore tumorale, la mesotelina, presente comunemente nei tumori ovarici e in altri tumori solidi. Le cellule CAR-T convenzionali sono state ottenute da linfociti T del sangue adulto, analoghe a quelle impiegate nei prodotti clinici attuali. Le CAR-NKT, invece, sono state generate da cellule staminali del sangue cordonale differenziate in un sottogruppo immunitario specializzato chiamato invariant natural killer T cells, quindi dotate sia di un recettore mirato al tumore sia di una riserva incorporata del fattore di crescita IL-15. Mentre le CAR-T attaccano principalmente tramite il recettore ingegnerizzato, le CAR-NKT possono uccidere in più modi contemporaneamente: tramite la CAR, tramite il loro recettore T naturale e tramite potenti recettori di tipo natural killer. In colture di laboratorio, le CAR-NKT hanno distrutto un’ampia gamma di linee cellulari di cancro ovarico, incluse quelle con poca o nessuna mesotelina, mentre le CAR-T erano per lo più limitate ai tumori con forte espressione del bersaglio.
Migliore controllo tumorale con meno effetti sistemici
Quando testate in topi portatori di tumori ovarici umani, il contrasto è diventato ancora più evidente. Entrambe le terapie sono state iniettate nella cavità addominale, dove i tumori crescevano. Le CAR-T inizialmente rallentavano la crescita tumorale ma alla fine si sono diffuse ampiamente nell’organismo e si sono espanse in modo esplosivo, causando una malattia simile al graft-versus-host e la morte in tutti gli animali trattati. Le CAR-NKT, invece, si sono concentrate efficacemente sui tumori, si sono espanse in modo controllato, hanno eliminato il cancro e poi si sono gradualmente contratte restando rilevabili per più di 100 giorni. Sono rimaste in gran parte confinate all’area tumorale invece di invadere gli organi sani, e i topi non hanno sviluppato le tossicità gravi osservate con le CAR-T. Gli autori hanno anche mostrato che aggiungere IL-15 alle CAR-T aumentava la loro potenza ma peggiorava molto gli effetti collaterali, mentre le CAR-NKT ingegnerizzate con IL-15 guadagnavano in persistenza senza scatenare infiammazione pericolosa.
Come localizzazione, metabolismo e memoria distinguono le CAR-NKT
Per capire perché queste due terapie si comportano in modo così diverso, i ricercatori hanno profilato centinaia di migliaia di singole cellule prelevate da tumori, sangue, milza e fegato nel corso di diverse settimane. Le CAR-NKT presentavano un pattern di recettori per chemochine che favoriva la permanenza nei tessuti infiammati e nei tumori, piuttosto che la ricircolazione attraverso i linfonodi. All’interno dei tumori, assumevano stati effetti e di tipo memoria durevoli con segni relativamente bassi di esaurimento e mantenevano vie energetiche robuste come la fosforilazione ossidativa e un metabolismo aminoacidico stabile. Le CAR-T, al contrario, mostravano spostamenti più erratici tra stati proliferativi, d’attacco e di esaurimento, specialmente nei tumori e nella milza, e i loro programmi metabolici erano meno stabili. Nel complesso, le CAR-NKT avanzavano più lentamente verso l’esaurimento terminale e conservavano maggiore flessibilità per continuare a combattere.
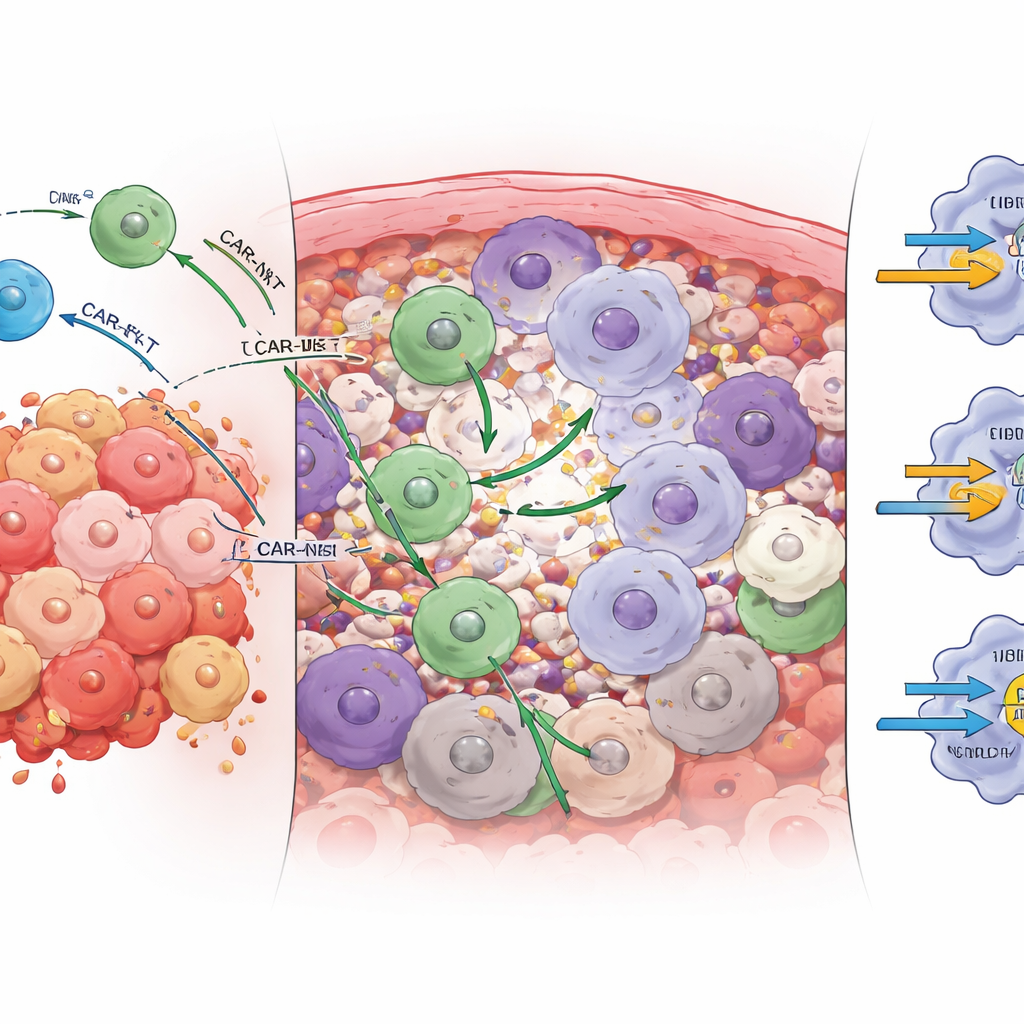
Diverse “frenate” controllano ciascuna terapia cellulare
L’ambiente tumorale usa i cosiddetti checkpoint immunitari—freni molecolari sulle cellule immunitarie—per attenuare gli attacchi. Analizzando come le cellule ingegnerizzate e le cellule tumorali comunicano tramite coppie recettore–ligando, lo studio ha rilevato che i freni dominanti non sono gli stessi per le CAR-T e le CAR-NKT. Nelle CAR-T, un’interazione inibitoria chiave coinvolgeva il recettore TIGIT sulle cellule immunitarie che si lega al suo partner sulle cellule tumorali. Nei topi, bloccare TIGIT migliorava significativamente il controllo tumorale e la sopravvivenza con le CAR-T. Le CAR-NKT, invece, risultavano principalmente ristrette da un recettore correlato chiamato CD96. Bloccare CD96—non TIGIT—incrementava il numero, l’attivazione e la capacità di eliminazione tumorale delle CAR-NKT. Il blocco tradizionale PD‑1/PD‑L1, che ha deluso in molti trial su tumori solidi, aveva poco effetto in questo modello, coerentemente con i bassi livelli di PD‑L1 nei tumori ovarici studiati.
Cosa significa per le terapie oncologiche di nuova generazione
Per un lettore non specialista, il messaggio principale è che non tutte le cellule immunitarie ingegnerizzate sono uguali. Le CAR-NKT, soprattutto se prodotte da cellule staminali come prodotti standardizzati off-the-shelf, hanno mostrato una capacità di uccisione tumorale più ampia, migliore capacità di raggiungere il tumore, memoria a lungo termine più solida e meno effetti collaterali pericolosi rispetto alle classiche CAR-T in questi modelli di tumori solidi. Altrettanto importante, lo studio rivela che ogni tipo cellulare è regolato da checkpoint dominanti propri—TIGIT per le CAR-T e CD96 per le CAR-NKT—individuando combinazioni farmacologiche più mirate invece di approcci universali. Nel loro insieme, questi risultati sostengono l’ipotesi che le CAR-NKT potrebbero costituire la spina dorsale di terapie cellulari più sicure e versatili per i tumori solidi difficili da trattare.
Citazione: Li, YR., Li, M., Chen, Y. et al. Spatiotemporal profiling reveals distinct dynamics and checkpoint regulations of CAR-T and CAR-NKT cells against solid tumors. Sig Transduct Target Ther 11, 92 (2026). https://doi.org/10.1038/s41392-026-02602-x
Parole chiave: Terapia con cellule CAR-NKT, Cellule CAR-T, Tumori solidi, Checkpoint immunitari, Immunoterapia cellulare