Clear Sky Science · it
La stabilizzazione mediata dall’ubiquitina di KDM5B guida la chemioresistenza tramite la repressione della fosfatasi a doppia specificità 4 nel cancro ovarico
Perché alcuni tumori ovarici smettono di rispondere alla chemioterapia
Molte donne con carcinoma ovarico rispondono inizialmente bene a farmaci a base di platino come il cisplatino, per poi affrontare la devastante ricomparsa di tumori che non reagiscono più al trattamento. Questo studio rivela un circuito molecolare nascosto all’interno delle cellule tumorali che le aiuta a diventare resistenti ai farmaci. Scoprendo come uno specifico “interruttore epigenetico” viene attivato e disattivato, i ricercatori indicano nuovi modi per prevedere quali tumori resisteranno alla terapia e come ri-sensibilizzarli ai farmaci esistenti.
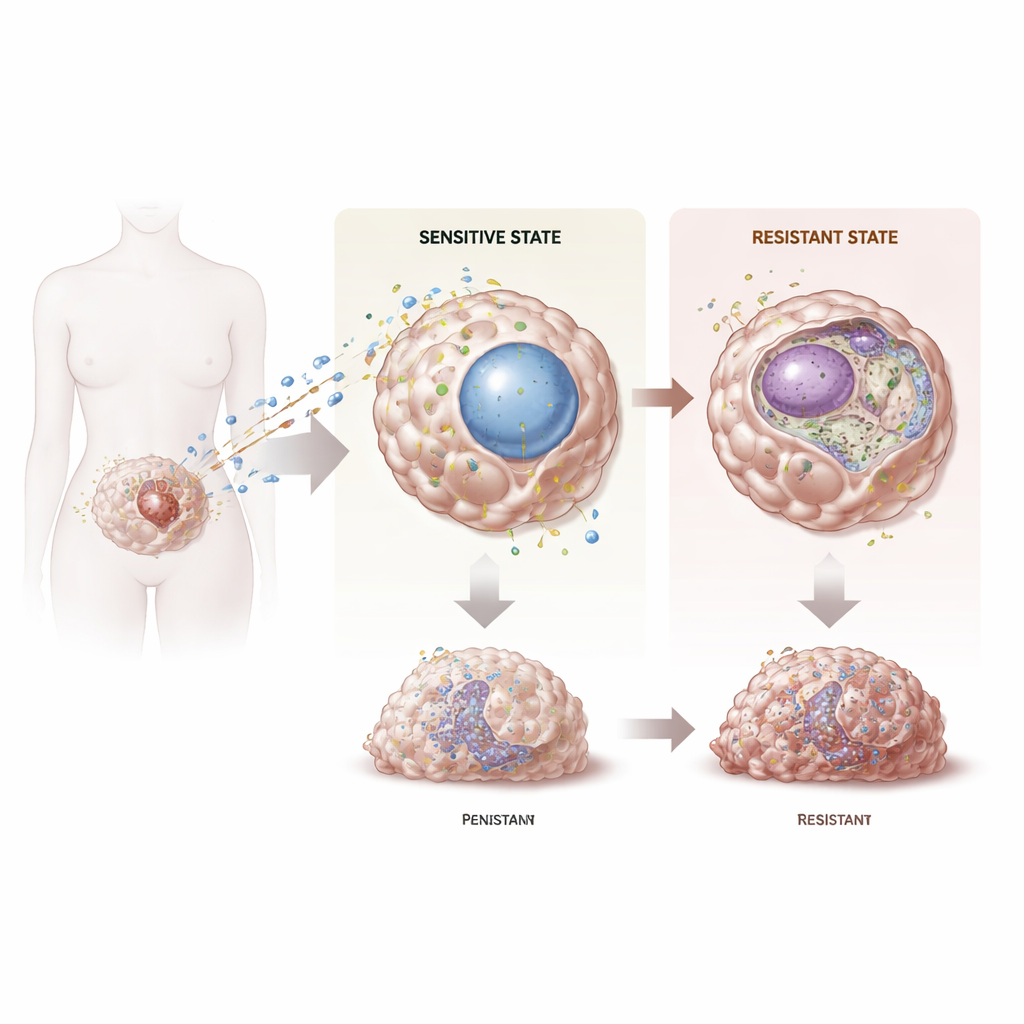
La tenace ricomparsa di un cancro letale
Il carcinoma ovarico è uno dei tumori ginecologici più letali in parte perché viene spesso diagnosticato in fase avanzata e perché la resistenza alla chemioterapia è comune. Sebbene fino all’80% delle pazienti benefici inizialmente della chemioterapia a base di platino, la maggior parte va incontro a recidiva con tumori che non rispondono più, lasciando poche opzioni efficaci e prognosi infauste. Lavori recenti hanno mostrato che i cambiamenti nel modo in cui il DNA è impacchettato e letto—cambiamenti epigenetici—possono aiutare le cellule tumorali ad adattarsi al trattamento. Gli autori si sono concentrati su una famiglia di enzimi chiamata KDM5, che modulano finemente l’attività genica rimuovendo marche chimiche dalle proteine istoniche che organizzano il DNA. Si sono chiesti se membri particolari di questa famiglia potessero essere cruciali per la resistenza al platino nel carcinoma ovarico.
Un enzima fa pendere la bilancia verso la resistenza
Analizzando grandi database di genomica del cancro e poi testando più linee cellulari di carcinoma ovarico, il team ha scoperto che un membro della famiglia KDM5, KDM5B, emerge nei tumori resistenti. I suoi livelli sono più alti nei carcinomi ovarici ricorrenti, nelle lesioni metastatiche e nelle linee cellulari che non rispondono più al cisplatino, mentre il suo parente stretto KDM5A non mostra lo stesso andamento. Quando i ricercatori hanno rimosso selettivamente KDM5B dalle cellule resistenti, queste sono tornate vulnerabili al cisplatino e hanno mostrato un aumento della morte cellulare programmata. L’aggiunta di KDM5B in eccesso a cellule inizialmente sensibili ha avuto l’effetto opposto, rendendole più difficili da eliminare con la chemioterapia. Questi risultati sono stati confermati in vari modelli cellulari indipendenti e in topi portatori di tumori ovarici umani, implicando con decisione KDM5B come un fattore guida della chemioresistenza.
Un freno alla segnalazione di crescita messo a tacere
Approfondendo, gli autori hanno indagato quali geni KDM5B stesse reprimendo per favorire la sopravvivenza delle cellule tumorali. Mediante sequenziamento dell’RNA e mappatura della cromatina, hanno scoperto che KDM5B reprime direttamente un gene chiamato DUSP4, che normalmente agisce come freno su una principale via di crescita e risposta allo stress nota come via MAPK. KDM5B si lega al promotore di DUSP4 ed elimina marche “di attivazione”, riducendo i livelli di DUSP4 e rilasciando di fatto il freno sulla segnalazione MAPK. Quando DUSP4 è ridotta, l’attività MAPK aumenta, promuovendo la crescita cellulare e aiutando le cellule a sopportare i danni al DNA indotti dal cisplatino. Ripristinare DUSP4 inverte questa resistenza, mentre la delezione di DUSP4 annulla i benefici derivanti dalla rimozione di KDM5B, sia in colture cellulari che in tumori murini. I dati dei pazienti rispecchiano queste osservazioni: i tumori con alto KDM5B e basso DUSP4 sono associati a una sopravvivenza peggiore.
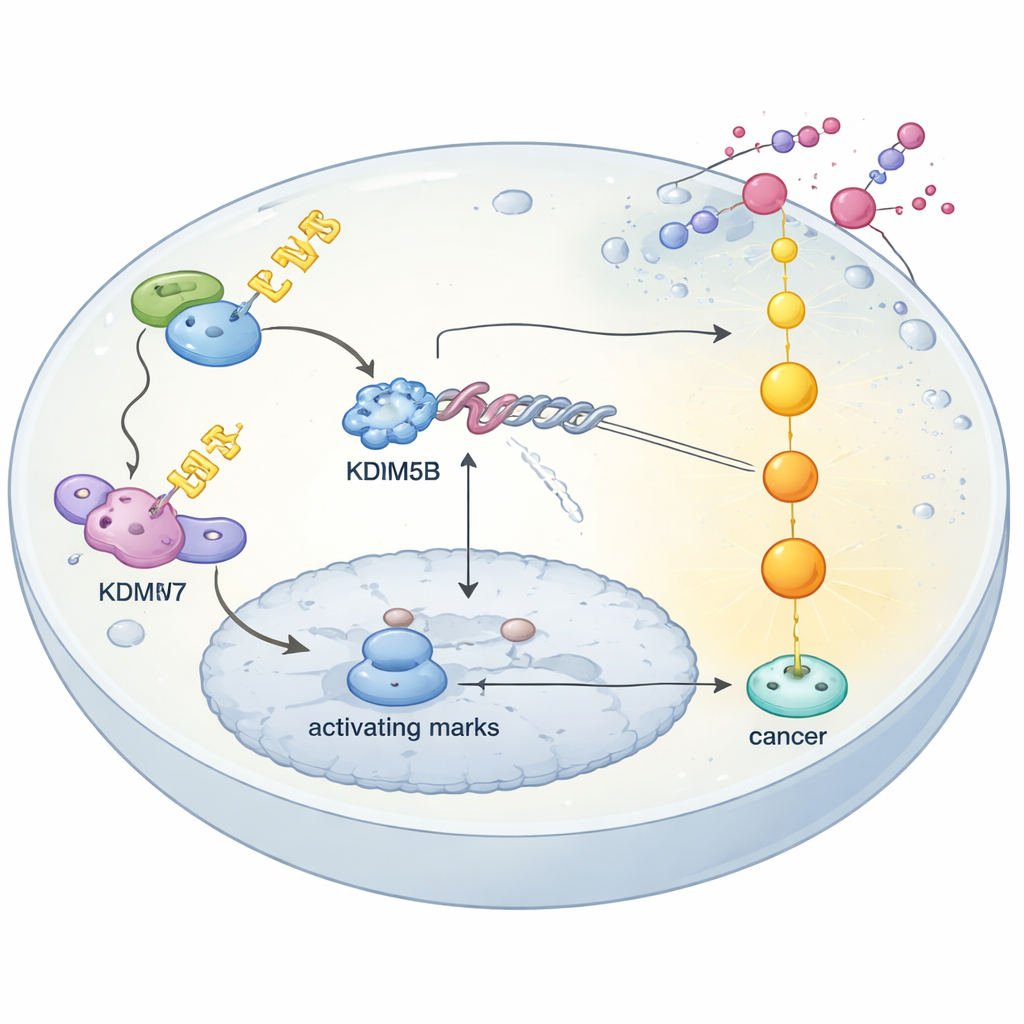
Il controllo qualità delle proteine modella la risposta ai farmaci
Lo studio rivela anche come le cellule tumorali stabilizzino KDM5B in primo luogo. All’interno delle cellule, molte proteine vengono continuamente etichettate per la distruzione o risparmiate da un sistema di controllo qualità basato su catene di ubiquitina. I ricercatori dimostrano che un enzima chiamato USP7 protegge KDM5B rimuovendo queste etichette, impedendone la degradazione. Quando USP7 è bloccato geneticamente o con un inibitore piccolo molecolare, i livelli di KDM5B calano e le cellule di carcinoma ovarico resistenti riacquistano sensibilità al cisplatino. Al contrario, un complesso ligasi E3 costruito attorno a una proteina chiamata FBXW7 riconosce KDM5B solo dopo che un altro enzima, HIPK1, lo fosforila in un sito specifico, segnalandolo per la distruzione. Interferire con questa via FBXW7–HIPK1 rende KDM5B più stabile. Complessivamente, la resistenza emerge quando il ruolo protettivo di USP7 prevale sul ruolo smaltitore di FBXW7, permettendo l’accumulo di KDM5B e mantenendo DUSP4 spenta.
Nuovi modi per aggirare i tumori ostinati
Mappando questo asse USP7–KDM5B–DUSP4–MAPK, gli autori forniscono una spiegazione coerente di come le cellule del carcinoma ovarico evolvano la resistenza al cisplatino. Per i non specialisti, il messaggio chiave è che il problema non è semplicemente un aumento delle mutazioni, ma anche una riorganizzazione del controllo genico e del turnover proteico. Il lavoro suggerisce diverse strategie verificabili: usare i livelli di KDM5B, USP7 e DUSP4 come biomarcatori per prevedere chi risponderà male alla terapia a base di platino, e combinare il cisplatino con farmaci che inibiscono KDM5B o USP7, o che potenziano la degradazione di KDM5B, per ripristinare la sensibilità ai farmaci. Sebbene questi approcci richiedano ancora validazione clinica, offrono un progetto promettente per trasformare alcuni carcinomi ovarici resistenti in tumori nuovamente trattabili.
Citazione: Yoo, J., Kim, G.W., Jeon, Y.H. et al. Ubiquitin-mediated stabilization of KDM5B drives chemoresistance via repression of dual-specificity phosphatase 4 in ovarian cancer. Sig Transduct Target Ther 11, 89 (2026). https://doi.org/10.1038/s41392-026-02601-y
Parole chiave: carcinoma ovarico, resistenza al cisplatino, regolazione epigenetica, KDM5B, segnalizzazione MAPK