Clear Sky Science · it
Nanoreattori enzimatici a cascata confinata ispirati alla natura per una terapia mirata dell’aterosclerosi
Combattere i tappi arteriosi con piccoli aiutanti intelligenti
L’aterosclerosi — arterie ostruite e infiammate — è una delle principali cause di infarto e ictus. Molte persone assumono già farmaci per abbassare il colesterolo, ma le placche pericolose possono comunque accumularsi e rimanere infiammate. Questo studio descrive un “nanoreattore” ispirato alla natura, una minuscola particella ingegnerizzata che imita le difese antiossidanti del nostro organismo per calmare le placche infiammate, eliminare molecole dannose e rallentare l’invecchiamento delle arterie in modelli animali. 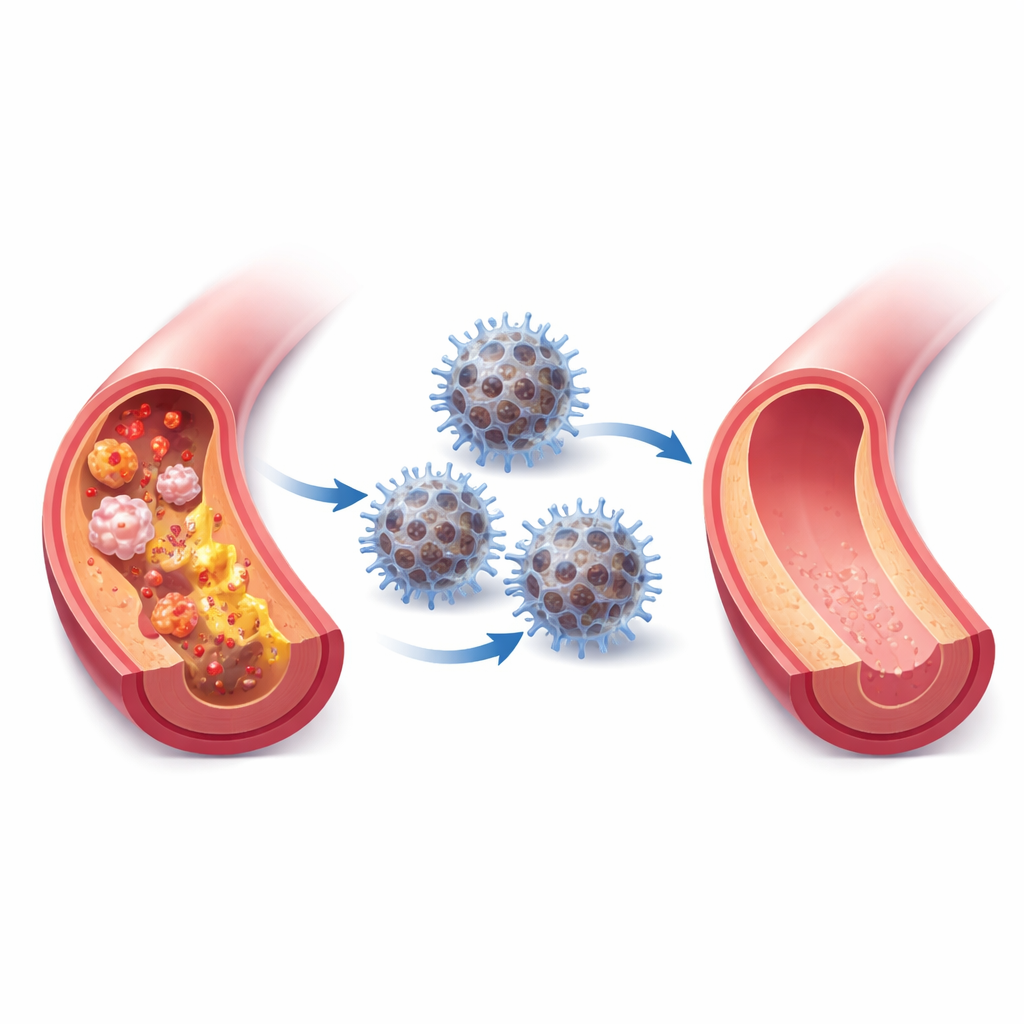
Perché le placche sono più che semplice grasso
I medici un tempo pensavano che le placche arteriose fossero principalmente dovute all’accumulo di colesterolo. Ora sappiamo che sono anche guidate dallo stress ossidativo e dall’infiammazione cronica. Nelle arterie malate, molecole instabili chiamate specie reattive dell’ossigeno danneggiano i lipidi, trasformando il colesterolo normale in una forma più dannosa che viene ingerita dalle cellule immunitarie, creando «cellule schiumose» e placche instabili. L’invecchiamento e lo stress delle cellule che rivestono i vasi aggiungono carburante al fuoco rilasciando segnali infiammatori. Gli enzimi naturali nei tessuti sani normalmente tengono sotto controllo queste molecole reattive, ma nelle placche l’equilibrio è perso e la semplice somministrazione di singoli antiossidanti non ha finora dato buoni risultati nei pazienti.
Prendere in prestito strategie dalle fabbriche enzimatiche della natura
Nelle cellule viventi, gli enzimi protettivi che neutralizzano le specie reattive dell’ossigeno spesso lavorano fianco a fianco in squadre compatte, trasferendo rapidamente intermedi dannosi da uno all’altro in una cascata. I ricercatori hanno voluto copiare questa strategia con materiali sintetici. Hanno costruito un nanoreattore a «cascata confinata» impacchettando particelle ultrasottili di blu di Prussia — che si comportano come diversi enzimi antiossidanti — all’interno di una sfera di silice dendritica a struttura spugnosa, drogata con selenio, un ingrediente chiave di un altro enzima antiossidante naturale. Questa struttura porosa concentra sia i catalizzatori sia i loro bersagli, permettendo una detossificazione graduale delle specie reattive dell’ossigeno più efficiente rispetto a quando ciascun componente è disperso singolarmente nel flusso sanguigno. 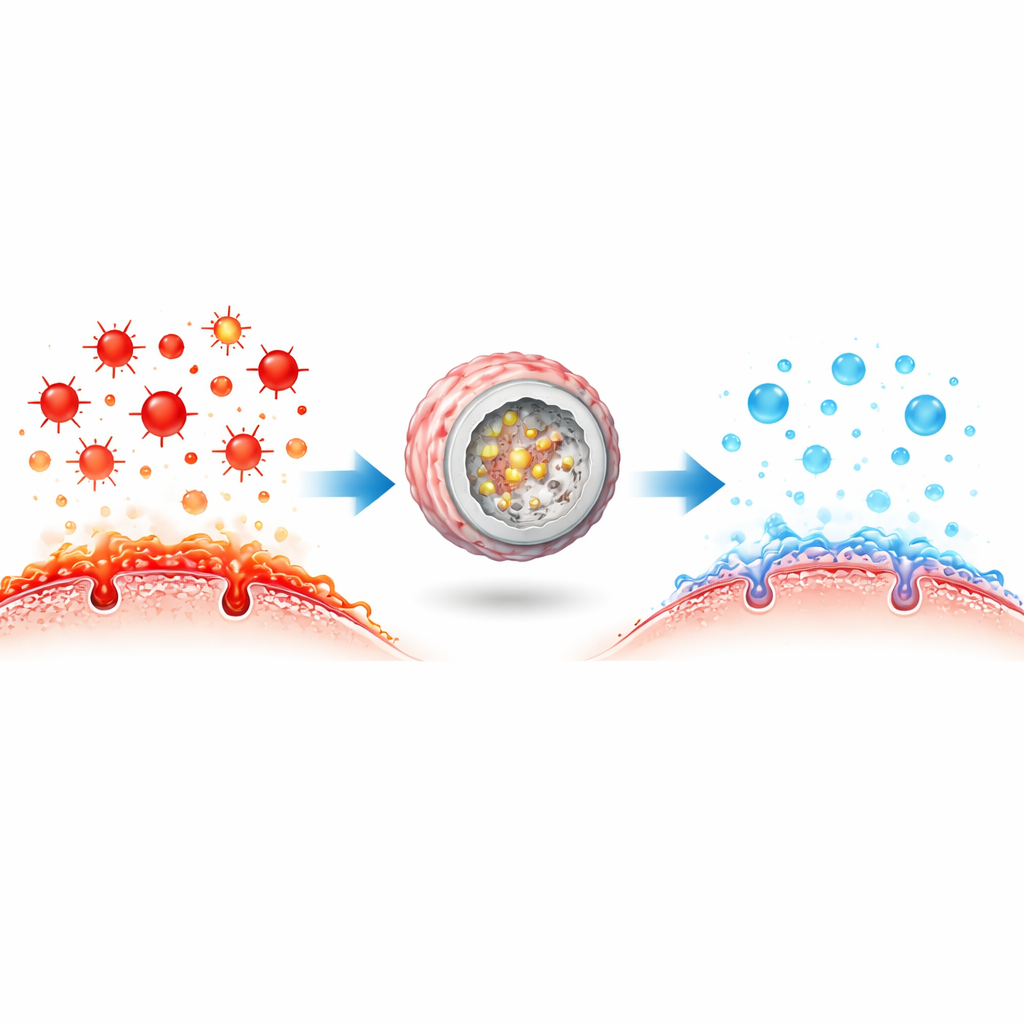
Dare ai nanoreattori la camuffatura dei neutrofili
Portare un farmaco nel punto giusto è una sfida importante. In questo lavoro, il gruppo ha rivestito i nanoreattori con membrane prelevate dai neutrofili, un tipo di globulo bianco naturalmente attratto dai siti infiammati. Questo mimetismo aiuta le particelle a circolare più a lungo, evitare una rapida eliminazione e indirizzarsi verso le placche, dove le cellule vascolari malate e le cellule immunitarie espongono marker di adesione corrispondenti. Negli esperimenti cellulari, questi nanoreattori rivestiti venivano assorbiti più facilmente dalle cellule endoteliali infiammate e dai macrofagi rispetto ai controlli non rivestiti, dimostrando che il «guscio» biologico li dirige attivamente verso le aree problematiche.
Calmare infiammazione, cellule schiumose e invecchiamento cellulare
Negli studi in vitro, i nanoreattori si sono dimostrati in grado di imitare più enzimi contemporaneamente, degradando diversi tipi di specie reattive dell’ossigeno e producendo prodotti innocui. Quando aggiunti a cellule immunitarie e cellule endoteliali infiammate, hanno ridotto drasticamente lo stress ossidativo, diminuito il rilascio di importanti messaggeri infiammatori e spinto i macrofagi da uno stato che favorisce il danno verso uno stato favorevole alla riparazione. Hanno anche ridotto l’accumulo di lipidi all’interno dei macrofagi, limitando la formazione di cellule schiumose, e protetto le cellule endoteliali da danni al DNA e segni di invecchiamento. Questi effetti erano più forti rispetto a quelli osservati con ciascun componente singolarmente, sottolineando l’importanza del design multistep e confinato.
Proteggere le arterie in un modello murino
Il team ha poi testato i nanoreattori rivestiti con membrane di neutrofili in topi geneticamente predisposti all’aterosclerosi e nutriti con una dieta ricca di grassi. Le particelle hanno circolato nel sangue per molte ore, si sono accumulate nelle placche e hanno mostrato un accumulo limitato negli organi sani. Dopo diverse settimane di trattamento, i topi che avevano ricevuto il nanoreattore completo presentavano aree di placca più piccole, meno cellule infiammatorie, più collagene stabilizzante e livelli più bassi di enzimi associati alla rottura della placca rispetto ai controlli o agli animali trattati con formulazioni più semplici. Le colorazioni tissutali hanno rivelato una riduzione dello stress ossidativo e meno cellule senescenti nella parete vascolare, il tutto senza segnali evidenti di tossicità o perdita di peso.
Cosa potrebbe significare per i futuri trattamenti cardiaci
Per un lettore non specialista, questo lavoro suggerisce un nuovo modo di affrontare la malattia arteriosa: invece di limitarsi ad abbassare il colesterolo o bloccare un singolo trigger infiammatorio, si utilizzano minuscole macchine ispirate alla natura per ripulire discretamente molecole dannose, raffreddare l’infiammazione e rallentare l’invecchiamento cellulare direttamente all’interno delle placche. Pur essendo ancora lontani dall’essere pronti per l’uso umano, questi nanoreattori a cascata confinata mostrano che combinare materiali intelligenti con una camuffatura biologica potrebbe offrire un approccio più mirato e potente per stabilizzare le arterie ostruite e, un giorno, ridurre il rischio di infarti e ictus.
Citazione: Wu, Y., Xia, H., Ding, H. et al. Nature-inspired confined cascade enzyme nanoreactors for targeted atherosclerosis therapy. Sig Transduct Target Ther 11, 84 (2026). https://doi.org/10.1038/s41392-026-02598-4
Parole chiave: aterosclerosi, nanomedicina, stress ossidativo, infiammazione, nanozima