Clear Sky Science · it
L’ablazione di DUSP6 ripristina la fitness delle cellule CAR T compromessa dalla perdita di CD58 nel tumore mediante il potenziamento del segnale AP-1
Perché potenziare le cellule che combattono il cancro è importante
Cellule immunitarie ingegnerizzate chiamate CAR T hanno trasformato il trattamento di alcuni tumori del sangue, eppure molti pazienti vanno incontro a recidiva perché i loro tumori imparano a eludere l’attacco. Questo studio svela una debolezza nascosta in alcuni tumori che disabilita silenziosamente le CAR T dall’interno — e mostra come una precisa modifica genetica possa ripristinare la resistenza, la riserva energetica e la capacità citotossica di queste cellule. Per il lettore, è uno sguardo su come le terapie cellulari di nuova generazione potrebbero diventare più durature ed efficaci per un maggior numero di persone.
Una maniglia mancante sulle cellule tumorali
Le CAR T hanno bisogno di un contatto saldo con il bersaglio per funzionare al meglio. Molte cellule tumorali esprimono una molecola di superficie chiamata CD58 che funge da “maniglia” per le cellule immunitarie, aiutandole ad agganciarsi e a formare una zona di contatto stretta. Lavori precedenti hanno mostrato che quando i tumori perdono CD58, le CAR T faticano a stabilire questo contatto e diventano meno efficaci. In questo studio, i ricercatori si sono posti una domanda più profonda: oltre a questo problema meccanico del contatto, come riconfigura la perdita di CD58 la biologia interna delle CAR T così da smorzarne le prestazioni nel tempo?
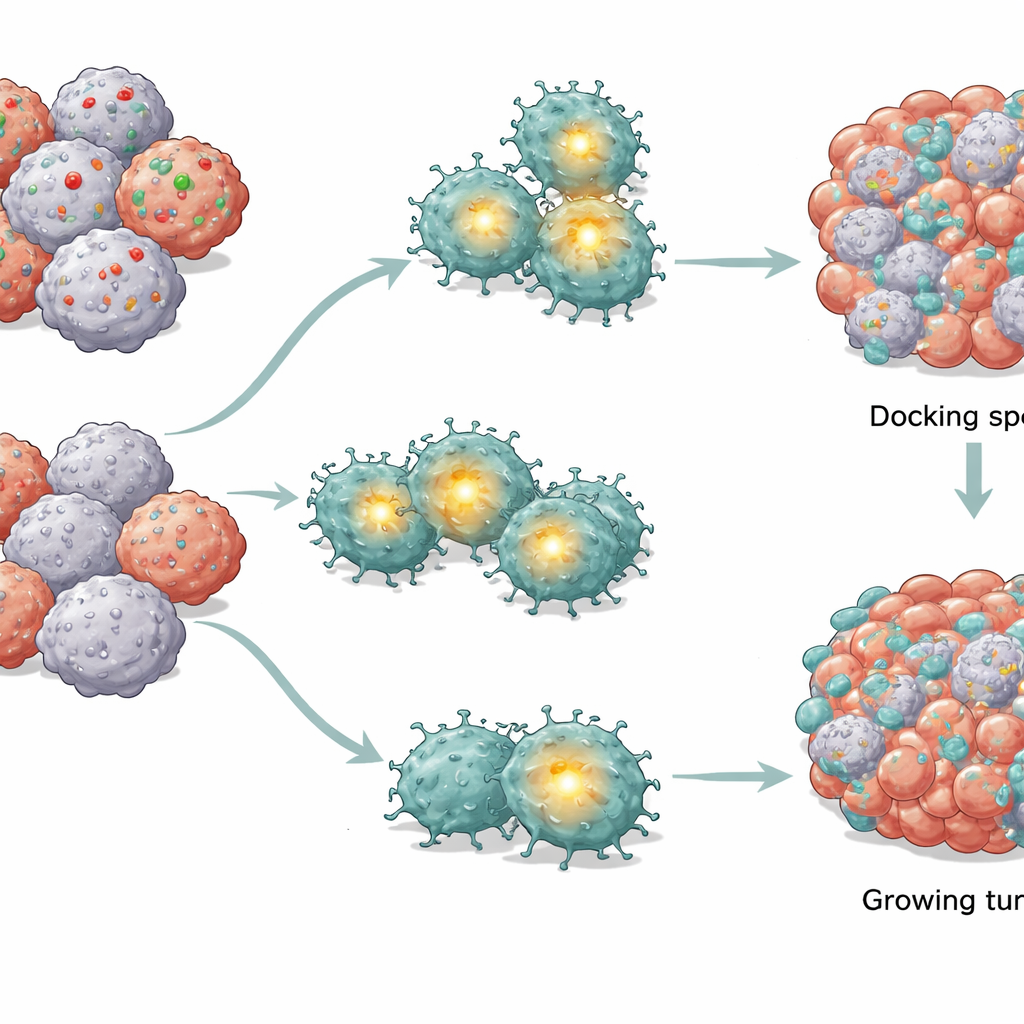
Cortocircuito interno nelle CAR T
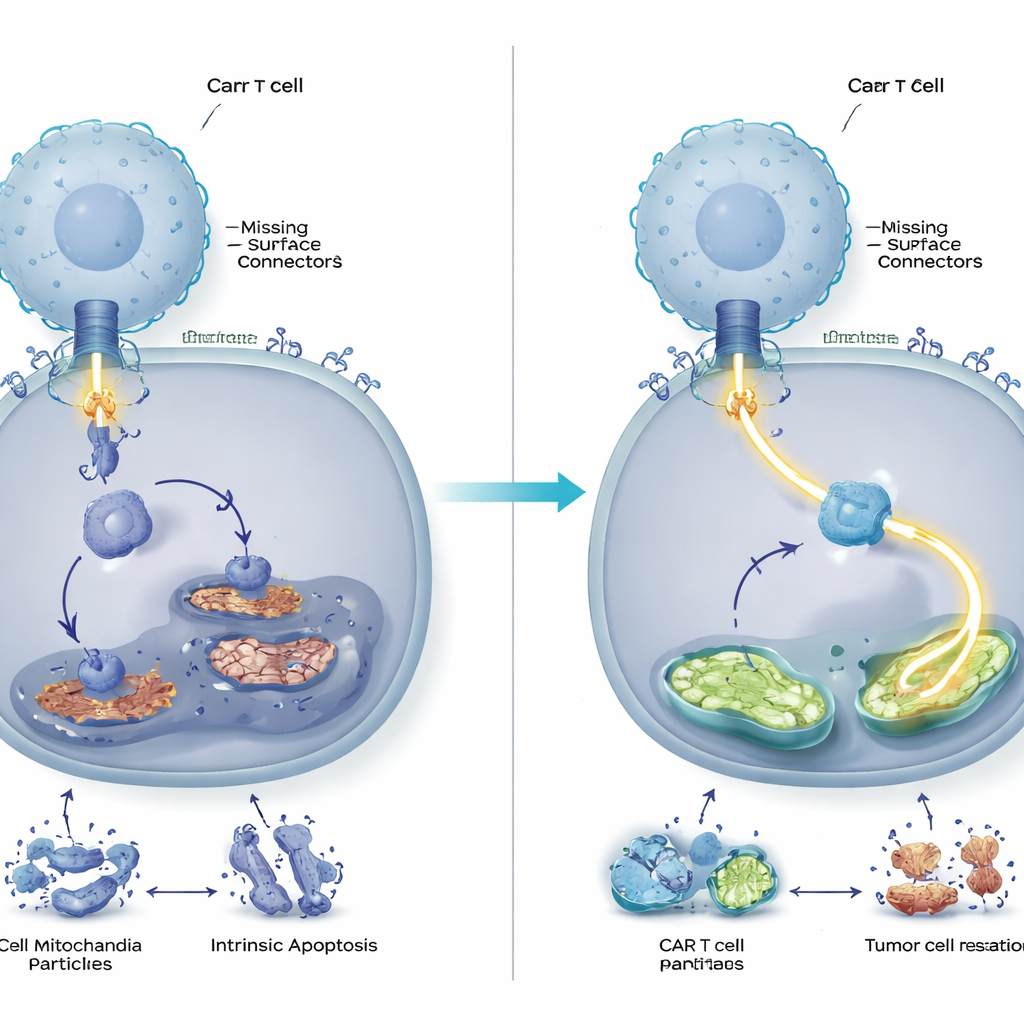
Confrontando CAR T esposte a tumori normali con quelle confrontate a tumori privi di CD58, il team ha scoperto che un hub di controllo chiave all’interno delle cellule T — chiamato AP-1 — risultava selettivamente indebolito, mentre altri principali percorsi di segnalazione restavano sostanzialmente intatti. AP-1 è un complesso di proteine che attivano geni coinvolti nell’attivazione e nella sopravvivenza. Quando l’attività di AP-1 calava, le CAR T mostravano segni tipici di una crisi energetica interna: mitocondri meno numerosi e più piccoli (i loro impianti energetici), ridotta capacità di consumare ossigeno e utilizzare zuccheri, e perdita del potenziale elettrico attraverso le membrane mitocondriali. Contemporaneamente, si accumulavano specie reattive dell’ossigeno dannose. Questi cambiamenti spingevano insieme le CAR T verso un programma di autodistruzione basato sul danno mitocondriale interno, anche in assenza di segnali esterni di morte.
Spegnere un freno interno
Per capire perché AP-1 fosse tanto attenuato, i ricercatori hanno cercato a monte dei “freni” molecolari che potessero essere iperattivi. Hanno scoperto che le CAR T esposte a tumori privi di CD58 aumentavano l’espressione di diverse fosfatasi — enzimi che spengono le vie di segnalazione — in particolare una chiamata DUSP6. Usando farmaci e in seguito un editing genetico preciso per bloccare questi enzimi, hanno constatato che la rimozione di DUSP6 era quella che più efficacemente riattivava AP-1. Le CAR T con DUSP6 eliminato si espandevano meglio, formavano più mitocondri, metabolizzavano il carburante in modo più efficiente, producevano più molecole citolitiche antitumorali e tendevano meno all’apoptosi, soprattutto quando sfidate ripetutamente da cellule tumorali prive di CD58.
Controllo tumorale più forte e duraturo negli animali
Il team ha poi testato se questo aggiustamento molecolare avesse rilevanza in sistemi viventi. In topi portatori di cellule di tumore ematologico umano che esprimevano o meno CD58, le CAR T prive di DUSP6 hanno eliminato i tumori in modo più efficace e li hanno tenuti sotto controllo più a lungo rispetto alle CAR T convenzionali. Le cellule ingegnerizzate si moltiplicavano con maggiore vigore, mostravano meno marcatori di esaurimento e secern evano livelli più alti di messaggeri immunitari chiave. È importante notare che i benefici della rimozione di DUSP6 si osservavano non solo quando i tumori erano privi di CD58, ma anche quando lo conservavano, suggerendo che questa modifica potrebbe migliorare in modo più ampio le terapie con CAR T piuttosto che rappresentare una correzione ristretta per un sottotipo tumorale raro.
Indizi dai dati dei pazienti
Per esplorarne la rilevanza nell’uomo, i ricercatori hanno esaminato dati di espressione genica provenienti da persone trattate con CAR T o con farmaci che modulano i checkpoint immunitari. In pazienti con linfoma a grandi cellule B diffuso trattati con una terapia CAR T a doppio bersaglio, livelli più bassi di DUSP6 nelle cellule T CD8 prima o poco dopo l’infusione erano associati a tassi più elevati di risposta completa. In una coorte separata di melanoma trattata con anticorpi anti-PD-1, le cellule T CD8 esauste dei non responder tendevano a esprimere più DUSP6 rispetto a quelle dei responder. Nel complesso, queste osservazioni suggeriscono che DUSP6 funge da marcatore negativo della fitness delle cellule T attraverso diverse immunoterapie e che la sua riduzione potrebbe migliorare gli esiti.
Cosa significa per le terapie antitumorali future
Per un lettore non specialista, il messaggio è che alcuni tumori sfuggono all’attacco delle CAR T non solo nascondendosi al riconoscimento, ma sabottando i motori interni delle cellule. La perdita della “maniglia” CD58 sulle cellule tumorali abbassa silenziosamente la segnalazione AP-1 nelle CAR T, svuotando i mitocondri, aumentando sottoprodotti tossici e spingendo verso una morte prematura. Rimuovendo il freno rappresentato da DUSP6, gli scienziati possono ripristinare questa segnalazione perduta, riparare la salute mitocondriale e conferire alle CAR T maggiore resistenza e potenza citotossica, anche contro tumori resistenti. Pur richiedendo ulteriori studi di sicurezza e test clinici, l’ablazione di DUSP6 emerge come una promettente strategia di ingegneria per rendere le terapie cellulari viventi più potenti, più durature e potenzialmente efficaci per una platea più ampia di pazienti.
Citazione: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Parole chiave: Cellule CAR T, CD58, DUSP6, immunoterapia del cancro, metabolismo delle cellule T