Clear Sky Science · it
Scatenare il potenziale della via STING mediata da nanobombe bimetalliche per potenziare gli engager bispecifici delle cellule T nella foto-immunoterapia del cancro colorettale
Rivoltare il sistema immunitario contro il cancro del colon
I tumori del colon e del retto sono diffusi e spesso letali, in parte perché imparano a nascondersi dal sistema immunitario. Questo studio esplora una nuova strategia che racchiude diversi strumenti anti‑tumore in una piccola “nanobomba” per risvegliare le difese dell’organismo, aiutare le cellule immunitarie a trovare il tumore e impedire che il cancro ritorni o si diffonda.
Perché gli immunoterapici attuali necessitano di miglioramenti
Una classe promettente di farmaci oncologici, chiamata engager bispecifico per cellule T, funziona come un cupido biologico: un’estremità afferra una cellula T (un’arma chiave del sistema immunitario) e l’altra si aggancia a un marcatore sulla cellula tumorale, mettendole in contatto diretto così che la cellula T possa uccidere il tumore. Pur essendo molto efficaci nei tumori del sangue, questi farmaci faticano nei tumori solidi come quello colorettale. Vengono eliminati rapidamente dall’organismo, possono attaccare tessuti sani che esprimono lo stesso marcatore e spesso si scontrano con tumori “freddi” che non contengono abbastanza cellule immunitarie perché il trattamento funzioni. Perciò medici e ricercatori cercano modi per somministrare questi farmaci in modo più sicuro e trasformare i tumori freddi in tumori “caldi” pieni di cellule immunitarie attivate.
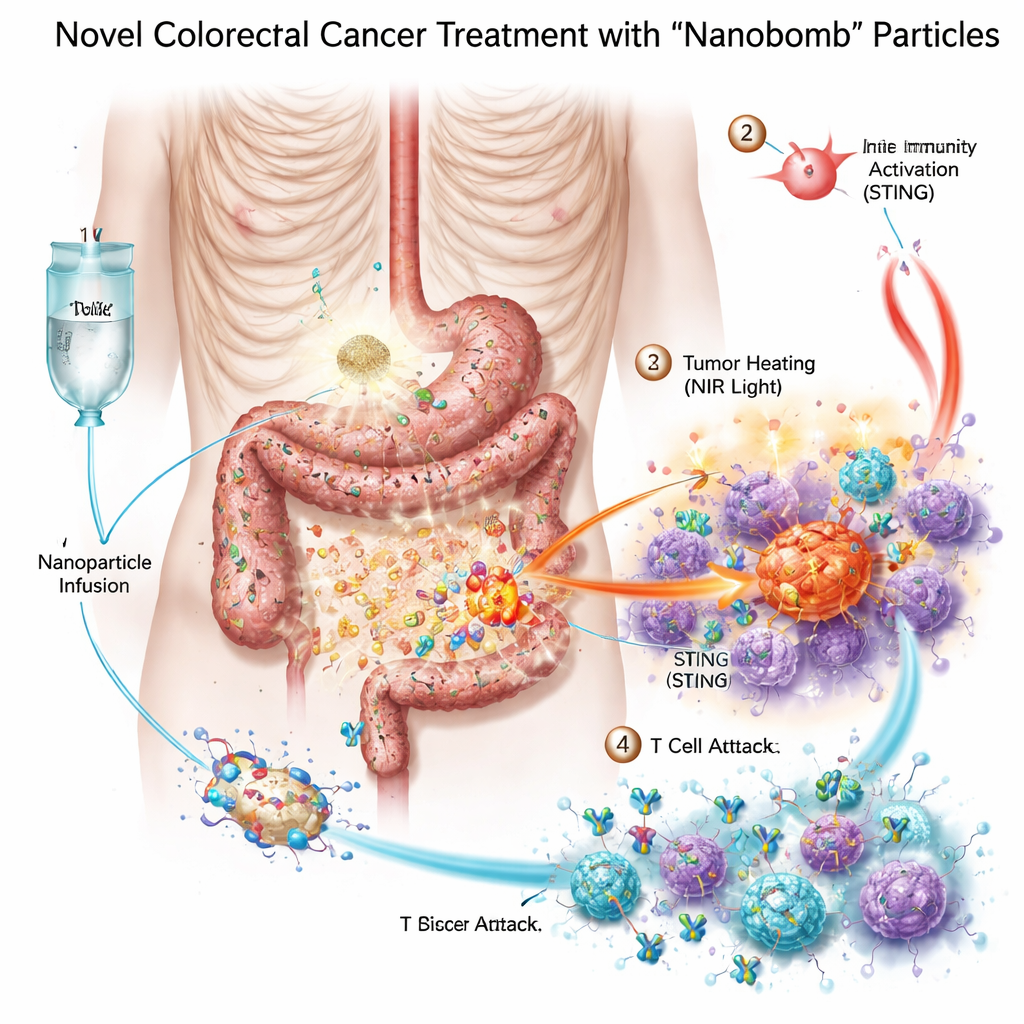
Tre armi in una piccola “nanobomba”
I ricercatori hanno progettato una nanobomba bimetallica—denominata scientificamente MnO2/Co‑DA@BiTE/HPT—che combina tre modalità terapeutiche in una particella. Innanzitutto, il nucleo contiene manganese e cobalto, metalli capaci di attivare un sistema d’allarme cellulare chiamato via STING, il quale aiuta l’organismo a percepire il pericolo e richiamare le cellule immunitarie. In secondo luogo, la superficie della particella è rivestita con un engager bispecifico per cellule T che connette le cellule T alle cellule tumorali. Terzo, il materiale assorbe la luce nel vicino infrarosso, permettendo ai medici di riscaldare il tumore dall’esterno con una forma di fototerapia termica. Per far sì che le nanobombe si dirigano verso le cellule del cancro colorettale, il gruppo ha aggiunto un breve frammento di DNA, un aptamero, che riconosce PD‑L1, una molecola spesso abbondante su questi tumori. Una volta che le particelle raggiungono il tumore, enzimi naturali presenti nel tessuto tumorale le degradano e rilasciano il loro carico proprio dove è necessario.
Riscaldare, allertare e reclutare l’esercito immunitario
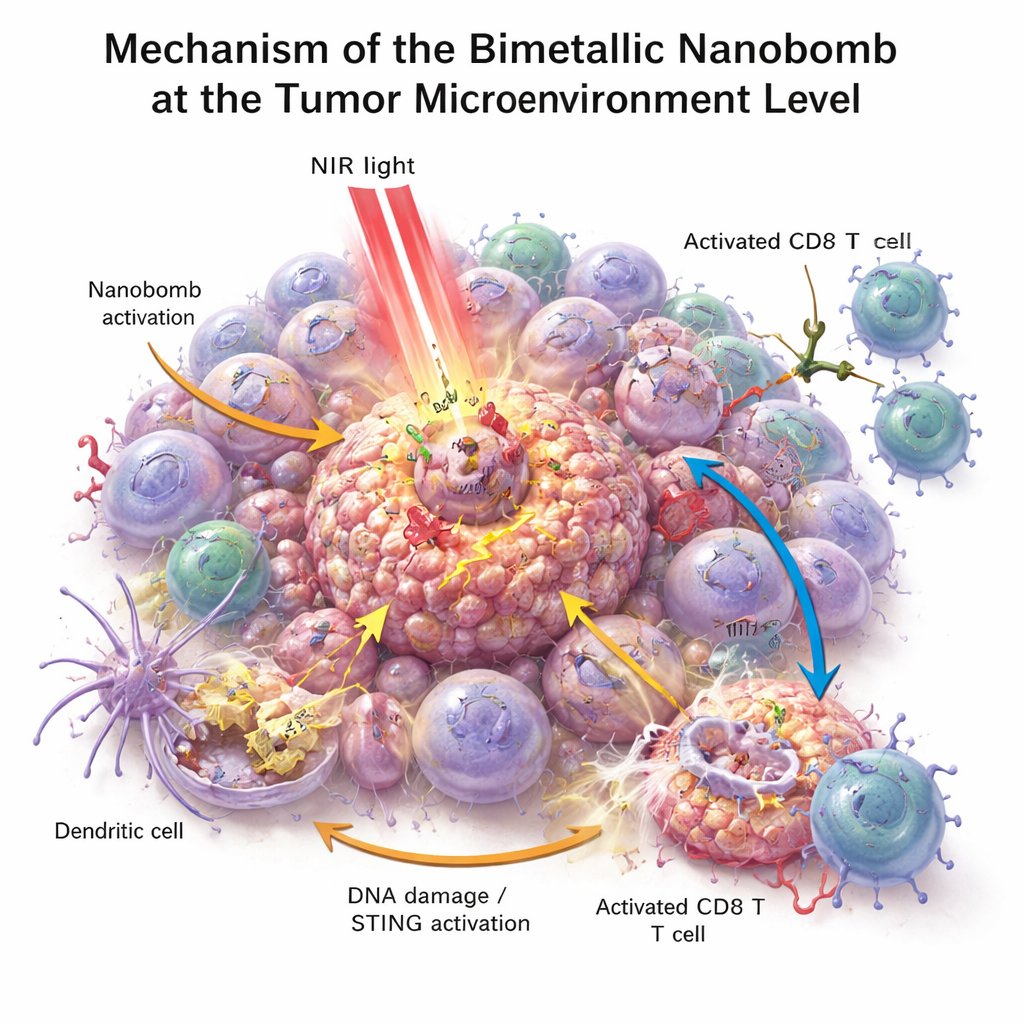
In provetta, le nanobombe uccidevano le cellule del cancro colorettale in modo più efficace di ciascun componente singolarmente. Quando illuminate con luce nel vicino infrarosso, le particelle si riscaldavano, stressavano e danneggiavano le cellule tumorali e favorivano la generazione di specie reattive dell’ossigeno—molecole altamente reattive che ulteriormente danneggiano le cellule tumorali. Questo stress provocava rotture del DNA e spingeva le cellule verso una forma di morte particolarmente visibile che emette segnali di “pericolo”. Le cellule immunitarie vicine, in particolare le cellule dendritiche, ingerivano il materiale tumorale morente e attivavano la via STING grazie al rilascio di manganese e cobalto. Esse quindi producevano interferoni e altri messaggeri infiammatori che maturano e attraggono le cellule T. Allo stesso tempo, l’engager bispecifico sulla nanobomba collegava fisicamente le cellule T alle cellule tumorali PD‑L1‑positive, migliorando l’attivazione delle cellule T e la distruzione tumorale anche in tumori precedentemente freddi.
Dalla riduzione del tumore a una memoria immunitaria duratura
In diversi modelli murini—inclusi tumori colorettali sottocutanei, tumori su entrambi i lati del corpo, metastasi polmonari e un modello di recidiva post‑operatoria—le nanobombe più la luce rallentavano fortemente o quasi arrestavano la crescita tumorale. I tumori trattati contenevano molte più cellule T CD8 in grado di uccidere il cancro e meno cellule T regolatorie che normalmente sopprimono le risposte immunitarie. Le cellule dendritiche all’interno dei tumori e nei linfonodi mostravano segni di maturazione, e gli esami del sangue rivelavano livelli elevati di citochine stimolanti il sistema immunitario. È importante sottolineare che i topi che avevano eliminato i tumori dopo il trattamento con le nanobombe erano meglio protetti quando il cancro veniva reintrodotto, e sviluppavano meno metastasi polmonari, dimostrando che la terapia contribuiva a costruire una memoria immunitaria a lungo termine anziché provocare solo una riduzione transitoria del tumore.
Cosa potrebbe significare per la cura del cancro in futuro
Questo lavoro presenta una nanomedicina “a tripla azione” che riscalda i tumori, attiva un allarme interno e guida le cellule T direttamente verso le cellule tumorali, il tutto in una singola particella mirata. Nei topi, questo approccio non solo ha trasformato i tumori colorettali freddi in tumori caldi e infiammati, ma ha anche contribuito a prevenire recidive e diffusione. Pur essendo la tecnologia ancora lontana dall’essere applicata clinicamente—la produzione su scala, la sicurezza a lungo termine e i test sull’uomo restano sfide importanti—offre un modello per trattamenti futuri che combinano materiali intelligenti e farmaci immunoterapici per dare ai pazienti una risposta anticancro più forte e duratura.
Citazione: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Parole chiave: cancro colorettale, immunoterapia, nanoparticelle, via STING, engager bispecifico per cellule T