Clear Sky Science · it
Terapia guidata farmacocinetica–farmacodinamica personalizzata tramite una piattaforma multi-organoidi derivata da cellule staminali pluripotenti indotte nel carcinoma mammario con mutazione NF1
Perché questa ricerca è importante per i pazienti
Molte persone con il cancro assumono farmaci che funzionano bene in alcuni pazienti ma non in altri, e spesso provocano effetti collaterali pesanti. Questo studio descrive un nuovo modo per testare i trattamenti antitumorali fuori dal corpo utilizzando mini-organi coltivati in laboratorio a partire dalle cellule della stessa paziente. Il lavoro si concentra su una forma difficile da trattare di carcinoma mammario guidata da alterazioni in un gene chiamato NF1 e mostra come combinare una strategia di riparazione genica con un farmaco mirato potrebbe portare a terapie più sicure, più efficaci e realmente personalizzate.
Costruire una versione in miniatura del corpo della paziente
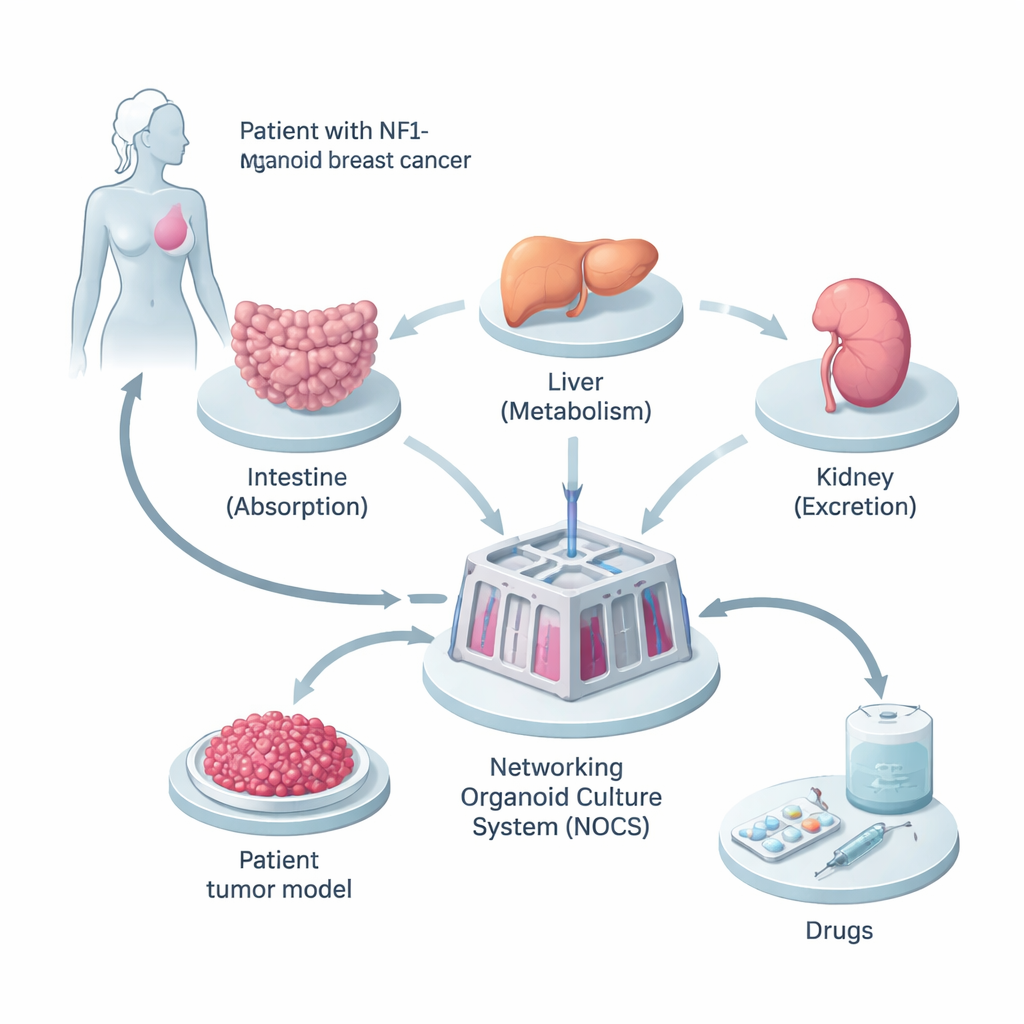
I ricercatori sono partiti da un tessuto prelevato da una donna il cui carcinoma mammario presentava una mutazione ereditaria del gene NF1. Hanno riprogrammato le sue cellule normali simili alla pelle in cellule staminali pluripotenti indotte, che possono diventare quasi qualsiasi tipo cellulare del corpo. Da queste hanno coltivato tre tipi di mini-organi—intestino tenue, fegato e rene—perché sono i siti chiave in cui i farmaci vengono assorbiti, metabolizzati ed eliminati. Parallelamente, hanno creato «sferoidi» tumorali 3D dalle sue cellule cancerose, preservando la miscela di tipi cellulari e le alterazioni genetiche presenti nel tumore originale.
Un circuito vivente per testare i farmaci
Per far comportare questi mini-organi più come un corpo reale, il team li ha collegati in un dispositivo riempito di fluido chiamato Networking Organoid Culture System, o NOCS. In questo sistema, il mezzo fluido scorre tra i compartimenti di intestino, fegato, rene e tumore, imitando la circolazione sanguigna. I farmaci possono essere aggiunti in modo che assomigli all’ingestione di una pillola o a una iniezione, e sensori e pompe controllano la velocità del «sangue» e la frequenza di rinnovo. Ciò ha permesso agli scienziati di tracciare quanto farmaco viene assorbito, quanto rapidamente viene degradato e quanto forte è la sua azione sul tumore—tutto in un modello umano e specifico per la paziente.
Riparare un gene difettoso con l’eson skipping
Il tumore della paziente portava una mutazione dannosa in NF1 che mantiene attive le vie di crescita e rende molti farmaci standard inefficaci. Il team ha progettato brevi frammenti di materiale genetico, chiamati oligonucleotidi antisenso, per indurre la macchina di processamento dell’RNA della cellula a saltare il tratto difettoso (esone 2) del gene NF1. Usando un sistema di veicolazione virale che rimane attivo per giorni, hanno indotto uno «skip degli esoni» stabile nelle cellule tumorali della paziente. Questo ha prodotto una proteina NF1 più corta ma funzionale, ha ridotto i segnali di crescita iperattivi e ha reso le cellule tumorali più sensibili al trattamento.
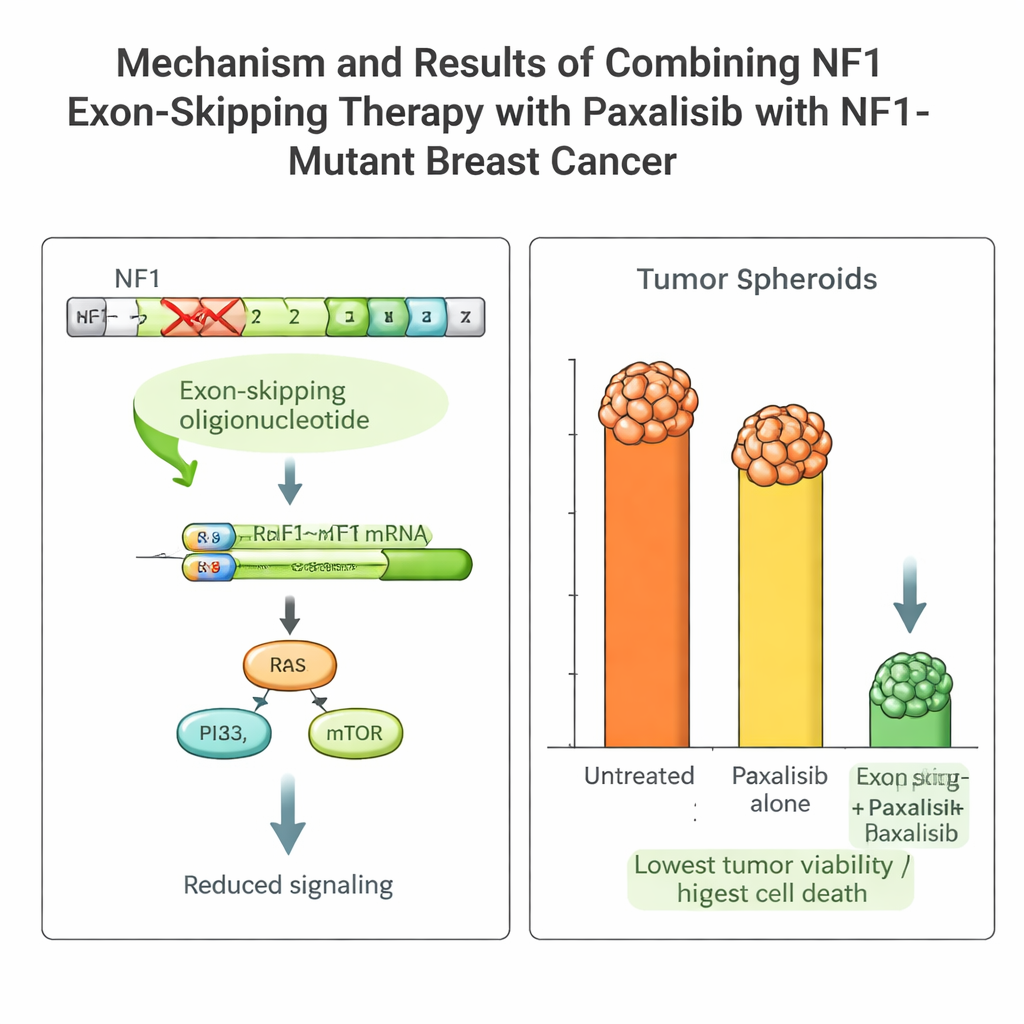
Scegliere il farmaco mirato giusto con la guida PK/PD
Con questa piattaforma, il team ha confrontato diversi farmaci avanzati che bloccano la via PI3K–mTOR, che agisce a valle di NF1. Hanno misurato la farmacocinetica (come l’organismo gestisce il farmaco) e la farmacodinamica (come il farmaco agisce sul tumore) sia nei topi sia nel NOCS. Un farmaco, il Paxalisib, è emerso come particolarmente promettente: veniva assorbito bene nell’intestino, persisteva nel sistema a livelli utili e mostrava un comportamento simile negli animali e nel dispositivo con organoidi. Quando combinato con lo skip dell’esone NF1, il potere citotossico del Paxalisib contro le cellule tumorali della paziente aumentò in modo significativo, con forti riduzioni della crescita e chiari segni di morte cellulare programmata, sia nel NOCS sia in topi impiantati con il tumore della paziente.
Bilanciare vantaggi e rischi tra gli organi
Poiché i modelli di intestino, fegato e rene facevano parte dello stesso circuito, i ricercatori hanno potuto anche osservare segnali precoci di danno agli organi. Il Paxalisib ha provocato risposte di stress e un indebolimento sottile delle barriere nei modelli di intestino e rene e segni di affaticamento nel fegato, ma senza perdita significativa di vitalità cellulare alla dose testata. Questo tipo di visione d’insieme, usando tessuto umano, offre un modo per confrontare le opzioni terapeutiche non solo in base alla loro capacità di ridurre i tumori, ma anche in base a come potrebbero influire sugli organi sani prima che un farmaco raggiunga mai il paziente.
Cosa potrebbe significare per la cura del cancro in futuro
In termini semplici, questo studio dimostra che è ora possibile coltivare un «mini corpo su chip» semplificato e specifico per il paziente che può testare come diversi farmaci—e anche approcci di correzione genica—si comporteranno e interagiranno. Per questa paziente con carcinoma mammario NF1-mutato, la strategia ottimale è stata la combinazione della terapia di skip dell’esone NF1 e del farmaco orale Paxalisib, che insieme hanno rallentato la crescita tumorale molto più di ciascuno da solo. Se sviluppate ulteriormente e testate in più pazienti, piattaforme di questo tipo potrebbero guidare i medici verso piani di trattamento su misura per i geni e la biologia di ciascuna persona, migliorando le probabilità di successo e riducendo la tossicità non necessaria.
Citazione: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Parole chiave: oncologia personalizzata, carcinoma mammario, organoidi, mutazione NF1, terapia mirata