Clear Sky Science · it
Sfruttare le vie immunometaboliche guidate dai lipidi nelle metastasi omentali per potenziare l’immunoterapia nelle pazienti con carcinoma ovarico
Perché il grasso addominale conta nel carcinoma ovarico
Il carcinoma ovarico spesso si diffonde a un grembiule adiposo nell’addome chiamato omento. Quest’area è ricca di adipociti e cellule immunitarie, e si rivela molto più di un semplice spettatore passivo. Lo studio sintetizzato qui mostra che il modo in cui le cellule immunitarie usano e gestiscono i lipidi in questi depositi omentali può aiutare a spiegare perché solo una piccola frazione di pazienti trae beneficio dalle immunoterapie moderne. Suggerisce inoltre nuove combinazioni farmacologiche e test basati sull’imaging che potrebbero rendere questi trattamenti efficaci per più persone.
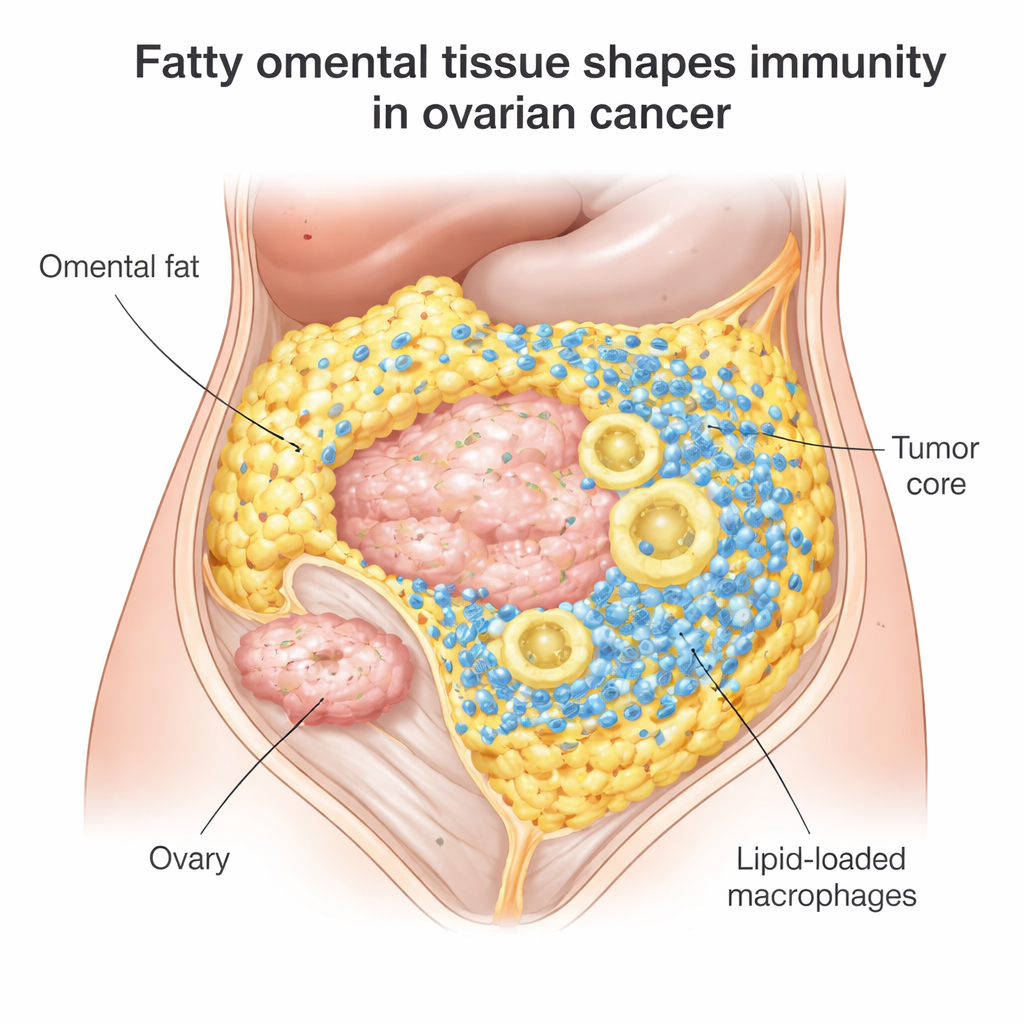
Un campo di battaglia nascosto nel grasso addominale
La maggior parte delle donne con carcinoma ovarico epiteliale risponde inizialmente a chirurgia e chemioterapia, ma nel 70–80% dei casi la malattia recidiva, e farmaci che modulano i checkpoint immunitari come nivolumab o pembrolizumab aiutano solo circa il 10–15%. I ricercatori si sono concentrati sulle metastasi omentali, un sito comune in cui il tumore si impianta tra le cellule adipose. Esaminando più di 100 campioni tumorali, hanno scoperto che i tumori omentali erano pieni di cellule immunitarie: linfociti T citotossici in grado di attaccare il cancro e grandi cellule spazzine chiamate macrofagi. C’era però un problema. Questi T tendevano a raggrupparsi al margine tra tumore e grasso, invece di penetrare il nucleo tumorale dove servirebbero di più.
Il grasso che alimenta alcune cellule immunitarie ma ne sovraccarica altre
Approfondendo, il gruppo ha mostrato che i T in questi tumori adiposi si adattano all’ambiente locale captando lipidi, cioè grassi, dalle cellule adipose vicine. Questo sembra mantenerli metabolicamente “in forma”: l’attività genica e i test di laboratorio indicavano che erano capaci di riconoscere e uccidere le cellule tumorali della paziente. Allo stesso tempo, molti macrofagi associati al tumore nell’omento erano fortemente carichi di goccioline lipidiche. Questi macrofagi intrisi di lipidi mostravano segni di elevato stress ossidativo—usura chimica legata a specie reattive dell’ossigeno—andavano verso uno stato immunosoppressivo e di supporto al tumore. In altre parole, lo stesso ambiente ricco di grasso che può nutrire T efficaci spinge anche i macrofagi in una modalità dannosa che smorza l’attacco immunitario complessivo.
Riprogrammare i macrofagi sovralimentati con farmaci esistenti
Gli scienziati si sono poi chiesti se fosse possibile riconvertire questi macrofagi stressati in alleati. Utilizzando frammenti tumorali freschi coltivati in laboratorio, hanno testato due approcci. Uno ha impiegato maraviroc, un farmaco anti-HIV che blocca CCR5, un recettore per il segnale immunitario CCL5, abbondante al confine tumore–grasso. L’altro bloccava CD36, un recettore “spazzino” chiave che permette ai macrofagi di importare acidi grassi. Entrambi i trattamenti hanno ridotto il carico lipidico all’interno dei macrofagi, abbassato i marcatori di stress ossidativo e di perossidazione lipidica dannosa, e scatenato ondate di segnali infiammatori. In modo cruciale, hanno permesso ai linfociti T citotossici di moltiplicarsi e di spostarsi dal bordo grasso verso il nucleo tumorale, potenziando l’attività immunitaria locale senza aggiungere cellule immunitarie esterne.
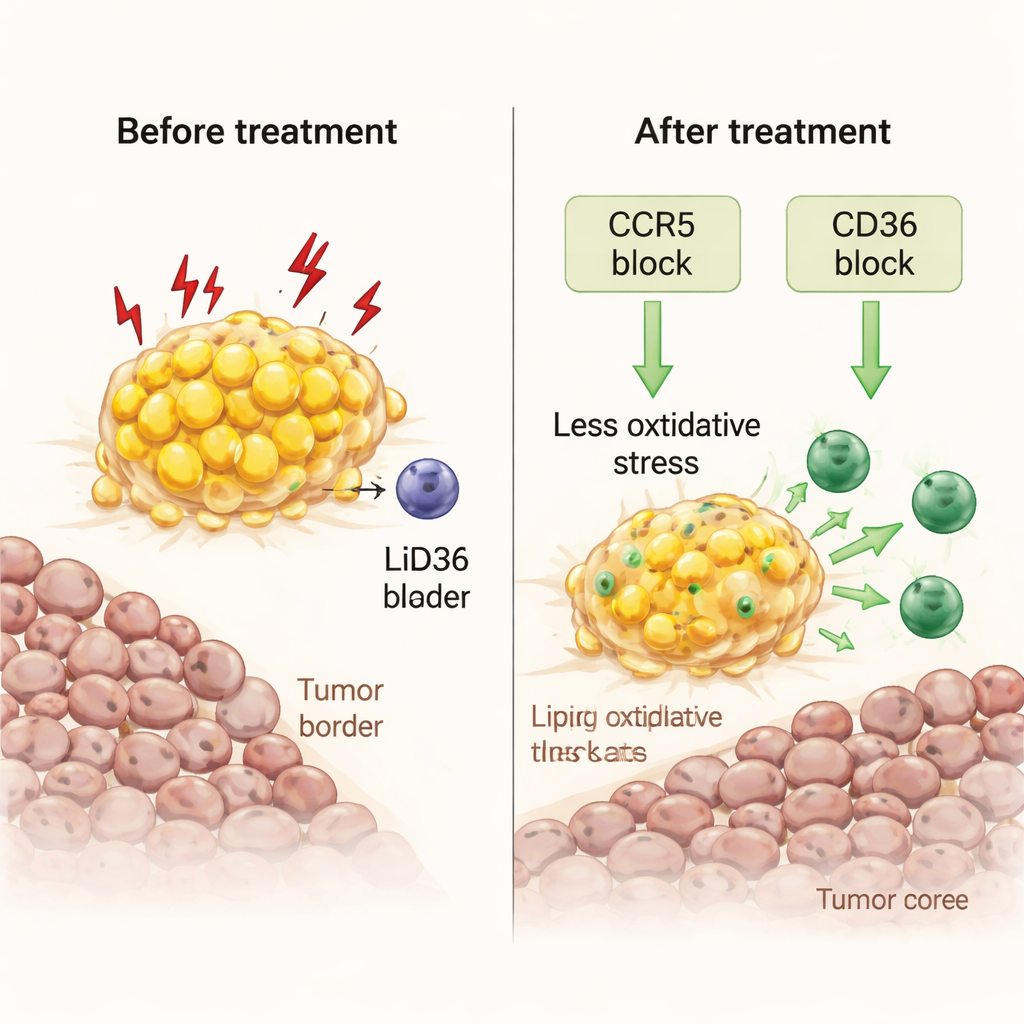
Dalle vie cellulari ai modelli realistici e ai pazienti
Per mettere alla prova queste idee in un contesto più realistico, il gruppo ha usato topi umanizzati ingegnerizzati per portare un sistema immunitario di tipo umano e li ha impiantati con tumori mammari umani in tessuto ricco di grasso. Il trattamento con maraviroc ha riprogrammato i macrofagi umani in questi animali in modi rispecchianti i campioni derivati dai pazienti: riduzione dei segni lipidici e di stress, maggiore produzione di citochine e supporto più forte per le vie correlate ai T. Sul piano clinico, i ricercatori hanno riesaminato uno studio giapponese su nivolumab per il carcinoma ovarico resistente alla chemioterapia. Ogni paziente che aveva beneficiato del farmaco presentava metastasi omentali visibili nei campioni chirurgici. Usando TC o risonanza magnetica combinate con analisi di machine learning della distribuzione del grasso corporeo, hanno costruito un albero decisionale in grado di segnalare in modo non invasivo i pazienti i cui tumori probabilmente si trovano vicino al grasso viscerale—e in un caso prospettico questo metodo ha previsto correttamente una paziente che in seguito ha risposto a nivolumab.
Cosa potrebbe significare per i trattamenti futuri
Per il non specialista, il messaggio principale è che “dove” il carcinoma ovarico cresce nel corpo, e come il grasso vicino rimodella le cellule immunitarie, può influenzare fortemente se l’immunoterapia funziona. I depositi omentali ricchi di grasso sembrano ospitare T vigorosi ma anche macrofagi sovralimentati e stressati che attenuano l’attacco. Alleggerendo il carico lipidico in questi macrofagi e riducendo il loro disagio ossidativo—usando bloccanti di CCR5 come maraviroc, agenti mirati su CD36 o strategie affini—potrebbe essere possibile trasformare una risposta immunitaria parzialmente bloccata in un’assalto a tutto campo contro il tumore. Allo stesso tempo, misure di imaging sull’interessamento omentale potrebbero aiutare i medici a selezionare i pazienti più probabilmente beneficiari dei farmaci checkpoint, offrendo un approccio più personalizzato e potenzialmente più efficace per trattare il carcinoma ovarico.
Citazione: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Parole chiave: carcinoma ovarico, grasso omentale, immunoterapia, macrofagi associati al tumore, metabolismo lipidico