Clear Sky Science · it
GPR54 regola lo sviluppo del carcinoma polmonare non a piccole cellule tramite la dopa decarbossilasi
Perché questa scoperta sul cancro ai polmoni conta
Il cancro ai polmoni resta uno dei tumori più letali e la maggior parte dei casi è una forma chiamata carcinoma polmonare non a piccole cellule (NSCLC). Molti pazienti esauriscono infine le opzioni terapeutiche efficaci perché i tumori si adattano o diventano resistenti ai farmaci attuali. Questo studio mette in luce un sistema di controllo interno alle cellule del tumore finora poco considerato, incentrato su un recettore chiamato GPR54 e su un enzima chiamato dopa decarbossilasi (DDC). Comprendendo come queste molecole favoriscono la crescita e il sostentamento dei tumori, i ricercatori indicano nuove strategie per rallentare o addirittura ridurre l’NSCLC.
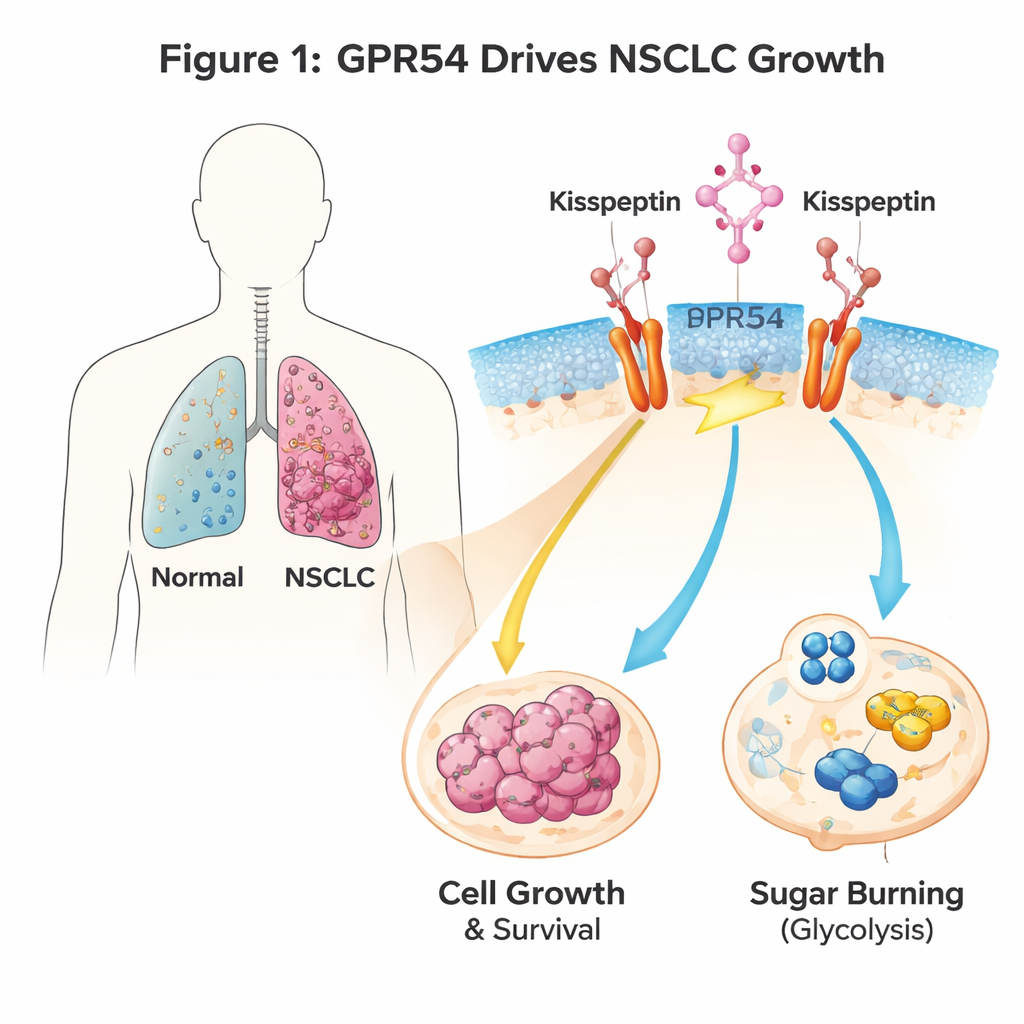
Un interruttore di segnale sulle cellule tumorali polmonari
GPR54 è un sensore che si trova sulla superficie cellulare e risponde a un segnale naturale chiamato kisspeptina. È noto soprattutto per ruoli nella pubertà e nella riproduzione, ma compare anche in molti tumori. Gli autori hanno utilizzato topi geneticamente modificati che sviluppano NSCLC quando un gene oncogenico chiamato Kras viene attivato nelle cellule polmonari. Eliminando il gene Gpr54 in questi animali, gli animali hanno vissuto più a lungo, hanno sviluppato tumori polmonari meno numerosi e più piccoli e le loro cellule tumorali hanno mostrato chiari segni di autodistruzione (apoptosi). Linee cellulari umane di NSCLC hanno raccontato la stessa storia: quando i livelli di GPR54 sono stati ridotti, le cellule tumorali crescevano più lentamente, formavano meno colonie e morivano più facilmente, indipendentemente dalle loro specifiche mutazioni genetiche.
Come GPR54 mantiene vive le cellule tumorali
Approfondendo, i ricercatori hanno indagato quali circuiti interni utilizzi GPR54. Hanno scoperto che GPR54 alimenta due grandi vie di crescita nella cellula, note come AKT ed ERK. Entrambe sono “hub” di segnalazione comuni che spingono le cellule tumorali a dividersi e a resistere alla morte. Quando GPR54 è stato bloccato o rimosso, l’attività di AKT ed ERK è diminuita e le cellule sono diventate più inclini all’apoptosi. Ripristinare segnali AKT o ERK forti poteva in parte salvare le cellule, confermando che GPR54 aiuta le cellule NSCLC a sopravvivere appoggiandosi a questi circuiti di crescita.
Rimodellare come il cancro usa lo zucchero
Le cellule tumorali spesso riprogrammano l’uso dei nutrienti, privilegiando la rapida degradazione degli zuccheri (glicolisi) per alimentare la crescita. Il profilo di espressione genica dei tumori di topo privi di Gpr54 ha mostrato che molti geni coinvolti nella gestione degli zuccheri e nella produzione di energia erano attenuati. Nelle cellule di carcinoma polmonare trattate con kisspeptina per attivare GPR54, le misure dell’uso di ossigeno e della produzione di acido — proxy del metabolismo energetico — hanno rivelato che GPR54 aumenta la glicolisi. Bloccare la via di segnalazione di GPR54 a vari livelli (l’interruttore Gαq/11, PI3K, AKT o mTOR) ha ridotto il consumo di glucosio e la produzione di lattato e ha spinto le cellule verso l’apoptosi. In termini semplici, GPR54 aiuta le cellule NSCLC a bruciare zucchero più rapidamente ed efficientemente, sostenendo la loro rapida crescita.
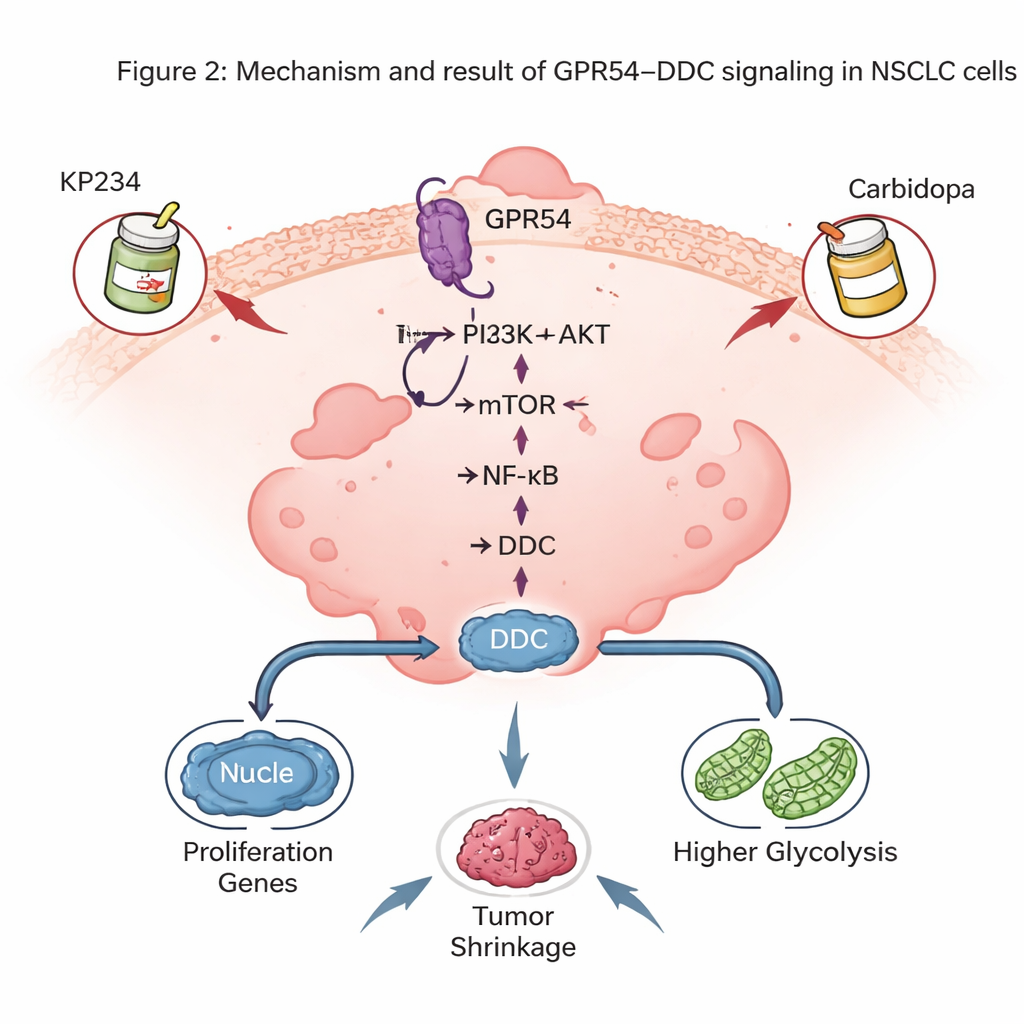
Il ruolo sorprendente di un enzima associato al cervello
Una delle scoperte più sorprendenti è che GPR54 controlla i livelli di DDC, un enzima noto soprattutto per produrre i neurotrasmettitori dopamina e serotonina. Nei tumori murini, i livelli di DDC seguivano da vicino la quantità di GPR54: meno GPR54 significava meno DDC. Anche i tumori e le linee cellulari umane di NSCLC mostravano livelli di DDC più elevati rispetto alle cellule polmonari normali, e i pazienti con più DDC avevano una sopravvivenza peggiore. Ridurre l’espressione di DDC nelle cellule tumorali polmonari rallentava la crescita tumorale nei topi, riduceva la divisione cellulare in coltura e scatenava più apoptosi. A livello molecolare, DDC contribuiva a mantenere l’attività della via NF-κB, un regolatore principale che promuove la sopravvivenza delle cellule tumorali e l’infiammazione, e supportava anche lo stato di alta glicolisi delle cellule tumorali.
Testare una strategia di combinazione farmacologica
Poiché la DDC è già bersaglio in malattia di Parkinson da un farmaco chiamato carbidopa, gli autori hanno esplorato se combinare un inibitore di GPR54 (KP234) con la carbidopa potesse colpire l’NSCLC da due lati. In colture cellulari e in modelli murini in cui cellule umane di NSCLC erano cresciute nel polmone, il trattamento duale ha ridotto la crescita tumorale più di ciascun farmaco da solo e ha aumentato la morte delle cellule tumorali, senza perdita di peso evidente negli animali. Queste combinazioni hanno mostrato promettenti risultati anche in associazione con alcuni farmaci mirati moderni diretti contro geni RAS mutati, suggerendo che la segnalazione GPR54–DDC può essere sovrapposta alle terapie di precisione esistenti.
Cosa significa per la cura futura del cancro polmonare
Per il pubblico non specializzato, il messaggio chiave è che le cellule NSCLC dipendono da una collaborazione finora poco considerata tra un interruttore di superficie (GPR54) e un enzima metabolico (DDC) per restare vive e metabolizzare rapidamente il carburante. Interrompere questa collaborazione indebolisce i tumori, facendoli crescere più lentamente e morire più facilmente nei modelli sperimentali. Sebbene molto lavoro rimanga prima che tali strategie arrivino in clinica, questo studio pone GPR54 e DDC come potenziali biomarcatori per identificare NSCLC aggressivi e come promettenti bersagli per nuove terapie combinate che potrebbero migliorare gli esiti per i pazienti i cui tumori sfuggono alle terapie standard.
Citazione: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Parole chiave: carcinoma polmonare non a piccole cellule, GPR54, dopa decarbossilasi, metabolismo del cancro, terapia mirata