Clear Sky Science · it
Specie reattive dell'ossigeno (ROS) nel cancro: dal meccanismo alle implicazioni terapeutiche
Quando molecole utili diventano pericolose
All'interno di ogni cellula, piccole scintille chimiche chiamate specie reattive dell'ossigeno, o ROS, vengono costantemente prodotte come parte della vita normale. A livelli appropriati aiutano le cellule a crescere, comunicare e difendersi dai microrganismi. Ma questa rassegna spiega come le stesse molecole possano anche danneggiare il DNA, alterare i circuiti cellulari e guidare la crescita, la diffusione e la resistenza alle terapie del cancro. Comprendere questa “doppia vita” dei ROS sta aiutando gli scienziati a progettare nuove terapie oncologiche che o attenuano lo stress ossidativo dannoso o lo spingono deliberatamente oltre la soglia per uccidere le cellule tumorali.
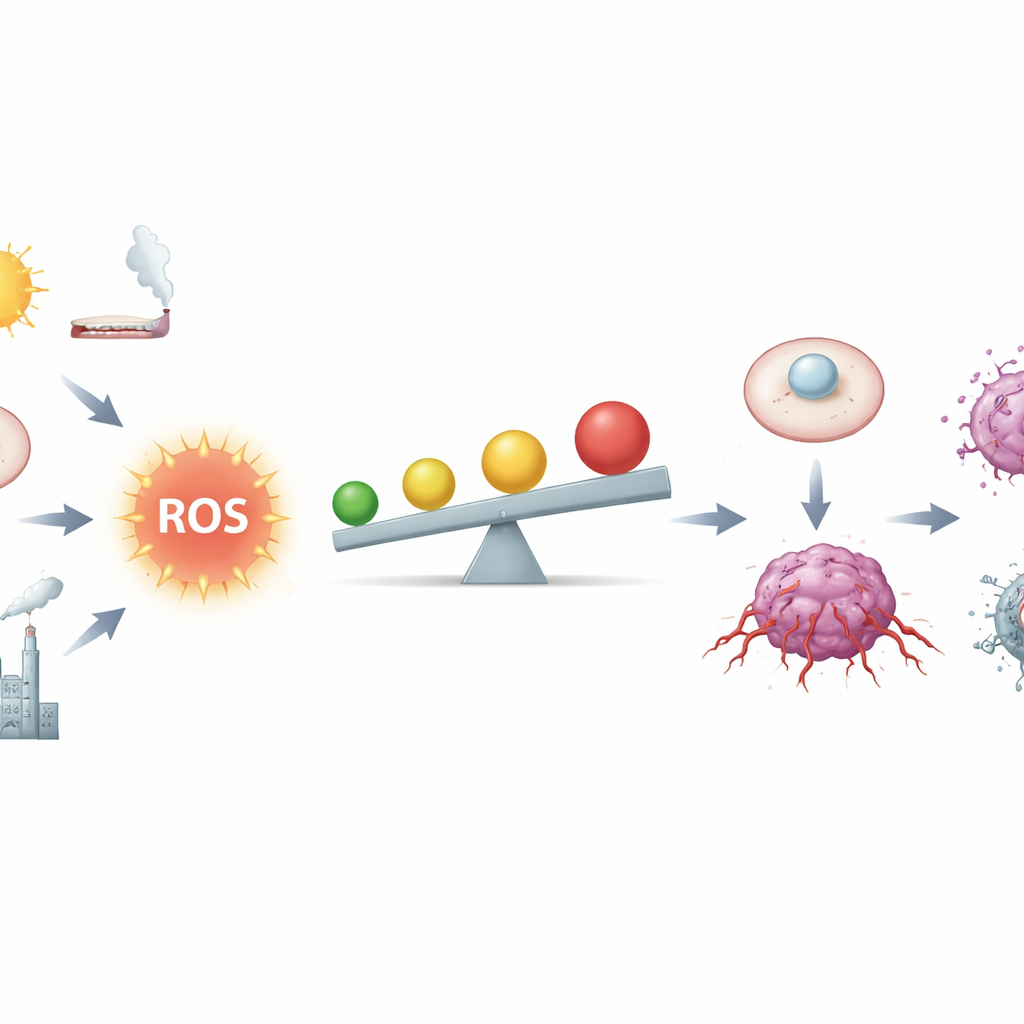
La sottile linea tra carburante e incendio
Gli autori descrivono i ROS come sottoprodotti chimici della respirazione e del metabolismo, ma anche come messaggeri potenti. Nei tessuti sani, piccole quantità di ROS aiutano a controllare il ciclo cellulare, riparare i danni e modulare il sistema immunitario. Le cellule mantengono questi segnali sotto controllo tramite una intricata rete antiossidante, che include molecole come il glutatione ed enzimi regolati da un interruttore maestro chiamato Nrf2. Le cellule tumorali, tuttavia, vivono più vicine alla zona di pericolo: geni difettosi, mitocondri sovraccarichi, infiammazione cronica, fumo di tabacco, radiazioni e alcuni metalli aumentano i ROS. A livelli moderatamente elevati, i ROS possono lesionare il DNA, destabilizzare i cromosomi e attivare cronicamente circuiti di crescita e sopravvivenza, facilitando la trasformazione di una cellula normale in una cellula cancerosa.
Come lo stress ossidativo modella il comportamento del tumore
Una volta che un tumore è instaurato, i ROS continuano a plasmare la sua biologia. Uno stress ossidativo moderato attiva molte vie di crescita che incoraggiano le cellule a dividersi, a sviluppare vasi sanguigni, a invadere i tessuti circostanti e a resistere alla chemioterapia. I ROS possono riprogrammare l'uso di zuccheri, grassi e amminoacidi da parte delle cellule tumorali, indirizzando il combustibile verso vie che producono potere antiossidante aggiuntivo e mattoni per nuove cellule. Influenzano anche le decisioni sul destino cellulare: a seconda dell'intensità e del contesto, i ROS possono inclinare l'equilibrio verso segnali di sopravvivenza o verso una delle varie forme di morte cellulare programmata, inclusa l'apoptosi classica e forme più recenti come la ferroptosi, la necroptosi e la cuproptosi. Questo rende i ROS sia complici della progressione tumorale sia potenziali inneschi dell'autodistruzione del tumore.
Rimodellare l'immunità e la risposta ai farmaci
La rassegna sottolinea che i ROS non agiscono solo all'interno delle cellule tumorali: rimodellano il quartiere del tumore. Un elevato stress ossidativo può esaurire o uccidere le cellule T e le cellule natural killer che combattono il cancro, mentre favorisce cellule soppressive che proteggono il tumore dall'attacco. I ROS aiutano inoltre i tumori ad aumentare segnali del tipo “non uccidermi”, come le proteine di checkpoint, attenuando gli effetti dell'immunoterapia. Allo stesso tempo, livelli moderati di ROS possono favorire la resistenza ai farmaci potenziando pompe di efflusso e risposte allo stress, permettendo alle cellule tumorali di espellere la chemioterapia o riparare i danni che essa provoca. Tuttavia, in altre condizioni, spingere i ROS oltre una soglia critica può smantellare queste difese e riportare i tumori a essere sensibili ai trattamenti.
Trasformare la debolezza redox in una strategia terapeutica
Dal momento che le cellule tumorali camminano su un filo tra l'uso dei ROS e la loro tossicità, gli autori vedono l'equilibrio dei ROS come una leva terapeutica. Una strategia ampia è ridurre i ROS dannosi o rafforzare gli antiossidanti, principalmente per la prevenzione o per proteggere i tessuti sani durante il trattamento. Un'altra è fare il contrario nei tumori: inibire i sistemi antiossidanti o aumentare la produzione di ROS finché le cellule tumorali non superano una soglia letale, specialmente in combinazione con radiazioni, farmaci mirati o immunoterapia. Un terzo approccio è lasciare inalterati i livelli di ROS ma bloccare gli interruttori specifici sensibili ai ROS — proteine di segnalazione, enzimi metabolici o vie di morte — su cui i tumori fanno affidamento. Attraverso queste idee passa il tema della personalizzazione: diversi tumori presentano differenti “firme redox”, perciò le terapie future potrebbero richiedere test ematici o tissutali di danno ossidativo, capacità antiossidante e geni legati ai ROS per scegliere il trattamento redox-target giusto per ogni paziente.
Cosa significa questo per i pazienti
In termini semplici, questo articolo sostiene che i ROS non sono né totalmente cattivi né totalmente buoni; sono strumenti potenti che le cellule, e i tumori, utilizzano. Le cellule tumorali tendono a operare più vicine a un punto di svolta dello stress ossidativo rispetto alle cellule sane, il che può creare una finestra terapeutica. Tuttavia, poiché antiossidanti e pro-ossidanti possono aiutare o danneggiare a seconda di dose, tempistica e tipo di tumore, l'uso indiscriminato di integratori o farmaci che aumentano i ROS è rischioso. Gli autori concludono che il futuro risiede in terapie e diagnostiche accuratamente progettate che valutino lo stato redox di ogni tumore e poi modulino i ROS e i sistemi antiossidanti nella giusta misura — o abbassandoli per proteggere i tessuti normali, o aumentandoli per spingere le cellule tumorali oltre il loro punto di rottura.
Citazione: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Parole chiave: specie reattive dell'ossigeno, stress ossidativo, metabolismo del cancro, terapia redox, microambiente tumorale